Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
MOLECULAR MODELING AND SYNTHESIS OF NEW NSAIDS IN THE SERIES OF 1H-PYRIMIDIN-4-ONE DERIVATIVES
В настоящее время для лечения заболеваний, связанных с воспалительными процессами, используется множество НПВС, однако эти препараты обладают различными негативными побочными эффектами. К ним относятся эрозивно-язвенные поражения ЖКТ, диспепсические расстройства, аллергические реакции, нарушения функций печени и почек. Исходя из этого поиск новых НПВС является актуальным.
В более ранних работах было подтверждено противовоспалительное действие ряда 2-стирил- и 2-виниленгетерилпроизводных пиримидин-4-онов [1]. По этой причине значительный интерес вызывает выявление влияния фармакофорных фрагментов производных 4-оксопиримидина на величину противовоспалительного действия. В связи с этим нами был осуществлен поиск и синтез новых НПВС в ряду производных 1Н-пиримидин-4-она.
Материалы и методы исследования
На первом этапе молекулярного конструирования осуществлен анализ биологических свойств виртуальных структур с использованием программы PASS (Prediction of Activity Spectra for Substances). Эта программа позволяет определить вероятность проявления различных фармакологических эффектов прогнозируемыми веществами [2].
Далее, для наиболее перспективных структур был осуществлен молекулярный докинг. В качестве мишени для докинга был выбран фермент циклооксигеназа-2, играющий ключевую роль в механизме воспаления [5]. Модель фермента получена из банка данных протеинов. Докинг проводили программой Molegro Virtual Docker, версии 5.5, использующей один из наиболее точных на данный момент алгоритмов – MolDock Score [6]. Молекулы лигандов предварительно были оптимизированы при помощи программы HyperChem 8, методом молекулярной механики.
Результаты исследования и их обсуждение
Как известно, результаты расчета программы PASS не могут дать полностью достоверную оценку фармакологической активности прогнозируемых струтур. Однако они позволяют предположить наличие либо отсутствие различных видов фармакологических свойств у анализируемых молекул. Осуществлен прогностический анализ около 70 виртуальных 2-винилензамещенных 1H-пиримидин-4-онов. Среди них отобраны наиболее перспективные структуры, характеризующиеся противовоспалительной активностью (Pi > 50 %). Результаты прогноза PASS приведены в табл. 1.
Таблица 1
Прогноз биологической активности 2-виниленпроизводных 2,6-диметил-5-фенил-1Н-пиримидин-4-она
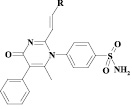
|
Вид биологической активности |
Заместитель |
Соединение |
||||
|
1 |
2 |
3 |
4 |
5 |
||
|
R |
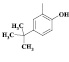
|
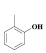
|
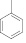
|
-C3H7 |
-C2H5 |
|
|
Pa, % - характеризует вероятность проявления активности |
||||||
|
Агонист D4-рецептора |
80,4 |
83,9 |
88,1 |
86,9 |
87,4 |
|
|
Антипротозойная |
71,6 |
77,0 |
82,0 |
78,6 |
78,7 |
|
|
Ингибитор ЦОГ |
63,3 |
68,8 |
74,1 |
64,4 |
64,6 |
|
|
Нейропротекторная |
55,7 |
49,5 |
56,2 |
41,5 |
39,7 |
|
|
Антиартритная |
48,2 |
47,6 |
50,3 |
38,6 |
39,6 |
|
Исходя из табл. 1, видно, что все приведенные соединения могут обладать противовоспалительной активностью [4]. По этой причине, мы сочли целесообразным провести дальнейший компьютерный скрининг противовоспалительной активности методом молекулярного докинга.
Таблица 2
Энергии взаимодействия лигандов с активным центром ЦОГ-2
|
Лабораторный шифр |
Энергия образования комплекса |
|
1 |
–141,534 |
|
2 |
–135,348 |
|
3 |
–137,573 |
|
4 |
–130,192 |
|
5 |
–136,723 |
|
Диклофенак |
–100,325 |
Известно, что образование более устойчивого лиганд-ферментного комплекса должно приводить к более высокому фармакологическому ответу [3]. В связи с этим оценка результатов молекулярного докинга осуществлялась исходя из энергий взаимодействия между лигандом и ЦОГ-2 – ферментом. Параметры связывания лигандов с сайтом связывания ЦОГ-2 приведены в табл. 2.
Исходя из данных молекулярного докинга, видно, что все анализируемые структуры могут образовывать прочные комплексы с ферментом циклооксигеназа-2. Соединение 3, согласно результатам молекулярного докинга, может образовывать максимально устойчивый лиганд-ферментный комплекс.
Согласно литературным данным, рентгено-структурного анализа комплексов лиганд-ЦОГ-2, доказано, что наиболее значимыми остатками аминокислот сайта связывания с лигандом являются Tyr385 и Ser530 [5]. По результатам молекулярного докинга соединений ряда 2-винилензамещенных производных 4-(2,6-диметил-4-оксо-5-фенил-4H-пиримидин-1-ил)-бензсульфамида, выявлено взаимодействие сульфамидного фрагмента молекул с данными аминокислотами. Можно предположить, что в приведенной конформации соединение-лидер образует устойчивый комплекс за счет водородных связей фенольного гидроксила стирильного фрагмента и атома азота в положении 3 с остатком аминокислоты Tyr355.
Синтез прогнозируемых веществ осуществлялся путем взаимодействия 4-(2,6-диметил-4-оксо-5-фенил-4H-пиримидин-1-ил)-бензсульфамида с ароматическими и алифатическими альдегидами в смеси спирта и диметилсульфоксида по схеме, приведенной ниже.
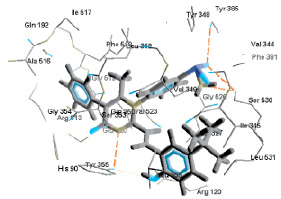
Рис. 1. Расположение соединения-лидера (3) в полости связывания ЦОГ-2
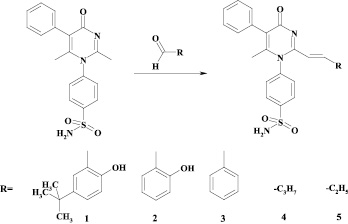
Рис. 2. Схема синтеза целевых соединений
В реакциях винилирования на выход целевых продуктов оказывает влияние зарядовое распределение карбонильной группы альдегидной компоненты. Мы сочли целесообразным выявить зависимость между величиной положительного заряда на атоме углерода карбонильной группы и выход целевого продукта. Расчет зарядов осуществлялся при помощи программы HyperChem 8, методом аb initio с использованием базиса 6-31G. В табл. 3 приведены значения зарядов на атомах углерода и кислорода карбонильной группы и выходы продуктов реакции.
Таблица 3
Сравнение зарядов на кислороде и углероде альдегидной группы с выходами целевых продуктов
|
Соединение |
Заряд |
Выход, % |
|
|
С |
О |
||
|
1 |
0,416 |
–0,523 |
85 |
|
2 |
0,413 |
–0,490 |
76 |
|
3 |
0,405 |
–0,507 |
56 |
|
4 |
0,379 |
–0,490 |
54 |
|
5 |
0,376 |
–0,487 |
48 |
Данные, приведенные в табл. 3, указывают на зависимость выхода целевого продукта от величины положительного заряда на атоме углерода альдегидной группы. Таким образом, можно отметить, что с увеличением заряда на атоме углерода возрастает и выход целевых продуктов, при этом влияние заряда на атоме кислорода на выходы незначительно.
Осуществлено молекулярное конструирование и синтез 2-винилензамещенных производных 2,6-диметил-5-фенил-1Н-пиримидин-4-она, предположительно обладающих выраженной противовоспалительной активностью. В дальнейшем, с целью подтверждения достоверности молекулярного моделирования новых НПВС, будут проведены скрининговые фармакологические исследования.
Рецензенты:
Оганесян Э.Т., д.фарм.н., профессор, заведующий кафедрой органической химии, Пятигорский медико-фармацевтический институт, филиал ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Кодониди И.П., д.фарм.н., доцент, профессор кафедры органической химии, Пятигорский медико-фармацевтический институт, филиал ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Библиографическая ссылка
Сочнев В.С. МОЛЕКУЛЯРНОЕ МОДЕЛИРОВАНИЕ И СИНТЕЗ НОВЫХ НПВС В РЯДУ ПРОИЗВОДНЫХ 1H-ПИРИМИДИН-4-ОНА // Фундаментальные исследования. 2015. № 2-25. С. 5610-5613;URL: https://fundamental-research.ru/en/article/view?id=38472 (дата обращения: 30.04.2026).



