Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
USE OF THE HPLC-METHOD FOR STUDYING OF PHENOLIC COMPOUNDS OF LEAVES OF A SKUMPIYA TANNING (COTINUS COGGYGRIA SCOP.)
Скумпия кожевенная (Cotinus coggygria Scop.) представляет собой ветвистый кустарник или деревце семейства Сумаховые (Anacardiaceae). Произрастает от юга Западной Европы до Китая и Гималаев. На территории России встречается в нижнем течении Дона и повсеместно на территории Северного Кавказа, преимущественно на сухих каменистых склонах, в лесах и зарослях кустарников [4].
Листья скумпии кожевенной являлись сырьём для промышленного получения танина. Наряду с дубильными веществами в сырье скумпии содержится значительное количество флавоноидов, содержание которых в сумме превышает 1 %. Основными компонентами данной группы биологически активных веществ (БАВ) являются мирицетин, кверцетин и кемпферол [2]. На основе содержания в сырье суммы флавоноидных агликонов была разработана фармацевтическая субстанция «флакумин», обладающая желчегонным и спазмолитическим действием [1]. Препараты из сырья растения издавна применяются в народной медицине при заболеваниях кишечника, печени и жёлчевыводящих путей, при кожных заболеваниях и дерматомикозах и др. Экспериментально установлено, что экстракты из листьев обладают антиоксидантными свойствами [6].
Основным сепарационным методом анализа фенольных соединений в растительных объектах является высокоэффективная жидкостная хроматография (ВЭЖХ). Следует также отметить, что данный метод требует наличия большого количества стандартных образцов, особенно в условии отсутствия в сырье одного-двух характеристических компонентов. Учитывая, что в основном фенольные соединения представлены в сырье в виде гликозидов и сложных эфиров небольшого числа агликонов флавоноидов, то одним из решений данной проблемы может служить гидролиз указанных структур до характерного агликона и определение последнего с использованием ВЭЖХ. Это также важно для оценки качества лекарственного растительного сырья, так как качественный и количественный состав гликозидов может быть очень вариабельным в зависимости от места сбора и года заготовки.
Цель исследования – изучение возможности использования ВЭЖХ для анализа фенольных соединений листьев скумпии кожевенной.
Материал и методы исследования
Объектом исследования служили высушенные образцы сырья листьев скумпии кожевенной, заготовленные в 2013 году в фазу цветения растения на юго-восточном склоне горы Машук в городе Пятигорске Ставропольского края.
В работе были использованы стандартные образцы (СО) рутина (CAS 153-18-4), кверцетина (CAS 117-39-5), кемпферола (CAS 520-18-3), гиперозида (CAS 482-36-0), и феруловой кислоты (CAS 1135-24-6) с чистотой более 95 % (производитель – Sigma-Aldrich).
На первом этапе работы необходимо было установить наличие изучаемых фенольных соединений в извлечении из листьев скумпии кожевенной. Для этого около 2 г сырья (точная навеска), измельченного до размера частиц, проходящих сквозь сито с отверстиями диаметром 1 мм, помещали в плоскодонную колбу со шлифом вместимостью 100 мл, заливали 50 мл 70 % спирта этилового и нагревали с обратным холодильником на кипящей водяной бане в течение 1 ч с момента закипания спиртовой смеси в колбе. Полученное извлечение охлаждали до комнатной температуры и фильтровали в мерную колбу вместимостью 50 мл, доводили объем тем же растворителем до метки и перемешивали. Перед вводом в хроматограф извлечение фильтровали через фильтр с диаметром пор 0,25 мкм. Параллельно готовили серию растворов стандартных образцов (СО) рутина, кверцетина, кемпферола, гиперозида и феруловой кислоты в 70 % спирте этиловом.
По 20 мкл извлечения и модельной смеси растворов СО вводили в хроматографическую систему «Стайер» (Аквилон, Россия – США – Чехия), снабженную колонкой «Luna C18» 150×4,6 мм (Phenomenex, США) с размером зерен 5 мкм. Элюирование осуществляли в градиентном режиме. Элюент А – ацетонитрил («Вектон», Россия, ОСЧ 2), элюент В – 2 % раствор кислоты муравьиной («Вектон», Россия, 99 %). Содержание ацетонитрила изменялось от 20 до 60 % за 40 мин, при расходе элюента 1 мл/мин. Детектирование проводили при длине волны 365 нм на УФ-детекторе [3, 5].
Далее необходимо было установить содержание в сырье идентифицированных фенольных соединений. Расчет проводили по площадям пиков соответствующих веществ, полученных при анализе извлечения из скумпии кожевенной и при анализе растворов их стандартных образцов.
Следующим этапом исследования было проведение кислотного гидролиза гликозидов и сложных эфиров флавоноидов. Для этого около 2 г (точная навеска) сырья помещали в колбу со шлифом вместимостью 250 мл, прибавляли 94 мл спирта этилового 70 % и 6 мл концентрированной хлористоводородной кислоты («Вектон», Россия, ОСЧ 20-4). Колбу присоединяли к обратному холодильнику и нагревали на кипящей водяной бане в течение 3 часов. Затем колбу охлаждали до комнатной температуры и фильтровали в мерную колбу вместимостью 100 мл и доводили объем до метки 70 % спиртом. Далее проводили ВЭЖХ-анализ согласно вышеизложенной методике.
Результаты исследования и их обсуждение
В извлечении без проведения гидролиза идентифицировано 5 фенольных соединений: оксикоричные кислоты – феруловая кислота; гликозиды флавоноидов – рутин, гиперозид; агликоны флавоноидов – кверцетин и кемпферол (рис. 1). В извлечении после кислотного гидролиза обнаружено только два исследуемых вещества: агликоны флавоноидов кверцетин и кемпферол (рис. 2).
Проведенная количественная оценка фенольных соединений до и после гидролиза (таблица) свидетельствует, что изучаемое сырье содержит флавоноиды в основном в виде гликозидов (гиперозид, рутин и другие). Данный факт подтверждается также значительным увеличением содержания кверцетина и кемпферола после проведения процедуры гидролиза. Практически полное разрушение феруловой кислоты после гидролиза, возможно, связано с жесткими условиями его проведения.
Результаты анализа фенольных соединений листьев скумпии кожевенной методом ВЭЖХ
|
Вещество |
Содержание, % |
|
|
До гидролиза |
После гидролиза |
|
|
Рутин |
0,076 ± 0,004 |
– |
|
Гиперозид |
0,36 ± 0,02 |
– |
|
Феруловая кислота |
0,75 ± 0,04 |
– |
|
Кверцетин |
0,0130 ± 0,0007 |
1,44 ± 0,07 |
|
Кемпферол |
0,000110 ± 0,000006 |
0,0150 ± 0,0008 |
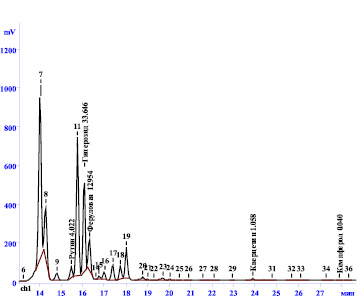
Рис. 1. ВЭЖХ – хроматограмма фенольных соединений листьев скумпии кожевенной из извлечения, полученного без гидролиза
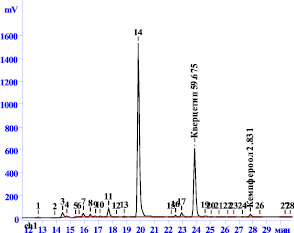
Рис. 2. ВЭЖХ – хроматограмма фенольных соединений листьев скумпии кожевенной из извлечения, полученного после кислотного гидролиза
Выводы
С использованием метода ВЭЖХ идентифицирован ряд фенольных соединений листьев скумпии кожевенной. Преобладающими веществами в извлечении являются гиперозид и феруловая кислота, а также обнаружены кверцетин и кемпферол в незначительных количествах.
В извлечении, полученном после проведения кислотного гидролиза, установлено значительное повышение содержания кверцетина и кемпферола, что свидетельствует о значительном содержании в сырье их производных (гликозиды, сложные эфиры). Использование указанного подхода может быть использовано для оценки качества сырья скумпии кожевенной.
Рецензенты:Коновалов Д.А., д.фарм.н., профессор кафедры фармакогнозии, зам. директора по НИР, Пятигорский медико-фармацевтический институт, филиал, ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск;
Кодониди И.П., д.фарм.н., доцент кафедры органической химии, Пятигорский медико-фармацевтический институт, филиал, ГБОУ ВПО ВолгГМУ Минздрава России, г. Пятигорск.
Работа поступила в редакцию 18.03.2015.
Библиографическая ссылка
Гриценко А.И., Сенченко С.П., Попова О.И. ИСПОЛЬЗОВАНИЕ МЕТОДА ВЭЖХ ДЛЯ ИЗУЧЕНИЯ ФЕНОЛЬНЫХ СОЕДИНЕНИЙ ЛИСТЬЕВ СКУМПИИ КОЖЕВЕННОЙ (Cotinus coggygria Scop.) // Фундаментальные исследования. 2015. № 2-9. С. 1907-1910;URL: https://fundamental-research.ru/en/article/view?id=37331 (дата обращения: 19.05.2026).



