Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
HISTOPLANIMETRIC CHARACTERISTICS OF ASEPTIC WOUND BY DIFFERENT METHODS OF REGIONAL IMPACT
Оптимизация регенерационного процесса представляет большой интерес как для фундаментальных исследований, так и для практической медицины (Нузов Б.Г., 2012). Устранение раневого дефекта и ликвидация нарушения барьерной функции кожи, а также прогнозирование эффективности региональных методов воздействия являются основными направлениями при лечебных мероприятиях с целью восстановления целостности кожных покровов (Бабушкина И.В., 2013; Данилов Р.К., 2008).
Компенсаторно-приспособительные превращения, обеспечивающие купирование патологических процессов, требуют грамотной корректировки. При этом надо учитывать морфологические особенности кожи и анализировать степень влияния хирургических мероприятий и региональной терапии на восстановительные процессы (Глухов А.А., 2010). Клиническая целесообразность должна базироваться на морфологических законах межклеточных взаимодействий (Быков В.Л., 1999). Конечный результат зависит не только от площади раны, силы патогенного воздействия, но и от грамотной координации процессов альтерации, экссудации и пролиферации в области кожных ран.
Цель работы – провести гистопланиметрическую характеристику асептического раневого процесса при различных методах регионального воздействия.
Материалы и методы исследования
Исследования проведены на 308 белых лабораторных крысах-самцах массой 240 ± 12,5 г. Проведено три блока исследований течения раневого процесса в асептических ранах. Первый блок посвящен изучению процессов регенерации под воздействием различных режимов переменного магнитного поля (ПеМП). Второй блок направлен на изучение восстановления тканей под действием светотерапии (СТ) с заданными характеристиками. В третьем блоке оценивали процессы заживления под влиянием обогащенной тромбоцитами плазмы крови (ОТПК).
Для моделирования асептической раны под наркозом («Золитил-100» в дозе 8 мк/кг (согласно инструкции производителя)) на выбритом от шерсти участке наружной поверхности средней трети бедра производили линейный разрез кожи, подкожной жировой клетчатки длиной 1,0 см. Рану закрывали давящей марлевой асептической повязкой; лечение начинали сразу после моделирования. Источником ПеМП выступал модифицированный аппарат магнитотерапии АМТ-01М. Величина индукции магнитного поля – 10 ± 2,5 и 30 ± 2,5 мТл. Форма тока – синусоидальная или пульсирующая с частотой 50 Гц. В первом экспериментальном блоке для оценки регенерации при заживлении асептических кожных ран под воздействием ПеМП животные были разделены на пять групп: одну контрольную и четыре опытные. Схема эксперимента представлена в табл. 1.
Таблица 1
Схема эксперимента для оценки регенерации при заживлении асептических
кожных ран при воздействии ПеМП
|
Группа исследований |
Количество животных |
Характер и продолжительность воздействия |
|
Контрольная |
28 |
Магнитотерапия не проводилась |
|
1 опытная |
28 |
Синусоидальное ПеМП, 10 мТл, 10 мин |
|
2 опытная |
28 |
Синусоидальное ПеМП, 30 мТл, 10 мин |
|
3 опытная |
28 |
Пульсирующее ПеМП, 10 мТл, 10 мин |
|
4 опытная |
28 |
Пульсирующее ПеМП, 30 мТл, 10 мин |
Во втором экспериментальном блоке по изучению регенерации при заживлении асептических ран на фоне светотерапии животные были разделены на три группы – контрольную и две опытные. Схема эксперимента представлена в табл. 2.
СТ раневой поверхности у экспериментальных животных проводилась с помощью аппарата «Биоптрон компакт» («Zepter», Швейцария) с диаметром светового фильтра 4 см. Воздействие на раневую поверхность проводилось на расстоянии 9–10 см под прямым углом падения луча.
В третьем экспериментальном блоке для изучения процессов регенерации при заживлении асептических кожных ран при использовании ОТПК после моделирования раневого дефекта животные были разделены на три группы: контрольную и две опытные. Схема эксперимента представ-
лена в табл. 3.
Таблица 2
Схема эксперимента для оценки регенерации
при заживлении асептических ран на фоне светотерапии
|
Группа исследований |
Количество животных |
Характер и продолжительность воздействия |
|
Контрольная |
28 |
Лечение не проводилось |
|
1 опытная |
28 |
Поляризованное облучение 1 раз в сутки в течение 8 минут |
|
2 опытная |
28 |
Поляризованное облучение 2 раза в сутки в течение 8 минут с интервалом 8 часов |
Таблица 3
Схема эксперимента для оценки регенерации
при заживлении асептических кожных ран под селективным воздействием ОТПК
|
Группы |
Количество животных |
Характер воздействия |
|
Контрольная |
28 |
Дополнительное воздействие не проводилось |
|
1 опытная |
28 |
Гидроимпульсная санация |
|
2 опытная |
28 |
Нанесение ОТПК |
В первой опытной группе проводили гидроимпульсную санацию (ГИС) дефекта тканей 0,9 % раствором хлорида натрия. Во второй опытной группе на ткани наносили ОТПК. Для получения ОТПК из хвостовой вены каждого животного проводили забор 4 мл крови, которую центри-
фугировали при 6000 оборотах в минуту, затем наносили на рану.
Для оценки эффективности применяемых методов регионального воздействия определяли скорость заживления кожных ран, расчет производили по формуле
Vs = So – Sn/n,
где So – исходная площадь раны; Sn – площадь ран в соответствующий экспериментальный срок; n – изучаемый экспериментальный срок. Проведение планиметрического исследования осуществлялось по фотографиям экспериментальных ран в масштабе 1:1, с внесением в поле зрения эталонного объекта для верификации масштаба и последующего расчета пиксель/мм. После определения площади раны в пикселях, путем обводки с использованием инструмента «перо», выполнялся пересчет в мм2.
Для забора гистологического материала животных выводили из эксперимента на 1, 3, 5, 7 сутки для оценки особенностей восстановления тканей в различные периоды регенерационного процесса. Полученный материал фиксировался в 10 % нейтральном формалине с последующим обезвоживанием и заливкой в парафин. Из парафиновых блоков приготавливали срезы толщиной 6–7 мкм, ориентированные строго вертикально и проходящие через все слои стенок и дна раны.
Для оценки реакции клеточного компонента в зоне раневого дефекта изучалась реакция тучноклеточной популяции. Тучные клетки подсчитывали в тканях, окружающих рану, с учетом общего числа и морфофункциональных типов при окраске толуидиновым синим при рН = 5,6. Плотность тучных клеток определяли с помощью светового микроскопа при увеличении 40×10. Подсчет клеток и их типирование проводили в 20 полях зрения с последующим перерасчетом на единицу площади (S = 0,01 мм2).
Функциональную активность тучных клеток оценивали по индексу дегрануляции, который представляет собой отношение числа дегранулированных клеток к общему числу анализируемых клеток, выраженное в процентах. Значение индекса дегрануляции в дальнейшем сравнивалось в экспериментальных и контрольных группах.
Для анализа данных использовались статистические пакеты Statistica 10.0 фирмы StatSoft. Статистическая обработка включала сравнение доли дегранулированных тучных клеток с помощью углового критерия Фишера, полученных средних значений скоростей заживления ран – с помощью непараметрического критерия U-критерий Вилкоксона – Манна – Уитни, различия между группами признавались статистически значимыми при p < 0,05. Для анализа взаимосвязи параметров использовались регрессионный и корреляционный анализы.
Результаты исследования
и их обсуждение
Скорость заживления раневого дефекта демонстрирует тесные корреляционные зависимости с величинами индекса дегрануляции ТК, так как развитие раневого процесса уже в начальной фазе сопровождается изменениями морфофункционального состояния клеток данного дифферона. Данная связь носит нелинейный характер и для каждого вида регионального воздействия можно выделить оптимальные значения индекса дегрануляции, после достижения которого увеличения скорости заживления дефекта не происходит. В асептических ранах под действием различных региональных факторов выявляется общая закономерность – увеличение скорости эпителизации при росте индекса дегрануляции, наиболее ярко эта зависимость выявляется при использовании ОТПК (рис. 1).
а б
Рис. 1. Зависимость скорости заживления раневого дефекта от индекса
дегрануляции в асептических ранах:
а – контрольная группа; б – при региональном воздействии ОТПК
Вне зависимости от используемых видов воздействий отмечается повышение индекса дегрануляции, сопровождавшееся пропорциональным увеличением скорости заживления раневого дефекта, что подтверждает данные (Клименко Н.А., 1995) о стимулирующем влиянии тучноклеточной популяции на репарацию, выражающемся в модулирующем воздействии на клетки воспалительного ряда, а также в активирующем влиянии на фибробласты и, как следствие, на стимуляцию коллагеногенеза.
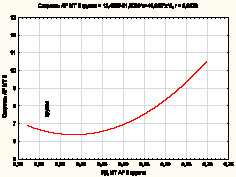
а
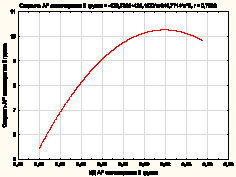
б
Рис. 2. Зависимость скорости заживления раневого дефекта
от индекса дегрануляции в асептических ранах:
а – при региональном воздействии магнитотерапии;
б – при региональном воздействии светотерапии
При применении ОТПК и магнитотерапии увеличение индекса дегрануляции тучных клеток приводило к росту скорости сокращения площади раневого дефекта. Под воздействием светотерапии определялось наличие максимума скорости заживления, соответствующего индексу дегрануляции 62 % после двукратного применения данного фактора, дальнейшее увеличение индекса дегрануляции не приводило к увеличению скорости заживления раневого дефекта.
В целом, для указанных значений индекса дегрануляции тучных клеток и при использовании магнитотерапии, и под воздействием ОТПК, отмечались близкие значения скорости заживления раневого дефекта, но при указанных факторах наблюдалось резкое увеличение скорости эпителизации при дальнейшем повышении индекса дегрануляции тучных клеток, так при индексе дегрануляции, составляющем 85 %, скорость достигала 18 мм2/сут.
Анализ хода регрессионных зависимостей демонстрирует сходство характера скорости изменения планиметрических показателей и величины индекса дегрануляции для спонтанного течения раневого процесса и использования светотерапии. Данное подобие может объясняться более мягким, физиологическим эффектом этого вида регионального воздействия на популяцию тучных клеток, локализующихся преимущественно на субэпидермальном уровне, без вовлечения в реакцию их большей доли из системного пула.
Таким образом, можно предположить, что наиболее мягким эффектом, с точки зрения реакции тучноклеточной популяции при сопоставимых значениях доли дегранулированных клеток, обладает светотерапия, для которой характерно преимущественно поверхностное действие, а тучные клетки расположены в тканях, составляющих пограничную среду организма, поэтому данный клеточный дифферон активно определяет восстановительные реакции, в то время как магнитотерапия и ОТПК в большей степени стимулируют регенерационные процессы, потенцируя функциональную активность тучных клеток системного пула.
Рецензенты:
Воронцова З.А., д.м.н., профессор, заведующая кафедрой гистологии, ГБОУ ВПО «Воронежская государственная медицинская академия им. Н.Н. Бурденко», г. Воронеж;
Корденко А.Н., д.м.н., профессор кафедры анатомии и физиологии, ФГБОУ ВПО «Воронежский государственный педагогический университет», г. Воронеж.
Библиографическая ссылка
Алексеева Н.Т. ГИСТОПЛАНИМЕТРИЧЕСКАЯ ХАРАКТЕРИСТИКА АСЕПТИЧЕСКОГО РАНЕВОГО ПРОЦЕССА ПРИ РАЗЛИЧНЫХ МЕТОДАХ РЕГИОНАЛЬНОГО ВОЗДЕЙСТВИЯ // Фундаментальные исследования. 2014. № 10-5. С. 817-821;URL: https://fundamental-research.ru/en/article/view?id=35744 (дата обращения: 17.05.2026).



