Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE ORIGINAL METHOD OF PREVENTING SEPTIC COMPLICATIONS IN LAPAROSCOPIC APPENDECTOMY
Острый аппендицит является наиболее распространенным заболеванием органов брюшной полости, требующим неотложного оперативного лечения. Количество пациентов с этой патологией составляет 30–40 % всех больных хирургического профиля [2, 4].
Несмотря на широкое развитие лапароскопической хирургии, её активное внедрение в ургентную практику, частота гнойно-септических послеоперационных осложнений при лапароскопической аппендэктомии стабильно отмечается на уровне 2–5,8 % [5, 6, 7, 9].
При этом следует отметить, что столь высокий уровень послеоперационных гнойно-септических осложнений обусловлен малоэффективной и недостаточной по своему содержанию, а зачастую формальной профилактикой гнойно-септических осложнений. На дооперационном этапе, как правило, она сводится к эмпирическому назначению антибактериальных препаратов широкого спектра действия, введение которых продолжается и в послеоперационном периоде. А объем интраоперационных мероприятий по профилактике такого рода осложнений сводится к промыванию брюшной полости растворами антисептиков, что способствует контаминации не вовлеченных в воспалительный процесс отделов брюшной полости и не всегда адекватным дренированием [1, 3, 9].
Таким образом, разработка и внедрение новых методов профилактики гнойно-септических осложнений является актуальной проблемой современной лапароскопической хирургии [8, 9].
Целью нашего исследования являлась оценка эффективности нового разработанного способа профилактики гнойно-септических осложнений при лапароскопической аппендэктомии.
Материалы и методы исследования
На базах кафедры хирургических болезней ФПК и ППС ГБОУ ВПО «РостГМУ» Минздрава России (г. Ростов-на-Дону) – отделении хирургическом клиники РостГМУ и отделении хирургическом МБУЗ городской больницы № 6 (г. Ростов-на-Дону) проведен комплексный анализ результатов клинического и инструментального обследования, а также результатов видеоэндохирургического лечения 294 больных с острым деструктивным аппендицитом в период с 2009 по 2013 гг.
В первую – контрольную – группу клинических наблюдений нами включен 151 пациент с острым деструктивным аппендицитом, которым проводилась профилактика гнойно-септических осложнений, заключающаяся в назначении антибактериального препарата, относящегося к группе цефалоспоринов 3-й генерации в комбинации с метранидазолом за 30 минут до операции и промывании брюшной полости раствором фурациллина интраоперационно.
Вторую группу наблюдений составили 143 больных острым деструктивным аппендицитом, которым проводилась профилактика гнойно-септических осложнений по оригинальной методике, основанной как на системном применении антибактериальных препаратов, так и местном повышении их концентрации путем мелкодисперсной локальной дозированной обработки брюшной полости в очаге воспаления (Федеральный патент России на изобретение № 2468739 от 10.12.2012 г.), при помощи разработанного устройства (Федеральный патент России на полезную модель № 122580 от 10.12.2012 г.).
Каждая группа больных разделялась ещё на 3 подгруппы в зависимости от способа обработки культи червеобразного отростка. Это обусловлено тем фактом, что способ обработки культи червеобразного отростка играет ключевую роль в профилактике гнойно-септических осложнений, поскольку от степени повреждения культи зависит выраженность инфильтративно-воспалительных изменений в ее стенках, что напрямую коррелирует со скоростью репаративно-восстановительных процессов и скоростью организации шовного материала как инородного предмета, расположенного в стенке кишки.
После использования полного комплекса неинвазивных методик исследования больным выполнялась диагностическая лапароскопия, в ходе которой окончательно определялся объем оперативного вмешательства.
Результаты исследования и их обсуждение
Диагностическая лапароскопия, проводимая в первой клинической группе, позволила выявить острый гангренозно-перфоративный аппендицит у 4 пациентов (2,65 %), острый гангренозный аппендицит у 15 пациентов (9,93 %), острый флегмонозный аппендицит у 132 пациентов (87,42 %) пациентов.
Во второй клинической группе острый гангренозно-перфоративный аппендицит обнаружен у 7 пациентов (4,90 %), острый гангренозный аппендицит у 11 пациентов (7,69 %), острый флегмонозный аппендицит у 125 пациентов (87,41 %).
Кроме того, в ходе диагностической лапароскопии выявлено, что наиболее распространенным в I клинической группе являлся серозный перитонит 131 (86,75 %) пациентов, серозно-фибринозный перитонит обнаружен у 12 пациентов, что составило 7,95 %, фибринозно-гнойный перитонит был обнаружен у 5 пациентов (3,31 %), гнойный перитонит был обнаружен всего у 3 пациентов (1,99 %).
Во второй группе также превалировало количество пациентов с серозным перитонитом 126 (86,11 %), серозно-фибринозный перитонит зарегистрирован у 12 (7,95 %) пациентов. Фибринозно-гнойный выпот был установлен у 3 пациентов (2,10 %), гнойный у 5 пациентов (3,50 %).
Наиболее распространенным дооперационным осложнением, как в первой, так и во второй группе клинических наблюдений является местный отграниченный перитонит 143 наблюдений в первой группе (94,70 %) и 128 наблюдений во второй группе (89,51 %). Вторым по распространенности дооперационным осложнением являлось наличие у больных рыхлого периаппендикулярного инфильтрата, который зарегистрирован у 26 больных первой группы (17,22 %) и у 25 больных (17,48 %) второй группы. Местный неотграниченный перитонит на дооперационном этапе являлся третьим по распространенности осложнением и определялся у 7 пациентов (4,64 %) I группы и 12 пациентов (18,390 %) II группы.
Такого рода осложнения не являлись причиной перехода на конверсию. Всем больным выполнялась лапароскопическая аппендэктомия. Распределение больных в зависимости от способа обработки культи червеобразного отростка отображено в табл. 1.
В подгруппе «А» производилась коагуляция слизистой культи отростка монополярным эндоскопическим крючком; в подгруппе «В» – культя обрабатывалась при помощи аппарата LigaSure; в подгруппе «С» – обработка культи производилась эндоскопическими коагуляционными ножницами (LCSK 5) при помощи аппарата Ultracision Harmonic Scalpel.
Такой подход в выборе способа обработки культи червеобразного отростка основывался на результатах проведенного нами экспериментального исследования на лабораторных крысах.
В основе же оригинальной разработанной методики учтены физиологические особенности брюшины, выстилающей органы брюшной полости, связанные со способностью к резорбции жидкости. Поэтому для профилактики бактериального инфицирования тканей в очаге воспаления нами был определен местный путь повышения концентрации антибактериального препарата (Метранидазола) и антисептика (Мирамистина) в очаге воспаления.
Таблица 1
Распределение больных в группах с учётом способа обработки культи аппендикса
|
Количество |
Всего абс. |
Всего % |
|||||
|
Мужчины |
Женщины |
||||||
|
Абс. |
% |
Абс. |
% |
||||
|
I |
А |
21 |
13,91 |
28 |
18,54 |
49 |
32,45 |
|
В |
23 |
15,23 |
30 |
19,87 |
53 |
35,10 |
|
|
С |
23 |
15,23 |
26 |
17,22 |
49 |
32,45 |
|
|
Сумма |
|
67 |
44,37 |
84 |
55,63 |
151 |
100 |
|
II |
А |
22 |
15,38 |
24 |
16,78 |
46 |
32,16 |
|
В |
22 |
15,38 |
26 |
18,18 |
48 |
33,57 |
|
|
С |
23 |
16,08 |
26 |
18,18 |
49 |
34,27 |
|
|
Сумма |
|
67 |
46,85 |
76 |
53,15 |
143 |
100 |
Кроме того, нами исключен фактор, предрасполагающий к развитию гнойно-септических осложнений, такой как процесс эвакуации гнойного выпота и орошения брюшной полости антисептиками, через просвет одного и того же инструмента-насадки для электроотсоса и аквапуратора, что способствует контаминации не вовлеченных в воспалительный процесс её отделов.
После удаления электроотсосом воспалительного выпота из брюшной полости производили основной этап операции – удаление червеобразного отростка. Затем в один из боковых троакаров, под контролем видеокамеры лапароскопа, вводили разработанное устройство и под оптическим контролем производили орошение брюшины в очаге воспаления мелкодисперсным раствором антисептика и антибактериального препарата (рис. 1).
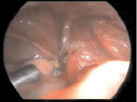
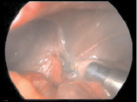
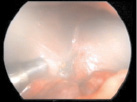
Рис. 1. Подведение устройства к очагу воспаления, распыление раствора антибактериального препарата и антисептика
При таком способе обработки брюшной полости малый диаметр частиц (4–5 мкм) способствует лучшей диффузии антибактериального препарата через «барьер» образуемый париетальной брюшиной, и способствует увеличению концентрации данного препарата в очаге воспаления. Следует также отметить, что до операции в обеих группах больным проводилась антибактериальная профилактика гнойно-септических осложнений по следующей схеме:
|
1) Цефалоспорины III поколения Цефтриаксон (цефобид) по 1 гр, при массе тела свыше 100 кг – 2 гр. При наличии гипертермии более 6 часов 2) Метронидазол 100,0 мл |
в/в – струйно, за 30 мин до интубации. в/в – капельно, за 30 мин до операции |
Подбор такой схемы антибактериальной терапии в обеих группах обусловлен рекомендациями по лечению острой абдоминальной хирургической инфекции разработанными академиком Гельфандом и академиком Савельевым В.С. (2005 г.).
В раннем послеоперационном периоде с целью оценки результатов оперативного лечения и эффективности применения оригинальной методики профилактики гнойно-септических осложнений проводили изучение уровня лейкоцитов, палочкоядерных нейтрофилов, скорости оседания эритроцитов и лейкоцитарного индекса интоксикации (табл. 2).
Таблица 2
Средние значения лабораторных показателей и ЛИИ у больных I и II клинических групп на первые сутки после операции
|
Подгруппы |
I группа |
II группа |
||||||
|
Лейк. |
Пя. % |
ЛИИ |
СОЭ |
Лейк. |
Пя. % |
ЛИИ |
СОЭ |
|
|
А |
8,46 ± 0,91 |
6,0 ± 1,04 |
2,97 ± 0,48 |
17,43 ± 3,16 |
7,16 ± 0,78 |
5,10 ± 0,74 |
2,72 ± 0,32 |
14,97 ± 2,37 |
|
В |
8,45 ± 0,87 |
5,97 ± 1,00 |
3,00 ± 0,46 |
17,39 ± 3,01 |
7,16 ± 0,76 |
5,12 ± 0,71 |
2,70 ± 0,30 |
15,01 ± 2,30 |
|
С |
8,43 ± 0,92 |
6,02 ± 1,05 |
2,97 ± 0,48 |
17,49 ± 3,18 |
7,14 ± 0,74 |
5,06 ± 0,69 |
2,70 ± 0,29 |
14,86 ± 2,23 |
Примечание. р < 0,05.
Как видно из табл. 2, наименьший показатель уровня лейкоцитов 7,14 ± 0,74 в послеоперационном периоде был зарегистрирован в подгруппе С II клинической группы, где пациентам проводилась обработка культи червеобразного отростка с применением аппарата Ultracision Harmonic Scalpel и оригинальная методика профилактики гнойно-септических осложнений.
При этом как в I, так и во II клинических группах отмечалась разница в средних значениях лабораторных показателей и среднем уровне лейкоцитарного индекса интоксикации в зависимости от способа обработки культи червеобразного отростка. Так, наиболее низкими показателями характеризовалась подгруппа С – применение аппарата Ultracision Harmonic Scalpel в обеих группах, что свидетельствует о роли выбора способа обработки культи червеобразного отростка в аспекте профилактики гнойно-септических осложнений.
Следует отметить, что в результате применения оригинальной методики профилактики гнойно-септических осложнений у больных острым деструктивным аппендицитом во II клинической группе в послеоперационном периоде средний уровень лейкоцитов был ниже в группе, чем в I группе, что отражено на рис. 2.
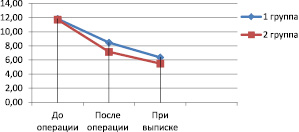
Рис. 2. График динамики изменения среднего значения уровня лейкоцитов I и II группах до и после операции
Из графика (рис. 2) следует, что во второй группе средний показатель среднего уровня лейкоцитов – 7,16 ± 0,43 после операции – характеризовался тенденцией к более резкому снижению, нежели аналогичный показатель в первой клинической группе – 8,45 ± 0,51. Однако следует отметить, что незначительный перевес дооперационного показателя среднего уровня лейкоцитов отмечался в первой группе – 11,83 ± 0,52 по сравнению со второй – 11,73 ± 0,70.
Изменения палочкоядерных нейтрофилов до и после оперативного лечения, во второй клинической группе характеризовались также более интенсивной нормализацией среднего показателя с 8,14 ± 0,63 до операции, до 5,11 ± 0,41 после операции, по сравнению с аналогичными показателями в первой клинической группе 8,78 ± 0,65 – 5,98 ± 0,58 при р < 0,05.
При анализе среднего значения лейкоцитарного индекса интоксикации нами также была отмечена более стремительная положительная динамика во второй клинической группе с 5,03 ± 0,47 – до операции к 2,72 ± 0,18 – после операции в сравнении с первой группой, где данный показатель до операции составлял 4,55 ± 0,55, а после операции 3,00 ± 0,27 (при р < 0,05).
Данные изменения среднего значения лейкоцитарного индекса интоксикации свидетельствуют об эффективности проведения оригинальной методики профилактики гнойно-септических осложнений.
В пользу данного утверждения также свидетельствует количество зарегистрированных, как в первой, так и во второй группах случаев возникновения инфильтрата правой подвздошной области и нагноения послеоперационных ран. В I клинической группе у 12 пациентов (7,95 %) отмечалось развитие инфильтрата правой подвздошной области и 1 пациента (0,66 %) развитие нагноения послеоперационных ран, во II клинической группе нагноения послеоперационных ран не отмечалось, а инфильтрат правой подвздошной области был зарегистрирован у 4 пациентов (2,80 %).
Кроме того, следует отметить, что больные II клинической группы, которым проводилась оригинальная методика профилактики гнойно-септических осложнений, на стационарном лечении пребывали в течение 8,13 ± 0,45 суток, а пациентам I клинической группы требовалось стационарное лечение в среднем в течение 10,20 ± 0,48 суток (р < 0,05), что обусловлено более длительной нормализацией уровня лейкоцитов, палочкоядерных нейтрофилов и, соответственно, лейкоцитарного индекса интоксикации.
Выводы
Комплексный подход с использованием вышеуказанных методик обработки культи червеобразного отростка в сочетании с применением оригинальной методикой профилактики гнойно-септических осложнений способствует скорейшему снижению воспалительного процесса, уменьшению количества нагноительных осложнений, а также снижению послеоперационного койко-дня.
Применение оригинального способа профилактики гнойно-септических осложнений показало свою эффективность. Считаем, что применение данного способа может улучшить результаты лечения больных с деструктивными формами острого аппендицита.
Рецензенты:
Татьянченко В.К., д.м.н., профессор, заведующий кафедрой клинической анатомии и оперативной хирургии факультета повышения квалификации и переподготовки специалистов, ГБОУ ВПО «Ростовский государственный медицинский университет» Минздрава России, г. Ростов-на-Дону;
Хитарьян А.Г., д.м.н., профессор, заведующий первым хирургическим отделением, НУЗ «Дорожная клиническая больница на ст. Ростов-Главный» ОАО «РЖД», г. Ростов-на-Дону.
Работа поступила в редакцию 18.09.2014.
Библиографическая ссылка
Черкасов М.Ф., Мрыхин Г.А. ОРИГИНАЛЬНАЯ МЕТОДИКА ПРОФИЛАКТИКИ ГНОЙНО-СЕПТИЧЕСКИХ ОСЛОЖНЕНИЙ ПРИ ЛАПАРОСКОПИЧЕСКОЙ АППЕНДЭКТОМИИ // Фундаментальные исследования. 2014. № 10-3. С. 581-585;URL: https://fundamental-research.ru/en/article/view?id=35468 (дата обращения: 15.05.2026).



