Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
SYNTHESIS AND BIOLOGICAL ACTIVITY AMIDES PYRIDINE-2-CARBOXYLIC ACIDS
Синтез новых органических потенциально биологически активных веществ (БАВ), изучение их активности и взаимосвязи, структура, биологическое действие является актуальной задачей фармацевтической химии. Весьма перспективным направлением является поиск новых БАВ в ряду замещенных амидов пиридин-2-карбоновой (пиколиновой) кислоты. В ранее проведенных нами исследованиях было показано, что синтезированные замещенные амиды пиридин-3- и пиридин-4-карбоновых кислот при биологических испытаниях на животных показали противовоспалительную или анальгетическую активность [5, 6]. В то же время мало изученными являются амиды пиридин-2-карбоновой кислоты. Известно, что незамещенные амиды пиколиновой, никотиновой и изоникотиновой кислот обладают противовоспалительной и анальгетической активностью [9]. В настоящее время в медицинской практике используется структурный аналог-оригинальный отечественный препарат – эфир пиперидин-2-карбоновой кислоты и спирта холина под названием димеколин в качестве ганглиоблокирующего средства [4]. Методом рентгеноструктурного анализа были изучены 4-бромфенилпиридин-2-[10] и 4-хлор-фенилпиридин-2-карбоновой кислот [11], но сведения о их биологической активности отсутствуют. Приведенные данные литературы свидетельствуют о том, что среди производных пиридин-2-карбоновой кислоты имеются биологически активные вещества.
В продолжение предыдущих исследований и с целью поиска новых биологически активных соединений, обладающих противовоспалительной и/или анальгетической активностью среди производных пиридин-2-карбоновой (пиколиновой) кислоты, нами были получены ранее неизвестные амиды данной кислоты.
Целью исследования является разработка методик синтеза новых потенциально биологически активных соединений в ряду производных пиридин-2-карбоновой кислоты на основе хлорангидрида пиридин-2-карбоновой кислоты в реакции с ариламинами, изучение их физико-химических свойств. Провести анализ результатов биологических испытаний полученных соединений в сравнении с активностью ранее полученных их структурных аналогов, а также и препаратами-эталонами. Выявить взаимосвязь структура-активность в ряду замещенных амидов пиридин-2-карбоновой кислоты.
Материалы и методы исследования
Структура полученных соединений подтверждена спектральными методами анализа. ЯМР 1Н-спектры записаны на спектрометре ЯМР MERCURY-300 фирмы Varian, (300 МГц), в ДМСО-d6, внутренний стандарт – ГМДС. ИК-спектры,сняты на ИК-спектрометре SPECORD М-80 (Германия), в вазелиновом масле.Ход реакций и чистоту соединений контролировали методом ТСХ на пластинах SilufolUV-254 в системе углерод четыреххлористый /ацетон (6:1), пятна детектировали парами йода. Данные элементного анализа синтезированных веществ соответствуют вычисленным значениям. Биологические испытания синтезированных соединений проведены согласно методическим указаниям.
Результаты исследования и их обсуждение
В ходе опытов было установлено, что при нагревании эквимолекулярных количеств хлорангидрида пиридин-2-карбоновой кислоты с ариламинами в бензоле в присутствии триэтиламина свыходами 74 – 82 % образуются соответствующие замещенные амиды пиридин-2-карбоновой кислоты (1–6) по схеме:
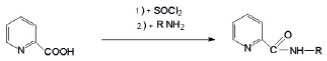
1–6
Где R = С6Н3Cl2-2,4 (1);C6H3CI2-2,6 (2); С6Н4Br-4 (3); С6Н4CI-3(4) С6Н4Cl-4 (5); C6H4СООС2Н5-4 (6)
Полученные соединения (1–6) – белые кристаллические вещества, не растворимые в воде и растворимые при нагревании в органических растворителях: диоксане, ДМФА. Характеристики синтезированных соединений приведены в (табл. 1).
Таблица 1
Характеристики замещенных амидов пиридин-2-карбоновойкислоты (1-6)
|
Соединение |
R |
Брутто-формула |
Т.пл., оС |
Выход, % |
Rf* |
|
1. |
С6Н3Cl2-2,4 |
C12H8CI2N2O |
144-145 |
82 |
0,62 |
|
2. |
С6Н3Cl2-2,6 |
C12H8CI2N2O |
120-122 |
76 |
0,50 |
|
3. |
С6Н4Br-4 |
С12Н9 BrN2O |
135-137 |
80 |
0,64 |
|
4. |
С6Н4CI-3[10] |
С12Н9CINO2 |
155-157 |
76 |
0.56 |
|
5. |
С6Н4CI-4[11] |
С12Н9CINO2 |
134-135 |
74 |
0.57 |
|
6. |
C6H4СООС2Н5-4 |
С15Н14N2O3 |
124-125 |
80 |
0,46 |
Примечание: *в системе углерод четыреххлористый – ацетон (6:1)
Общая методика получения амидов пиридин-2-карбоновой кислоты (1–6). К 1,23 г (0,01 моль) пиридин-2-карбоновой (пиколиновой) кислоты прибавляют 20-30 мл тионилхлорида и нагревают на водяной бане 3 часа. Избыток тионилхлорида отгоняют в вакууме. К охлажденной реакционной массе прибавляют (0,01 моль) соответствующего амина, растворенного в 40-50 мл бензола и 3-4-мл триэтиламина. Реакционную массу нагревают на водяной бане при 50 оС в течение 1 часа. Бензол и летучие продукты отгоняют с водяным паром. Остаток обрабатывают 10 % раствором NaHCO3, отфильтровывают и перекристаллизовывают соединения из диоксана. Выходы продуктов реакций составляют 74-82 %.Структура полученных соединений 1–6 подтверждена данными ИК-, ЯМР 1Н- спектров.
В спектрах ЯМР 1Н соединений 1–6 имеются характерные сигналы протонов δ, м.д.: 10,33-10,80 (1H, с., NH амид), группа линий ароматических и гетероциклических протонов в области 7,92-8,08. В ИК спектрах полученных соединений наблюдаются характерные полосы поглощения: 1688 – 1704 (СО), 3296 – 3336 (NH-амид) см-1.
Биологические исследования
Испытания синтезированных соединений проведены согласно методическим указаниям «Руководства по экспериментальному (доклиническому) изучению новых фармакологических веществ» [7]. Результаты обработаны статистически с использованием критерия Стьюдента, эффект считали достоверным при р ≤ 0,05 [1]. Анализ результатов биологических испытаний апробированных соединений проведен в сравнении с литературными данными по активности препаратов-эталонов: ортофена, аспирина [2].
Острая токсичность соединений (1, 2, 3) изучена на белых мышах-самках массой 18 – 22 г при однократном внутрибрюшинном введения с учетом гибели животных в течение 24 ч. Установлено, что ЛД50 соединений более 2150 мг/кг (табл. 3), и они относятся к малотоксичным веществам. Из данных литературы известно, что ЛД50 при этом же пути введения ортофенаравна – 132, аспирина – 495 мг/кг [3].
Противовоспалительная активность(ПВА) соединений (1–6) изучена на белых крысах обоего пола массой 180 – 220 г на каррагениновой модели воспаления, создаваемой субплантарным введением в заднюю лапу крыс 0,1 мл 1 % водного раствора каррагенина. Исследуемое вещество вводили внутрибрюшинно в дозе 25 мг/кг в 2 % крахмальной слизи, за один час до моделирования воспаления. Прирост объёма воспалённой стопы оценивали онкометрически через 3 и 5 часов после введения флогогенного агента и вычисляли процент торможения отёка к контролю. Проведено 7 опытов, в каждой группе было по 5 животных. Полученные результаты сравнивали с литературными данными по противовоспалительному действию диклофенака натрия в дозе 25 мг/кг и аспирина в дозе 50 мг/кг на каррагениновой модели воспаления [2].
Таблица 2
Острая токсичность, противовоспалительная активность амидовпиридин-2-карбоновых кислот (1-6)
|
Соединение / препарат- эталон |
R |
ЛД50, мг/кг |
Противовоспалительная активность, % торможения отека к контролю после введения каррагенина через |
||
|
Доза, мг/кг |
3 ч |
5 ч |
|||
|
1 |
С6Н3Cl2-2,4 |
>2150 |
25 |
84,5* |
32,7*** |
|
2 |
С6Н3Cl2-2,6 |
> 2150 |
25 |
88,0* |
37,0** |
|
3 |
С6Н4Br-4 |
> 2150 |
25 |
61,0* |
44,0* |
|
4 |
С6Н4CI-3 |
. . . |
25 |
-17,2**** |
-33,6**** |
|
5 |
С6Н4CI-4 |
. . . |
25 |
-33,3**** |
-21,7**** |
|
6 |
C6H4СООС2Н5-4 |
. . . |
25 |
47,8** |
5,7**** |
|
Диклофенак натрия (ортофен) [2] |
|
132 |
25 |
69,40** |
72,20** |
|
Ацетилсалициловая кислота (аспирин) [2] |
|
495 |
50 |
51,20** |
28,70** |
|
Контроль |
|
. . . |
. . . |
70,88 ± 0,16 |
87,07 ± 1,04 |
Примечания: *p > 0,001; **р > 0,01;***р < 0,02;****p < 0,5 по сравнению с контролем
Исследования показали, что апробированные соединения (1, 2, 3) при внутрибрюшинном пути введения в дозе 25 мг/кг после введения флогогенного агента тормозят развитие отека через 3 ч в пределах 61,0 – 88,0 и 5 ч – 32,7 – 44,0 %. Противовоспалительный эффект изученных соединений снижается в опытах через 5 часов. Наиболее активными являются замещенные амиды пиридин-2-карбоновой кислоты (соединения 1,2), ПВА которых сравнима с таковой диклофенака натрия в этой же дозе через 3 часа наблюдения, но менее токсичны, чем препарат-эталон сравнения. По противовоспалительному действию соединения 1, 2, 3 в дозе 25 мг/кг являются более активными, чем аспирин в дозе 50 мг/кг (табл. 2).
Анальгетическая активность соединений (1–6) и анальгина изучена на модели «уксусных корчей» на беспородных белых мышах-самцах массой 22-24 г. Мышам внутрибрюшинно вводили 0,75 % водный раствор уксусной кислоты из расчета 0,1 мл на 10 г массы животного и подсчитывали количество корчей в течение 15 минут. Исследуемые вещества в дозе 25 мг/кг вводили внутрибрюшинно в виде взвеси в 2 % крахмальной слизи за 30 мин до внутрибрюшинного введения уксусной кислоты, а препарат сравнения анальгин – в дозе 55 мг/кг, соответствующей ED50 по тесту «уксусных корчей» [8]. Результаты оценивали по способности тормозить количество корчей по сравнению с контрольными животными, получавшими растворитель. Каждое соединение исследовали на 6 животных. Данные опытов обрабатывали статистически с вычислением критерия достоверности. Разницу считали достоверной при р< 0,05 [1].
Анальгетическая активность соединений (1–6) изучена на беспородных белых мышах методом термического раздражения «горячая пластинка». Исследуемые соединения вводили в дозе 25 мг/кг внутрибрюшинно в виде 2 % крахмальной слизи за 30 минут до помещения животного на металлическую пластинку, нагретую до 55 оС. Показателем болевой чувствительности служила длительность пребывания животного на горячей пластинке до наступления оборонительного рефлекса (облизывания лапок, подскакивания). Наблюдение проводили через 0,5; 1,0; 1,5; 2 часа после введения вещества.
Таблица 3
Анальгетическая активность амидов пиридин-2-карбоновых кислот (1-6)
|
Соединение / препарат- эталон |
R |
Доза мг/кг |
«Горячая пластинка» |
«Уксусные корчи» |
|
|
время оборонительного рефлекса, с через 2,5 ч |
количество корчей |
% уменьшения корчей к контролю |
|||
|
1 |
С6Н3Cl2-2,4 |
25 |
19,20 ± 0,86* |
19,30 ± 1,05* р < 0,05 |
22,8 |
|
2 |
С6Н3Cl2-2,6 |
25 |
19,50 ± 1,02* |
17,7 ± 1,96* р < 0,05 |
28,7 |
|
3 |
С6Н4Br-4 |
25 |
21,90 ± 1,21 |
11,2 ± 1,04 р < 0,05 |
54,7 |
|
4 |
С6Н4CI-3 |
25 |
19,20 ± 0,58* |
17,8 ± 1,55* р < 0,05 |
28,8 |
|
5 |
С6Н4CI-4 |
25 |
20,00 ± 0,95* |
12,6 ± 2,69 p < 0,01 |
48,8 |
|
6 |
C6H4СООС2Н5-4 |
25 |
20,90 ± 1,71 |
14,7 ± 1,72 p < 0,01 |
40,8 |
|
Контроль |
. . . |
25 |
10,75 ± 1,63 |
25,0 ± 2,30 |
- |
|
Метамизол натрия (анальгин) |
. . . |
55 |
16,32 ± 3,0 |
10,6 ± 1,38 p < 0,001 |
58,0 |
Примечания: *достоверность различий по сравнению с контролем p < 0,05
Из приведенных данных таблицы 3 следует, что по тесту «уксусные корчи» соединения 3, 5, 6 вызывают защиту от корчей на уровне 40,8 – 54,7 %, а по тесту «горячая пластинка» апробированные соединения оказывают анальгетическое действие, сравнимое с действием метамизола натрия.
Данные, полученные в результате исследования показывают, что некоторые соединения обладают противовоспалительной и анальгетической активностью. Поиск в ряду амидов пиридин-2-карбоновых кислот представляет интерес для дальнейших исследований.
Выводы
- В ходе проведенного исследования установлено,что при нагревании хлорангидрида пиридин-2-карбоновой кислоты с ариламинами с хорошими выходами образуются соответствующие амиды пиридин-2-карбоновой кислоты.
- Индивидуальность полученных соединений установлена с помощью ТСХ, а химическая структура – спектральными данными.
- Фармакологические исследования показали, что апробированные соединения в дозе 25 мг/кг при внутрибрюшинном введении обладают противовоспалительной или анальгетической активностью, которая зависит от химической природы остатка амина в амидной группе данных соединений.
- Поиск новых биологически активных соединений в ряду амидов замещенных пиридин-2-карбоновых кислот является перспективным.
Рецензенты:
Хомов Ю.А., д.фарм.н., профессор кафедры фармацевтической химии ФДПО и ФЗО ГБОУ ВПО ПГФА Министерства здравоохранения России, г. Пермь;
Михайловский А.Г., д.фарм.н., профессор кафедры общей и органической химии ГБОУ ВПО ПГФА Министерства здравоохранения Россия, г. Пермь.
Работа поступила в редакцию 24.06.2014.
Библиографическая ссылка
Бояршинов В.Д., Михалев А.И., Ухов С.В., Юшкова Т.А., Махмудов Р.Р. СИНТЕЗ И БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ АМИДОВ ПИРИДИН-2-КАРБОНОВОЙ КИСЛОТЫ // Фундаментальные исследования. 2014. № 9-3. С. 606-610;URL: https://fundamental-research.ru/en/article/view?id=34896 (дата обращения: 21.05.2026).



