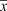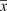В настоящее время особую актуальность приобретают исследования в плане расширения ассортимента доступных широким слоям населения препаратов на основе лекарственного растительного сырья [4–7]. Одной из актуальных задач современной фармации, в том числе фармакогнозии, является создание и внедрение импортозамещающих лекарственных средств, а также поиск рациональных путей использования лекарственных растений и лекарственного растительного сырья (ЛРС) в соответствии с принципами доказательной медицины [3]. В этом отношении особый интерес представляет солодка голая (Glycyrrhiza glabra L.), на основе корней которой выпускается целый ряд препаратов (экстракты густой и сухой, экстракт-концентрат, сироп солодкового корня и др.) [3, 4, 7]. Однако создание современных препаратов возможно лишь на основе методик, отвечающих параметрам валидации [4]. В этом контексте для успешной реализации Стратегии лекарственного обеспечения населения Российской Федерации на период до 2025 года имеются объективные предпосылки, поскольку в области фармакогнозии за последние 15–20 лет произошли качественные изменения в плане изучения химического состава лекарственных растений и ЛРС, причем этому способствовало то обстоятельство, что данная наука обогатилась современными спектральными и физико-химическими методами. Внедрение тонкослойной хроматографии (ТСХ), высокоэффективной жидкостной хроматографии, ЯМР-спектроскопии и других методов открыло новые возможности для совершенствования стандартизации ЛРС и фитопрепаратов, а также внедрения научно обоснованных технологий получения лекарственных средств корней солодки, в том числе на основе сапонинов и флавоноидов [1, 3–5, 8].
Цель данной работы – исследование по разработке методик качественного и количественного анализа лекарственного препарата «Солодки экстракт жидкий».
Материал и методы исследования
В качестве объектов исследования служили корни солодки голой, биологически активные соединения (глицирризиновая кислота, ликуразид, ликвиритин, ононин, ликвиритигенин, изоликвиритигенин, формононетин), выделенные из сырья данного растения, а также глицирам-стандартный образец и ликуразид-стандартный образец. Лекарственный препарат «Солодки экстракт жидкий» получали экстракцией из корней солодки голой (1:1) 40 % этиловым спиртом.
В работе использованы тонкослойная хроматография, регистрацию УФ-спектров проводили с помощью спектрофотометра «Specord 40» (Analytik Jena).
Результаты исследования и их обсуждение
Для достижения поставленной цели нами были изучены условия хроматографического разделения сапонинов и флавоноидов корней солодки и экстракта жидкого, позволяющие обнаруживать доминирующие БАС – глицирризиновую кислоту и ликуразид. Для достоверного определения веществ нами предложено использовать государственные стандартные образцы –глицирам (моноаммониевая соль глицирризиновой кислоты) (сапонин) и ликуразид (флавоноид). Использование данных стандартов позволяет исключить ошибки при идентификации диагностических веществ и, следовательно, обеспечивать валидацию методик качественного анализа сырья и препаратов солодки. Использование в качестве ГСО глицирама объясняется тем, что глицирризиновая кислота вещество нестабильное, что препятствует использованию данного соединения в качестве государственного стандартного образца.
При использовании пластинок «Сорбфил ПТСХ-АФ-А-УФ» (система растворителей хлороформ – метанол – вода, 26:14:3) ликуразид обнаруживается на хроматограмме в виде доминирующего желтого или желтовато-оранжевого пятна с величиной Rf около 0,5, а глицирризиновая кислота – в виде фиолетового флуоресцирующего пятна (254 нм) с величиной Rf около 0,3 (на уровне ГСО глицирама). При этом обнаруживаются также пятна ликвиритина (Rf около 0,6), ононина (Rf около 0,7), ликвиритигенина и изоликвиритигенина (Rf около 0,8), а также формононетина (Rf около 0,9) (рис. 1).
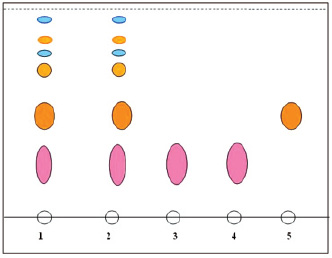
Рис. 1. Хроматографический профиль веществ корней и экстракта солодки голой. Обозначения: 1 – водно-спиртовое извлечение корней солодки голой; 2 – экстракт солодки жидкий; 3 – глицирам; 4 – глицирризиновая кислота; 5 – ликуразид
Для целей количественного анализа предложено, как и в случае корней солодки [1, 2], использование двух показателей – содержания глицирризиновой кислоты и содержания суммы флавоноидов (в пересчете на ликуразид). При количественном определении содержания глицирризиновой кислоты в электронном спектре испытуемого раствора содержится один интенсивный максимум поглощения при длине волны 258 ± 2 нм (рис. 2), коррелирующий с таковым глицирризиновой кислоты и глицирама [1]. Для определения суммы флавоноидов, как и в случае корней солодки, предложены подходы к стандартизации, заключающиеся в использовании дифференциальной спектрофотометрии при аналитической длине волны 420 нм [2], так как в УФ-спектре раствора Б экстракта солодки в присутствии AlCl3 наблюдается батохромный сдвиг длинноволновой полосы (рис. 3), соответствующий спектральным характеристикам ликуразида – одного из основных флавоноидов корней солодки голой.
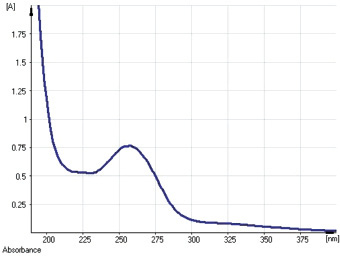
Рис. 2. УФ-спектр испытуемого раствора Б жидкого экстракта солодки
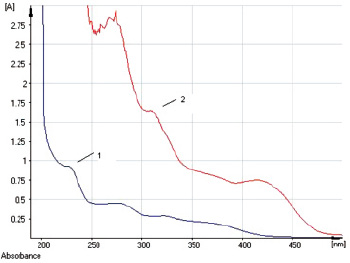
Рис. 3. УФ-спектры раствора Б экстракта солодки (1) и раствора Б в присутствии AlCl3 (2)
Методика количественного определения содержания глицирризиновой кислоты в препарате «Солодки экстракт жидкий». 2,00 мл экстракта солодкового корня жидкого помещают в колбу коническую со шлифом вместимостью 250 мл, прибавляют 20 мл спирта 95 % и перемешивают. Далее добавляют 50 мл 3 % ацетонового раствора кислоты трихлоруксусной и нагревают в течение 10 мин. После охлаждения полученный раствор фильтруют через бумажный фильтр, колбу промывают двумя порциями 3 % ацетонового раствора кислоты трихлоруксусной по 10 мл, фильтруя через тот же фильтр. К полученному фильтрату прибавляют по каплям раствор аммиака концентрированный до появления обильного осадка (рН от 8,3 до 8,6 по универсальному индикатору). Раствор с осадком переносят на беззольный фильтр, помещенный в воронку Бюхнера. Колбу и фильтр промывают 50 мл ацетона в три приема. Осадок с фильтром переносят в колбу, в которой проводилось осаждение, растворяют в 50 мл воды, количественно переносят в мерную колбу вместимостью 250 мл и доводят объем раствора водой до метки (раствор А). 1 мл раствора А помещают в мерную колбу вместимостью 25 мл и доводят объем раствора водой до метки (раствор Б).
Оптическую плотность раствора Б измеряют на спектрофотометре при длине волны 258 нм в кювете с толщиной слоя 10 мм, используя в качестве раствора сравнения воду.
Параллельно измеряют оптическую плотность раствора Б ГСО глицирама.
Содержание глицирризиновой кислоты в жидком экстракте в пересчете на глицирам в процентах (Х) рассчитывают по формуле:
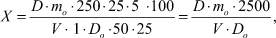
где D – оптическая плотность испытуемого раствора (Б) при длине волны 258 нм; DО – оптическая плотность раствора ГСО глицирама (Б) при длине волны 258 нм; V – объем препарата, в мл; mo – масса ГСО глицирама в граммах.
Ошибка единичного определения с доверительной вероятностью составляет 4,78 % (табл. 1).
Таблица 1
Метрологические характеристики методики количественного определения глицирризиновой кислоты в экстракте солодки жидком
|
f |
|
S |
P, % |
t(P, f) |
Dx |
E, % |
|
10 |
8,15 |
0,1746 |
95 |
2,23 |
±0,39 |
±4,78 |
В случае методики количественного определения суммы флавоноидов ошибка единичного определения с доверительной вероятностью составляет 3,78 % (табл. 2).
Таблица 2
Метрологические характеристики методики количественного определения суммы флавоноидов в экстракте солодки жидком
|
f |
|
S |
P, % |
t(P, f) |
Dx |
E, % |
|
10 |
1,94 |
0,0345 |
95 |
2,23 |
±0,077 |
±3,95 |
Опыты с добавками ГСО глицирама и ликуразида в жидкий экстракт показали, что ошибка анализа находится в пределах ошибки единичного определения, что свидетельствует об отсутствии систематической ошибки в разработанных методиках.
Следовательно, использование в методиках количественного анализа ГСО глицирама и ликуразида позволяет объективно оценивать уровень содержания глицирризиновой кислоты и суммы флавоноидов в экстракте солодки жидком. Содержание глицирризиновой кислоты в сырье и экстракте солодки жидком находится в интервале от 7,50 до 15,23 % (корни) и суммы флавоноидов от 1,90 до 2,11 % (экстракт) соответственно.
Выводы
- На основе изучения физико-химических и спектральных свойств сапонинов и флавоноидов корней солодки голой предложены новые подходы к стандартизации сырья и препаратов данного растения с использованием стандартных образцов ликуразида и глицирама.
- Разработаны унифицированные методики качественного и количественного анализа корней солодки и экстракта жидкого с использованием ТСХ и спектрофотометрии.
- Метрологические характеристики методики количественного определения глицирризиновой кислоты и суммы флавоноидов в экстракте солодки жидком свидетельствуют о том, что ошибка единичного определения составляет ±4,78 % и ±3,95 % соответственно.
Рецензенты:
Первушкин С.В., д.фарм.н., профессор, заведующий кафедрой фармацевтической технологии ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Самара;
Дубищев А.В., д.м.н., профессор, зав. кафедрой фармакологии им. заслуженного деятеля науки РФ, профессора А.А. Лебедева, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Самара.
Работа поступила в редакцию 30.04.2014.