Несмотря на успехи в лечении и широкое применение современных диагностических методов, своевременная постановка показаний к хирургическому вмешательству до сих пор является трудной задачей даже для опытного хирурга, особенно когда речь идет о пациентах детского возраста [1, 3]. И по сей день не прекращается поиск дополнительных диагностических методов, которые позволят снизить риск проведения необоснованной аппендэктомии. Атомно-силовая микроскопия (АСМ) – сравнительно молодой метод исследования, и хотя возможности ее весьма широки, попытки внедрения АСМ в клиническую практику начались лишь недавно [2, 6, 7, 8]. В настоящее время описаны изменения эритроцитов крови при механической желтухе, выявлена их взаимосвязь со степенью интоксикации. Так, доказано увеличение диаметра эритроцитов при уменьшении радиуса их центрального углубления [2].
Целью настоящего исследования явилось изучение морфофункциональных особенностей эритроцитов венозной крови детей, оперированных по поводу острого аппендицита, а также их сравнительный анализ в зависимости от патоморфологической характеристики аппендицита и этапа лечения.
Материалы и методы исследования
Выполнены исследования эритроцитов венозной крови 35 детей, находившихся на лечении в Детской областной клинической больнице г. Белгорода с острым аппендицитом. 6 детей были прооперированы по поводу недеструктивного аппендицита. 29 детей оперированы по поводу деструктивных форм аппендицита. В работе нами использована классификация Колесова В.И. (1959) [4] как наиболее широко распространенная в клинической практике. Неравновесность выборок по объему отражает реальное соотношение указанных форм острого аппендицита в клинической практике. Контрольную группу составили 14 детей, поступивших в стационар с абдоминальным болевым синдромом, которым впоследствии диагноз острой хирургической патологии был исключен.
Забор крови производился с согласия родителей ребенка по стандартной методике путем пункции кубитальной вены. Кровь набиралась в стерильную одноразовую вакуумную пробирку с добавлением гепарина в дозе 10 ед./мл в день поступления и при выписке. Патоморфологические изменения стенки аппендикса изучали стандартными методми. Для оценки ультраструктуры и упругих свойств клеточной поверхности использовали атомно-силовой микроскоп NTEGRA Vita фирмы NT-MDT (г. Зеленоград).
Измеряли диаметр и высоту профиля клетки, то есть максимальную его высоту от подложки, глубину и диаметр центральной ямки эритроцитов; с помощью прилагающейся АСМ графической программы рассчитывались площадь поверхности и объем клетки.
Статистическую обработку данных проводили с помощью программного пакета «Microsoft Office XP» методами параметрического анализа [5]. Определяли среднее (Х), ошибку среднего (м) и среднеквадратичное отклонение (δ). Достоверность различий определяли по t-критерию Стьюдента Уровень значимости p выбран менее 0,05.
Результаты исследования и их обсуждение
Нами были получены изображения эритроцитов венозной крови детей с острым аппендицитом, полученные при поступлении и при выписке (рисунок).
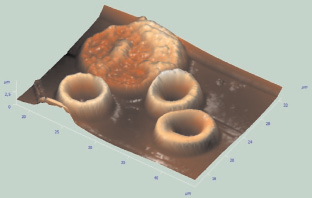
3D-реконструкция поверхности клеток крови при поступлении у ребенка с острым деструктивным аппендицитом
При анализе микрорельефа поверхности эритроцитов при большом разрешении статистически значимых отличий между двумя группами, а также в пределах одной группы при поступлении и при выписке получено не было. В единичных случаях при поступлении у детей с острым деструкивным аппендицитом отмечалось большое количество пор до 5 нм диаметром. В 2 случаях – наличие глобул до 4–5 нм диаметром, однако, учитывая отсутствие повторяемости этих особенностей нанорельефа, указанные находки следует считать скорее артефактом. При анализе морфологии эритроцитов методом АСМ выявлен ряд статистически достоверных отличий как при поступлении между двумя группами, так и в группе детей с деструктивным аппендицитом при поступлении и при выписке.
При сопоставлении морфофункциональных особенностей эритроцитов у детей с деструктивным и с недеструктивным аппендицитом обнаружено, что в первой группе достоверно при поступлении выше диаметр эритроцита (7,85 ± 0,36 мкм при деструктивном аппендиците и 7,37 ± 0,18 ‒ при катаральном, p < 0,05), а также диаметр центральной ямки эритроцита (5,69 ± 0,43 мкм при деструктивном аппендиците и 5,1 ± 0,28 ‒ при катаральном, p < 0,05).
Таблица 1
Статистически значимые отличия морфофункциональных особенностей эритроцитов у детей с острым деструктивным и недеструктивным аппендицитом (p < 0,05)
|
Деструктивный аппендицит |
Недеструктивный аппендицит |
|
|
Диаметр эритроцита, мкм |
7,85 ± 0,36 |
7,37 ± 0,18 |
|
Диаметр центральной ямки эритроцита, мкм |
5,69 ± 0,43 |
5,1 ± 0,28 |
Помимо указанных отличий имеется тенденция к увеличению площади поверхности клетки (98,83 ± 10,54 мкм2 при деструктивном аппендиците и 91,36 ± 6,44 мкм2 ‒ при катаральном), уменьшению высоты эритроцита (534 ± 125 нм при деструктивном аппендиците и 553 ± 105 нм ‒ при катаральном) и глубины его центральной ямки (373 ± 114 нм при деструктивном аппендиците и 395 ± 155 нм ‒ при катаральном) при практически одинаковом объеме клетки в обеих группах (28,08 ± 4,46 мкм3 при деструктивном аппендиците и 28,46 ± 2,86 мкм3 ‒ при катаральном)
Анализ динамики морфофункциональных особенностей эритроцитов у детей с острым деструктивным аппендицитом в процессе лечения выявил следующие характерные особенности. Площадь эритроцита при поступлении была достоверно выше (98,83 ± 10,54 мкм2 при поступлении и 89,05 ± 8,24 мкм2 ‒ при выписке, p < 0,05), объем клетки при поступлении также был достоверно выше (28,08 ± 4,46 мкм3 ‒ при поступлении и 24,26 ± 2,8 мкм3 ‒ при выписке, p < 0,05). Аналогичная динамика отмечена для диаметра центральной ямки эритроцита (5,69 ± 0,43 мкм при поступлении и 5,35 ± 0,34 мкм ‒ при выписке, p < 0,05). Изменения глубины центральной ямки имели обратную динамику – при поступлении она была меньше (373 ± 114 нм при поступлении и 464 ± 105 нм ‒ при выписке, p < 0,05).
Таблица 2
Статистически значимые отличия морфофункциональных особенностей эритроцитов у детей с острым деструктивным аппендицитом при поступлении и при выписке (p < 0,05)
|
Поступление |
Выписка |
|
|
Плошадь эритроцита, мкм2 |
98,83 ± 10,54 |
89,05 ± 8,24 |
|
Объем эритроцита, мкм3 |
28,08 ± 4,46 |
24,26 ± 2,8 |
|
Диаметр центральной ямки эритроцита, мкм |
5,69 ± 0,43 |
5,35 ± 0,34 |
|
Глубина центральной ямки эритроцита, нм |
373 ± 114 |
464 ± 105 |
При сопоставлении морфофункциональных особенностей эритроцитов у детей с острым деструктивным аппендицитом при поступлении с контрольной группой выявлены следующие характерные особенности. Площадь эритроцита при деструктивном аппендиците была достоверно выше (98,83 ± 10,54 мкм2 при деструктивном аппендиците и 90,25 ± 7,26 мкм2 ‒ в контроле, p < 0,05), диаметр клетки при деструктивном аппендиците также был достоверно выше (7,84 ± 0,35 мкм при деструктивном аппендиците и 7,48 ± 0,37 мкм ‒ в контроле, p < 0,05). Аналогичная динамика отмечена для диаметра центральной ямки эритроцита (5,69 ± 0,43 мкм при деструктивном аппендиците и 5,33 ± 0,25 мкм ‒ в контроле, p < 0,05).
Таблица 3
Статистически значимые отличия морфофункциональных особенностей эритроцитов у детей из контрольной группы и у детей с острым деструктивным аппендицитом при поступлении (p < 0,05)
|
Деструктивный аппендицит |
Контроль |
|
|
Площадь эритроцита, мкм2 |
98,83 ± 10,54 |
90,25 ± 7,26 |
|
Диаметр эритроцита, мкм |
7,84 ± 0,35 |
7,48 ± 0,37 |
|
Диаметр центральной ямки эритроцита, мкм |
5,69 ± 0,43 |
5,33 ± 0,25 |
Помимо указанных статистически достоверных отличий отмечена тенденция к увеличению диаметра клетки и уменьшению ее высоты (отношение диаметра клетки к ее высоте при поступлении 16,21 ± 4,83, при выписке 13,74 ± 2,47).
Подводя итог, можно утверждать, что увеличение диаметра эритроцита и его центрального углубления и характерно для всех форм острого аппендицита. В то же время для деструктивного аппендицита характерно увеличение площади поверхности. Учитывая, что и для некоторых других хирургических заболеваний, в частности, для обтурационной желтухи выявлены сходные изменения [2], указанные параметры, вероятнее всего, являются маркером интоксикации организма, наиболее целесообразно использование их не в качестве самостоятельного дифференциально-диагностического критерия, а как дополнительный критерий оценки тяжести состояния больного.
Рецензенты:
Медведев Д.С., д.м.н., доцент, с.н.с., ФГУП «НИИ гигиены, профпатологии и экологии человека» ФМБА России, Ленинградская обл.;
Суворова К.Н., д.м.н., профессор, профессор-консультант медицинского центра «Ваша клиника» ООО «БелМедИнвест», г. Москва.
Работа поступила в редакцию 18.07.2013.



