Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
CHEMICAL COMPOSITION OF AERIAL PARTS OF GINSENG
Корни женьшеня настоящего (Panax ginseng C.A. Meyer.) широко используются в медицинской практике как общетонизирующие и адаптогенные средства. В РФ сырье используется преимущественно для получения настойки, за рубежом – для производства эликсиров, таблеток, комбинированных витаминных препаратов [2, 4, 7].
В РФ осуществляется промышленное культивирование женьшеня как в европейской части страны (Самарская, Брянская, Тверская области), так и на Дальнем Востоке (Приморский край). При сборе корней остается значительная фитомасса надземной части растения. Существуют научные данные о противогипоксическом, актопротекторном, термопротекторном, стресспротекторном и адаптогенном действии извлечений из травы женьшеня [1, 5, 6]. Поэтому с точки зрения ресурсосберегающих технологий актуальным и перспективным является изучение листьев и стеблей женьшеня, сравнение их химического состава с активными компонентами корней и оценка биологической активности.
Целью настоящего исследования являлась оценка качественного и количественного состава сапонинов и флавоноидов в надземной части женьшеня.
Материал и методы исследования
Объектом исследования служили стебли и листья женьшеня настоящего, культивируемого в Самарской области (КФК «Питомник «Женьшень», г. Жигулевск). Сбор растительного материала осуществляли в июне-сентябре 2011–2012 гг. и подвергали сушке в хорошо проветриваемом помещении без доступа прямых солнечных лучей.
В ходе работы применялись такие методы исследования, как тонкослойная хроматография (ТСХ), бумажная и адсорбционная жидкостная колоночная хроматография, кристаллизация и перекристаллизация, УФ-, ЯМР-спектроскопия и масс-спектрометрия, кислотный и ферментативный гидролиз, а также статистические методы обработки данных. Масс-спектры регистрировали на масс-спектрометре Kratos MS-30 (UK), ЯМР-спектры записывали на приборе Bruker AM300. УФ-спектры получали на спектрофотометре «Specord 40» (Analytik Jena).
Результаты исследования и их обсуждение
Методом адсорбционной жидкостной колоночной хроматографии с использованием различных сорбентов (силикагель L 40/100 и полиамид) и путем последующей перекристаллизации из надземной части женьшеня выделено вещество, которое по физико-химическим константам, данным УФ-, ЯМР- и масс-спектрам предварительно охарактеризовано как 3-О-диксилозид 3,5,7,4’ – тетрагидроксифлавона (кемпферол-3-О-диксилозид) (рис. 1).
В гликозидной хроматографической системе н-бутанол – ледяная уксусная кислота – вода (БУВ) в соотношении 4:1:2 вещество имеет хроматографическую подвижность с Rf ~ 0,5 и проявляется в виде ярко-желтого пятна 3 % раствором алюминия хлорида (рис. 2) и в виде оранжевого пятна – раствором диазобензолсульфокислоты в насыщенном растворе натрия карбоната. При перекристаллизации выпадает из спирта в ацетон в виде мелкодисперсного порошка светло-желтого цвета. Спектр выделенного вещества в УФ-области имеет максимумы поглощения при 271 ± 2 и 355 ± 2 нм. УФ-спектры комплексов вещества с алюминия хлоридом м натрия ацетатом, а также дифференциальный спектр представлены на рис. 3 и 4.
3-О-диксилозид кемпферола
Желтое кристаллическое вещество состава С25Н26О16.
Масс-спектр (m/z): 286 (М+ агликона).
УФ-спектр: lmax 271, 355 нм.
1Н-ЯМР-спектр в DMSO-d6 300 МГц (δ, м.д.): 12,67 (с, 1Н, 5-ОН), (д, 9 Гц, 2Н, Н-21,61), 6,86 (д, 9 Гц, 2Н, Н-31,51), 6,43 (д, 2 Гц, 1Н, Н-8), 6,19 (д, 2 Гц, 1Н, Н-6), 5,68 (д, 7 Гц, 1Н, Н-111 ксилозы), 4,53 (1Н, Н-1111 ксилозы), 3,0–4,95 диксилозид (м, 10Н двух молекул ксилозы).
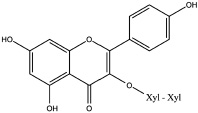
Рис. 1. Формула и 1Н-ЯМР-спектр кемпферол-3-О-диксилозида
а  б
б 
Реактивы: а- 20 % спиртовой раствор ФВК; б - 3 % спиртовой раствор AlCl3
Рис. 2. Схема ТСХ в системе БУВ (4:1:2):1 – извлечение из корней женьшеня (70 % этанол); 2 – извлечение из надземной части женьшеня (70 % этанол); 3 – рабочий стандартный образец (РСО) гинзенозида Rg1; 4 – доминирующий флавоноид женьшеня
Методом дифференциальной УФ-спектрофотометрии определено содержание суммы флавоноидов в листьях и стеблях женьшеня, а также суммарно в траве женьшеня в пересчете на государственный стандартный образец (ГСО) рутин (рис. 5, табл. 1).
Для количественной оценки суммы сапонинов в надземной части женьшеня адаптирована разработанная ранее методика определения суммы сапонинов в корнях женьшеня [3], предусматривающая использование рабочего стандартного образца (РСО) гинзенозида Rg1 или удельного показателя поглощения комплекса гинзенозида с 70 % серной кислотой (25). Методика модифицирована путем введения стадии очистки извлечения из травы женьшеня от хлорофилла и других липофильных веществ, легко окисляющихся серной кислотой, путем экстракции нативного извлечения хлороформом. Содержание суммы сапонинов в стеблях и листьях женьшеня, определенное с помощью данной методики, представлено в табл. 1.
Метрологические характеристики методик количественного определения суммы сапонинов и суммы флавоноидов в надземной части женьшеня представлены в табл. 2 и 3 соответственно.
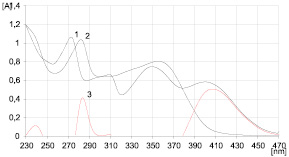
Рис. 3. Спектры поглощения раствора флавоноида:1 – исходного раствора; 2 – после добавления алюминия хлорида; 3 – дифференциальный спектр исходного раствора на фоне комплекса с алюминия хлоридом
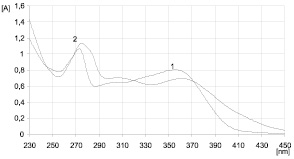
Рис. 4. Спектры поглощения раствора флавоноида:1 – исходного раствора; 2 – после добавления ацетата натрия
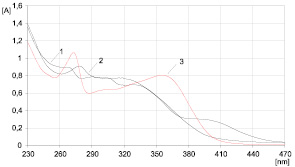
Рис. 5. Спектры поглощения извлечения из надземной части женьшеня:1 – исходного раствора (разведения 1:50); 2 – после добавления комплексообразователя алюминия хлорида; 3 – флавоноида, выделенного из травы женьшеня
Таблица 1
Содержание различных групп биологически активных веществ (БАВ) в частях растения, %
|
Группа БАС Сырье |
Сапонины (в пересчете на РСО гинзенозида Rg1) |
Флавоноиды (в пересчете на ГСО рутина) |
|
Корни |
6,11 ± 0,272 |
–– |
|
Листья |
4,30 ± 0,078 |
1,20 ± 0,053 |
|
Стебли |
1,30 ± 0,066 |
0,50 ± 0,032 |
|
Надземная часть (трава) |
3,10 ± 0,125 |
0,90 ± 0,029 |
Таблица 2
Метрологические характеристики методики количественного определения содержания суммы сапонинов в надземной части женьшеня
|
n |
f |
|
S |
S2 |
P, % |
t (P,f) |
ΔX |
E, % |
|
7 |
6 |
3,10 |
0,0510 |
0,0026 |
95 |
2,45 |
± 0,125 |
± 4,48 |
Таблица 3
Метрологические характеристики методики количественного определения содержания суммы флавоноидов в надземной части женьшеня
|
n |
f |
|
S |
S2 |
P, % |
t (P,f) |
ΔX |
E, % |
|
7 |
6 |
0,90 |
0,0118 |
0,00014 |
95 |
2,45 |
± 0,029 |
± 3,21 |
Выводы
1. Из надземной части женьшеня настоящего выделено вещество флавоноидной природы и установлены его спектральные и хроматографические свойства, позволяющие предварительно идентифицировать флавоноид как 3-О-диксилозид кемпферола.
2. Разработана методика количественного определения суммы сапонинов в надземной части женьшеня в пересчете на PCO гинзенозид Rg1.
3. Разработана методика оценки количественного содержания флавоноидов в надземной части женьшеня в пересчете на ГСО рутин.
4. С помощью разработанных методик получены данные о количественном содержании суммы сапонинов и суммы флавоноидов в надземной части женьшеня. Статистическая обработка данных позволяет сделать вывод о том, что ошибки единичных определения составляет ± 4,48 и ± 3,21 % соответственно.
Рецензенты:
Первушкин С.В., д.фарм.н., профессор, зав. кафедрой фармацевтической технологии, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения РФ, г. Самара;
Авдеева Е.В., д.фарм.н., профессор кафедры фармакогнозии с ботаникой и основами фитотерапии, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения РФ, г. Самара.
Работа поступила в редакцию 01.07.2013.
Библиографическая ссылка
Акушская А.С. ХИМИЧЕСКИЙ СОСТАВ НАДЗЕМНОЙ ЧАСТИ ЖЕНЬШЕНЯ // Фундаментальные исследования. 2013. № 8-2. С. 385-388;URL: https://fundamental-research.ru/en/article/view?id=31928 (дата обращения: 16.05.2026).





