Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
TREATMENT HYPERTROPHIC AND KELOIDNYKH OF HEMS
В течение ХХ-го века было сделано множество попыток найти способ эффективной коррекции рубцов. Среди них определенное место занимала общая терапия – инъекции алоэ или стекловидного тела; оксигенотерапия; лечение пирогеналом, мацестинскими сероводородными водами [1, 5]. Однако наиболее многочисленными и эффективными стали методы местного воздействия на рубцы. К ним относятся: применение гидрокортизона и его аналогов в виде мазей или инъекций (триамцинолон или «Кеналог-40»); рентгентерапия; лечение рубцов давящими повязками; криотерапия жидким азотом; лазеротерапия; применение силиконовых пластин и др. [2, 4].
Во второй половине нашего века отношение к рубцам стало постепенно изменяться. С одной стороны, этому способствовало развитие пластической хирургии, а с другой – все большее понимание обществом цивилизованных стран важнейшей роли внешнего вида в жизни каждого человека. Поэтому значительная часть пластических операций стала выполняться с целью повышения качества рубцов [2, 5].
Несмотря на бурное развитие хирургии, проблема улучшения качества рубцов по-прежнему волнует и пациентов, и хирургов. На качество будущего рубца влияют три основные группы факторов:
а) связанные с пациентом;
б) зависящие от хирурга;
в) определяемые объективными обстоятельствами, например, особенностями повреждения при открытых травмах, масштабы и сложность операции и т.д.
И здесь хирург сталкивается с необходимостью системного анализа ситуаций, который объективно труден и субъективно несовершенен. Тем более что все попытки повлиять на биологически детерминированный процесс формирования рубцовой ткани имеют жесткие рамки возможного.
Гипертрофические рубцы и келоид могут быть описаны как разновидности обычного заживления раны. С развитием рубца предел его прочности увеличивается в результате прогрессивных связей волокон коллагена. Когда появляется несоответствие между анаболическими и катаболическими процессами, большее количество коллагена производится, чем деградирует, и рубец имеет тенденцию к росту во всех направлениях, поднят выше уровня кожи и остается гиперемированным, классифицируется как келоид или гипертрофический рубец. Келоидный рубец часто вызывает беспокойство в виде зуда, жжения, болезненности. Кроме того, келоидные и гипертрофические рубцы отличаются от здоровой кожи богатой сосудистой сетью, высокой плотностью мезенхимальных клеток и утолщенным эпидермальным слоем [1, 3].
Цель исследования – повышение эффективности лечения гипертрофических или келоидных рубцов кожи, получение косметического и функционального эффекта.
Материалы и методы исследования
Способ осуществляют следующим образом: в течение 4 недель троекратно в толщу рубца вводят дипроспан из расчета 7 мг на 5 см2, но не более 14 мг на весь рубец за один раз. После полученной медикаментозной гипотрофии, рубцовую ткань подвергают воздействию инфракрасного лазерного излучения длиной волны 540 нм, энергией импульса 50–150 мДж, частотой следования импульсов 1–4 Гц, длительностью импульса 1–2 нс (режим генерации Q-sw), получаемого с помощью активной среды Nd:YAP (Q-sw)/KTP медицинского лазерного аппарата Multiline (патент № 2323021).
Под нашим наблюдением находилось 22 пациента с гипертрофическими и келоидными рубцами кожи с преимущественным расположением в области грудины, наружной поверхности плеча и заушной области. Топография, размеры и возраст гипертрофических рубцов не носили принципиального характера, поэтому не подвергались клинической классификации. Возраст пациентов составлял от 20 до 44 лет.
Математическая обработка результатов исследований проводили с помощью пакета прикладных программ «Statistiсa 6.0» на персональном компьютере.
Значимость различий качественных показателей определяли с помощью критерия c2 и двухстороннего точного метода Фишера для четырехпольной таблицы. Относительные величины, выраженные в процентах, приводили в тексте статьи с ошибкой процента. Степень отличий считали значимой при р < 0,05.
Результаты исследования и их обсуждение
В результате проведения лечебных мероприятий у пациентов с гипертрофическими и келоидными рубцами кожи были изучены следующие показатели: высота рубца над поверхностью кожи, площадь рубца, консистенция, цвет, состояние окружающей кожи, микроциркуляция рубца.
Использование кортикостероида пролонгированного действия (дипроспана) в лечении гипертрофических или келоидных рубцов носит патогенетический характер, поскольку, ингибируя провоспалительные ферменты, гормоны, простогландины, интерлейкины, не только препятствует дальнейшему разрастанию рубцовой ткани, но и приводит к значительному ее лизису.
Применение высоких терапевтических доз дипроспана позволяет в короткие сроки привести келоидные рубцы к состоянию гипотрофии. И в результате перехода гипертрофического или келоидного рубца сперва в состояние гипотрофии, а после лазерного воздействия – нормотрофии, происходит не только изменение структуры рубцовой ткани, но и уменьшение первоначальной ее площади.
Благодаря скоротечному изменению толщины рубцовой ткани под воздействием дипроспана и лазерного излучения, происходит значительное уменьшение и площади рубца. Это свойство использовано в лечебных целях, поскольку мы планомерно достигаем гипотрофического результата, который в последующем переводим в состояние нормотрофии (рис. 1, 2, 3). На рис. 1 изображена схема рубцовой ткани до лечения. На рис. 2 изображена схема рубцовой ткани после лечения с помощью дипроспана (отмечается гипотрофия рубца):
1 – рубцовая ткань;
2 – поверхность кожи;
31 – размер рубца.
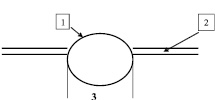
Рис. 1
На рис. 3. изображена схема рубцовой ткани после инфракрасного лазерного облучения (отмечается нормотрофия рубца):1 – рубцовая ткань; 2 – поверхность кожи; 32 – размер рубца. Динамика размеров рубца отмечалась следующая: 3 > 31 > 32.
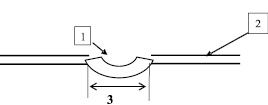
Рис. 2
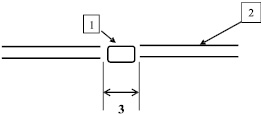
Рис. 3
На фоне использования инфракрасного лазерного излучения в режиме генерации Q-sw с длительностью импульса 1–2 нс происходит облитерация сосудов дна рубца без воздействия на собственно ткань рубца и на окружающие ткани. Через 8 недель от начала лечения отмечали уменьшение площади келоидных и гипертрофических рубцов в среднем на 23 ± 4,3 % (Р < 0,05) (табл. 1).
Таблица 1
Относительные показатели уменьшения площади рубцовой ткани на фоне лечения
|
До лечения |
1-я нед. |
2-я нед. |
4-я нед. |
6-я нед. |
8-я нед. |
|
100 % |
97,4 % |
94,1 % |
88,6 % |
82,9 % |
77,7 % |
Исследование состояния микроциркуляции рубца проводили методом лазерной доплеровской флоуметрии (ЛДФ) в красном спектре излучения с использованием лазерного анализатора капиллярного кровотока BLF-21.
Запись ЛДФ-грамм производилась до лазерной обработки, непосредственно после воздействия и на протяжении последующих 3 недель наблюдения. Измерения микроциркуляции проводили в области дна рубца и на симметричных точках здоровой кожи.
Сразу после лазерной обработки поверхности рубца отмечали снижение показателя микроциркуляции на 45 % по сравнению с исходными значениями (Р < 0,05) (табл. 2).
Таблица 2
Изменение тканевой перфузии в области дна рубца
|
Точка измерения |
Перфузия (перф. ед.) |
||||
|
до лазера |
ч/з 2 мин |
ч/з 7 дней |
ч/з 14 дней |
ч/з 21 день |
|
|
Дно рубца |
3,5 ± 0,43 |
1,94 ± 0,15* |
1,92 ± 0,18* |
1,90 ± 0,16* |
1,88 ± 0,22* |
|
симметричный участок кожи |
2,7 ± 0,2 |
2,6 ± 0,16 |
2,8 ± 0,21 |
2,7 ± 0,19 |
2,6 ± 0,14 |
Примечание. * – достоверность различий по сравнению с исходными данными при Р < 0,05.
На протяжении 3-недельного контроля показателя микроциркуляции у пациентов не происходило достоверного изменения перфузии патологического очага, что свидетельствует об эффективности однократного воздействия инфракрасного лазерного излучения на ткань рубца.
Заключение
Таким образом, использование инъекций дипроспана из расчета 7 мг на 5 см2, но не более 14 мг на весь рубец и в последующем инфракрасного лазера с длинной волны 540 нм, длительностью импульсов 1–2 нс (режим генерации Q-sw), с энергией 50–150 мДж и частотой следования импульса 1–4 Гц в лечении гипертрофических или келоидных рубцов позволяет получить стойкий клинический результат уже через 8 недель от начала лечения, заключающийся в уменьшении площади рубца (на 22,3 %), формировании нормотрофической рубцовой ткани, улучшении консистенции и изменении цвета, характерного для окружающей кожи. За счет сверхкороткого отрезка времени лазерного воздействия (1–2 нс), благодаря технологии Q-sw, способ является безболезненным и безопасным и не оказывает влияния на окружающие ткани, что подтверждается устойчивым клиническим результатом, наблюдаемым у пациентов через 1 год после лечения.
Рецензенты:
Штофин С.Г., д.м.н., профессор, заведующий кафедрой, Новосибирский государственный медицинский университет, г. Новосибирск;
Чернов В.Н., д.м.н., профессор, заведующий кафедрой общей хирургии Ростовского государственного медицинского университета, г. Ростов-на-Дону.
Работа поступила в редакцию 11.01.2013.
Библиографическая ссылка
Карапетян Г.Э., Пахомова Р.А., Кочетова Л.В., Соловьева Н.С., Назарьянц Ю.А., Василеня Е.С., Маркелова Н.М., Кузнецов М.Н., Арапова В.А., Гуликян Г.Н. ЛЕЧЕНИЕ ГИПЕРТРОФИЧЕСКИХ И КЕЛОИДНЫХ РУБЦОВ // Фундаментальные исследования. 2013. № 3-1. С. 70-73;URL: https://fundamental-research.ru/en/article/view?id=31148 (дата обращения: 04.05.2026).



