Известно, что местные и генерализованные тромбогеморрагические нарушения при заболеваниях пищеварительной системы встречаются весьма часто [1]. Грубые нарушения гомеостаза, возникающие при гнойно-септических осложнениях, острой кишечной непроходимости (ОКН), остром панкреатите и других острых абдоминальных хирургических патологиях, играют «триггерную» роль в развитии тромбогеморрагического синдрома [3, 4]. Ранняя правильная диагностика, незамедлительное адекватное оперативное вмешательство и своевременная коррекция нарушений гомеостаза, а также гемостаза являются залогом успеха в лечении больных с ОКН [5]. Определение характера нарушений гемостаза и их выраженности имеет большое значение как в диагностике, так и в лечении ОКН, являющейся одной из частых причин развития тромбогеморрагического синдрома [2].
Цель работы − выявление патогенетических механизмов и определение выраженности нарушений коагуляционно-литической системы тканей кишечника при различных формах (высокой и низкой) острой кишечной непроходимости.
Материалы и методы исследования
В основу работы положены материалы экспериментальных исследований, проведенных на 24 взрослых беспородных половозрелых собаках обоего пола массой от 7,9 до 12,6 кг. Изучали показатели системы гемостаза в общем и брыжеечном кровотоке, влияние экстрактов тканей кишечной стенки на некоторые показатели системы гемостаза на моделях острой высокой и низкой кишечной непроходимости. Оценивали показатели процессов перекисного окисления липидов, активность фосфолипазы А2 и антиоксидантных ферментов в тканях тонкой и толстой кишок. Вышеперечисленные показатели исследовали на фоне лечения, которое включало антибактериальную терапию (внутримышечные инъекции 2 раза в сутки раствора гентамицина из расчета 0,8 мг/кг массы тела), инфузионную терапию (внутривенные введения 5 % раствора глюкозы и 0,89 % раствора хлорида натрия из расчета 50 мл/кг массы животного).
В первой группе (n = 12) моделировали острую высокую кишечную непроходимость, во второй группе (n = 12) – острую низкую кишечную непроходимость. Животным выполняли срединный разрез вентральной стенки брюшной полости. В рану выводили тонкую или толстую кишку, которую перевязывали таким образом, чтобы не возникал некроз кишки в зоне лигатуры.
Через двое суток животным выполняли релапаротомию, устраняли кишечную непроходимость путем снятия лигатуры, брюшную полость санировали и ушивали наглухо. В контрольные сроки (1, 3, 5-е сутки) выполняли ререлапаротомию, проводили макроскопическую оценку органов брюшной полости, осуществляли забор крови из подкожных и брыжеечных вен, биопсию тонкой и толстой кишки.
Все вмешательства проводили под внутривенным тиопентал-натриевым наркозом (0,04 г/кг массы). После проведения исследований животных выводили из эксперимента введением летальной дозы тиопентал-натрия.
Исследования выполнялись в соответствии с этическими требованиями к работе с экспериментальными животными («Правила проведения работ с использованием экспериментальных животных» (приказ МЗ СССР № 755 от 12.08.1987 г.), Федеральный закон «О защите животных от жестокого обращения» от 01.01.1997 г., приказ МЗ РФ от 19.06.2003 г. № 267 «Об утверждении правил лабораторной практики»), одобрены локальным этическим комитетом.
В работе применялись следующие методы исследования: исследовали коагуляционный компонент гемостаза. Время спонтанного свертывания крови по R. J. Lee и P.D. White (1913), время рекальцификации обычной плазмы по Bergerhof и Roka (1954), толерантность плазмы к гепарину по Poller в модификации В.П. Балуды (1954), протромбиновое время плазмы по A.J. Quick (1966), концентрацию фибриногена по Р.А. Рутберг (1961), антитромбин III по A. Hensen, E.A. Loeliger в модификации К.М. Бышевского (1963), продукты деградации фибриногена и фибрина (ПДФ) в плазме по Nanniga Guest, естественный лизис кровяного сгустка по М.А. Котовщиковой и Б.И. Кузнику (1962), фибринолитическую активность эуглобулиновым методом по H. Kowarzyk, L. Buluck (1954). Коагуляционно-литическое состояние тканевых структур кишечника определялось указанными тестами при добавлении в реагирующую смесь экстракта ткани кишечника, для получения которого использовали способ В.П. Скипетрова (1969). Содержание диеновых и триеновых конъюгатов оценивали спектрофотометрическим методом (Ганстон Ф.Д., 1986). Уровень малонового диальдегида определяли спектрофотометрическим методом по реакции с тиобарбитуровой кислотой (Sigma) (Егоров Д.Ю., Козлов А.В., 1988). Активность супероксиддисмутазы определяли по способности фермента тормозить аэробное восстановление нитросинего тетразолия до формазана (Гуревич В.С. и др., 1990; Досон Р. и др., 1991). Активность фосфолипазы А2 оценивали в среде, содержащей 10 ммоль трис-HCl-буфер (рH 8,0), 150 ммоль тритона Х-100, 10 ммоль CaCl2 и 1,2 ммоль субстрата, в качестве которого использовали фосфатидилхолины яичного желтка. Полученные цифровые данные обрабатывали методом вариационной статистики с использованием критерия t Стьюдента. В каждой серии определяли достоверность различия по отношению к исходному или контрольному значению (Р). Вычисления производили на CPU 1600 MHz «Intel Pentium-IV» с помощью пакета программ Microsoft Office XP.
Результаты исследования и их обсуждение
Изучение показателей системы свертывания крови в плазме крови общего кровотока при острой кишечной непроходимости выявило следующие результаты.
При острой высокой кишечной непроходимости были отмечены существенные изменения показателей гемостазиограммы. Укорачивалось время свертывания крови на 1-е сутки после операции на 18,9 % (p < 0,05), к 3-м суткам – на 20,5 % (p < 0,05) и к 5-м суткам – на 12,8 % (p < 0,05). Время рекальцификации плазмы достоверно снижалось. Так, через сутки оно было ниже нормы на 25,4 % (p < 0,05), через трое суток – на 24,7 % (p < 0,05), а к конечному этапу наблюдения – на 16,2 % (p < 0,05). При острой высокой кишечной непроходимости достоверно нормы была снижена толерантность плазмы к гепарину на 18,1, 15,4 и 10,4 % соответственно (p < 0,05) этапам наблюдения. Протромбиновое время было укорочено на всех сроках наблюдения. Так, через сутки от начала инфузионной терапии оно было ниже нормы на 32,3 % (p < 0,05), через трое суток – на 24,9 % (p < 0,05), а к конечному этапу наблюдения – на 20,4 % (p < 0,05). Тромбиновое время на 1-е сутки терапии было уменьшено на 35,6 % (p < 0,05), на 3-и сутки – на 20,8 % (p < 0,05), а на конечном этапе наблюдения – на 13,6 % (p < 0,05). При острой высокой кишечной непроходимости снижался антикоагулянтный потенциал. Так, содержание антитромбина III в контрольной группе было снижено на всех сроках наблюдения. На 1-е сутки его содержание было достоверно ниже нормы на 35,4 % (p < 0,05), на 3-и – на 22,0 % (p < 0,05) и на 5-е – на 17,5 % (p < 0,05). Развитие острой высокой кишечной непроходимости способствовало угнетению фибринолитической активности эуглобулинов. Зафиксировано выраженное угнетение и спонтанного фибринолиза. В течение всего периода наблюдения за животными в первой группе достоверно нормы было увеличено содержание продуктов деградации фибрина – на 1-е сутки наблюдения – на 68,8 % (p < 0,05), на 3-и сутки – на 47,1 % (p < 0,05), на 5-е сутки – на 32,7 % (p < 0,05).
Изучение данных показателей при низкой кишечной непроходимости выявило, что изменения гуморального компонента системы гемостаза были аналогичны, но значительно менее выражены (рис. 1).
Под влиянием экстракта кишечной стенки показатели гемостаза при острой высокой кишечной непроходимости имели достоверные отличия от исхода на всех сроках исследования. При острой высокой кишечной непроходимости тканевый экстракт укорачивал время рекальцификации плазмы на 1-е сутки наблюдения – на 35,7 % (p < 0,05), на 3-и сутки – на 30,2 % (p < 0,05) и на 5-е сутки – на 29,1 % (p < 0,05). Каолиновое время было снижено через сутки от начала инфузионной терапии – на 25,2 % (p < 0,05), через трое суток – на 24,7 % (p < 0,05), а к конечному этапу наблюдения – на 19,0 % (p < 0,05). Через сутки от начала терапии прокоагулянтная активность экстракта тканей кишечной стенки возрастала, что установлено ускорением протромбинового и тромбинового времени соответственно на 30,6 и 38,8 % (p < 0,05), через трое суток – на 24,2 и 32,8 % (p < 0,05), а к конечному этапу наблюдения – на 21,1 и 28,6 % (p < 0,05).
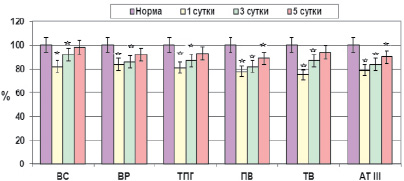
Рис. 1. Состояние системы свертывания крови при острой низкой кишечной непроходимости на фоне инфузионной терапии (ВС – время свертывания; ВР – время рекальцификации плазмы, ТПГ – толерантность плазмы к гепарину, ПВ – протромбиновое время, ТВ – тромбиновое время; АТ III – антитромбин III). Нормальные значения показателей приняты за 100 %; * – данные, изменение которых достоверно по отношению к норме
При низкой кишечной непроходимости влияние экстракта тканей толстой кишки на показатели гемостаза было менее выраженным (таблица).
Влияние экстрактов тканей кишечной стенки на некоторые показатели системы гемостаза при острой низкой кишечной непроходимости (M ± m)
|
Показатель |
Норма |
Этапы наблюдения |
||
|
1-е сутки |
3-и сутки |
5-е сутки |
||
|
Время рекальцификации, с |
24,92 ± 1,14 |
19,54 ± 0,66* |
20,20 ± 0,71* |
23,16 ± 1,33 |
|
Каолиновое время, с |
28,07 ± 1,41 |
23,37 ± 0,79* |
25,63 ± 0,84 |
27,52 ± 1,14 |
|
Протромбиновое время, с |
20,84 ± 0,93 |
16,42 ± 0,69* |
17,12 ± 0,72* |
19,97 ± 0,96 |
|
Тромбиновое время, с |
23,56 ± 1,05 |
15,70 ± 0,68* |
18,47 ± 0,79* |
20,88 ± 0,84 |
|
Эуглобулиновый фибринолиз, мин |
86,74 ± 4,21 |
129,57 ± 7,94* |
111,64 ± 7,35* |
108,61 ± 7,21* |
Примечание. * – достоверность изменений по отношению к норме при p < 0,05.
Изучение состояния процессов перекисного окисления липидов и активности фосфолипазных систем тканей кишки при исследованных видах кишечной непроходимости показало, что интенсификация липопереокисления в тканях тонкой и толстой кишки происходит с различной интенсивностью.
Так, при высокой кишечной непроходимости в тканях тонкой кишки содержание диеновых конъюгатов (ДК) было повышено на 32,1–40,0 % (р < 0,05), триеновых конъюгатов (ТК) – на 38,0–48,2 % (р < 0,05), концентрация малонового диальдегида (МДА) превышала норму на 52,5–66,3 % (р < 0,05). Выявлено угнетение системы антиоксидантной защиты, что проявлялось в снижении активности супероксиддисмутазы (СОД) на 13,9–35,2 % (р < 0,05). Активность фосфолипазы А2 (ФЛА2) была повышена на 40,8–72,7 % (p < 0,05).
При низкой кишечной непроходимости данные показатели исследованных процессов в тканях толстой кишки были также изменены, но в меньшей степени (рис. 2).
Проведение корреляционного анализа выявило наличие прямой сильной зависимости показателей перекисного окисления липидов, активности ферментов в ткани кишки и показателей системы гемостаза тканей органа (r = 0,84–0,98).
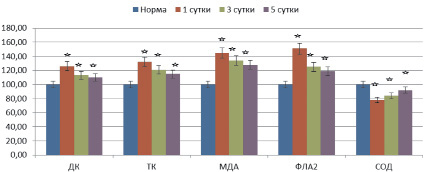
Рис. 2. Динамика молекулярных продуктов липопереокисления в ткани толстой кишки при острой низкой кишечной непроходимости. Примечание: нормальные значения показателей приняты за 100 %; * – данные, изменение которых достоверно по отношению к норме при p < 0,05
Выводы
1. При острой кишечной непроходимости нарушения в системе гемостаза отмечаются не только на организменном, но и на местном уровне – в тканевых структурах кишечной стенки.
2. Более значимые тромбогеморрагические нарушения в тканевых структурах кишечника возникают при высокой кишечной непроходимости.
3. Тромбогеморрагические нарушения в тканевых структурах кишечной стенки при острой кишечной непроходимости сопряжены с интенсивностью процессов перекисного окисления липидов, фосфолипазной активностью. В тонкой кишке указанные процессы протекают более интенсивно.
Рецензенты:
Смолькина А.В., д.м.н., профессор кафедры госпитальной хирургии медицинского факультета им. Т.З. Биктимирова, ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск;
Рубцов О.Ю., д.м.н., профессор кафедры факультетской хирургии, ФГБОУ ВПО «Мордовский государственный университет им. Н.П. Огарёва», г. Саранск.
Работа поступила в редакцию 06.12.2012.
Библиографическая ссылка
Власов А.П., Шибитов В.А., Царьков И.В., Власов П.А., Кормишкин А.Е. КОАГУЛЯЦИОННО-ЛИТИЧЕСКОЕ СОСТОЯНИЕ ТКАНЕЙ КИШЕЧНИКА ПРИ ОСТРОЙ КИШЕЧНОЙ НЕПРОХОДИМОСТИ // Фундаментальные исследования. 2013. № 2-1. С. 43-43;URL: https://fundamental-research.ru/en/article/view?id=31050 (дата обращения: 21.04.2026).



