Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
INFLUENCE OF SOLS PREPARATION ON THE MORPHOLOGY OF THE SAMPLES WITH NANO-η-TIO2
Уникальность образцов с наночастицами основана на том, что при уменьшении размеров частиц меняются такие свойства веществ (в зависимости от состава), как растворимость, прозрачность, цвет, электропроводность, температура плавления, температура фазовых переходов и др. и появляются новые – (фото)каталитические и сорбционные. Это обусловлено тем, что поверхностные атомы не связаны с соседними атомами, они обладают свободными связями и очень активны. Большее количество поверхностных атомов увеличивает каталитическую активность частиц – способность вещества ускорять химическую реакцию, не вступая в нее. Это качество делает образцы с наночастицами привлекательными для применения. Однако, если активные поверхности никак не защищены, наночастицы быстро объединяются в силу их высокой поверхностной энергии в группы – агрегаты (химически связанные друг с другом частицы) или агломераты (скопление агрегатов, связанных между собой посредством более слабых сил Ван-дер-Ваальса). Между агрегатами и агломератами существуют переходные состояния, но самое главное − они намного больших, чем наночастицы, размеров, меньшей удельной поверхности, у них теряются преимущества нанообъектов и по сравнению с нанообъектами они менее активны, т.е. у них уменьшается реакционная способность [2].
На рис. 1 представлены основные модели наночастиц.
1 модель. Размеры наночастицы (N) и области когерентного рассеяния D совпадают (N = D): наночастица состоит только из ядра.
2 модель. Размеры D и N не совпадают (D < N): наночастица состоит из ядра и внешнего слоя (core – shell структура).
3 модель. Размеры наночастицы (N), кристаллита (L) и области когерентного рассеяния (ОКР = D) не совпадают (N ≠ D ≠ L). Это связано с дефектной структурой нанообъекта (двойниками, некогерентными границами, малоугловыми областями). Необходимо обратить внимание, что в данной работе области когерентного рассеяния (величина D) приравнивается к размеру кристаллита (D = L).
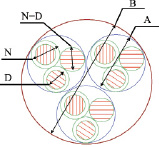
Рис. 1. Схематичное изображение нанообъекта: В – агломерат, А – агрегат, N – наночастица, D – область когерентного рассеяния (ОКР)
Наночастицы объединяются в агрегаты (А) и агрегаты в агломераты (В). Еще одной из особенностей агрегации частиц является иерархическое устройство агрегатов: при электронно-микроскопическом изучении становится видно, что имеются как минимум два-три уровня взаимной организации частиц, более крупные ансамбли состоят из более мелких и так далее [1]. В связи с этим появляется необходимость в разрушении агрегатов, что возможно, например, применением ультразвуковой обработки, однако в течение очень небольшого периода времени наночастицы снова агрегируют [1]. Не исключено, что направленное получение заданных размеров частиц в золях позволит варьировать ими и в твердом состоянии, т.е. в скоагулированных и высушенных образцах. Это и послужило мотивацией данной работы – нахождение возможной связи размеров частиц в золях и в образцах с нано-η-TiO2.
Материалы и методы исследования
В качестве исходных объектов использовались золи, которые были получены гидролизом в течение τгидр = 90 с водного раствора TiOSO4×xH2SO4×yH2O с концентрацией c0 = 0,5 моль/л при варьировании температуры гидролиза (tгидр, °С) и времени старения (tстар, сутки).
Характеризация золей осуществлялась методом динамического рассеяния света (ДРС) [4] на фотонном анализаторе частиц Zetasizer NanoZS фирмы «Malvern» (Великобритания): диапазон измерений частиц от 0,6 до 6000 нм; рабочий интервал температур – от 2 до 120 ° С; угол детектирования рассеянного света 173°; источник света – гелий-неоновый лазер с длиной волны 633 нм; мощность источника света 5 мВт. На рис. 2 представлено схематичное изображение частиц на основе диоксида титана в золе.
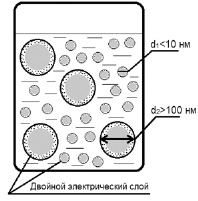
Рис. 2. Схематичное изображение частиц на основе TiO2 с бимодальным распределением гидродинамических диаметров
Установлено, что в золях с TiO2 присутствуют частицы с бимодальным распределением гидродинамических диаметров (диаметр сферы, испытывающей то же сопротивление среды, что и исследуемая частица) наночастиц с d1 < 10 нм и их содержанием ξ1 = 8...93 % и агрегатов с диаметром d2 > 100 нм (рис. 3).
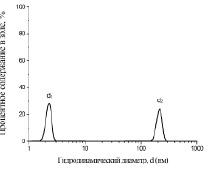
Рис. 3. Статистическое распределение частиц в золях с TiO2
Образцы получены коагуляцией золей 1,3 М водным раствором KCl, отфильтрованы, промыты дважды H2O и дважды ацетоном ((CH3)2C = O), просушены в сушильном шкафу при температуре 50...60 °С в течение 2 часов.
Образцы с нано-η-TiO2 охарактеризованы методами малоугловой (МУРР; специализированный малоугловой дифрактометр SAXSess, CuKα, линейная коллимация, время измерений – 3 мин, съемка на просвет в области углов 2q = 0...40°; функции распределения частиц и агрегатов частиц по размерам рассчитаны из кривых малоуглового рассеяния в области углов 2q = 0...7° с помощью программы GNOM с использованием аппроксимаций формы частиц в виде сфер) [5] и широкоугловой (ШУРР; ДРОН-З, графитовый плоский монохроматор, CuK на дифрагированном пучке в пошаговом режиме: время набора импульсов − 10 с, величина шага − 0,02°; съемка на отражение в интервале углов 2...50°2q) рентгенографии. Размер областей когерентного рассеяния (величина D, Å) определен по формуле Дебая−Шеррера: D = 0,9l/βcos q, где l длина волны, 2q ~ 25°, b – ширина пика на половине высоты), а размер наночастиц (величина N, нм) и агрегатов (величина А, нм) – сканирующей электронной микроскопии (СЭМ; микроскоп высокого разрешения JSM 7500F, режим низкоэнергетических вторичных электронов, энергия первичного пучка − 20 кВ, разрешение − 1 нм).
Результаты исследований и их обсуждение
Величины d1, d2 и ξ1 в золях по-разному зависят от условий процесса: с ростом τгидр величины d1 (рис. 4 а) и d2 (рис. 4 б) увеличиваются, с увеличением tгидр и c0 величина d1 увеличивается, а d2 уменьшается; величина ξ1 увеличивается с ростом величин τгидр, tгидр, c0 и уменьшается с увеличением tстар.
а)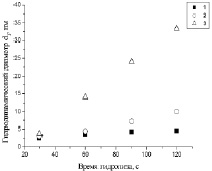 б)
б) 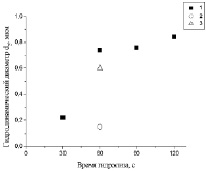
Рис. 4. Зависимость гидродинамического диаметра наночастиц d1 (а) и агрегатов (d2) (б) от времени гидролиза: 1 – tстар = 1 сутки, 2 – tстар = 12 суток, 3 – tстар = 30 суток
Вариация значениями tгидр и tстар позволила получить золи с разным набором величин d1, d2 и ξ1, в частности (таблица):
ЗОЛЬ 1:τгидр = 90 с, tгидр = 70 °С, с0 = 0,5 моль/л, tстар = 52 суток.
ЗОЛЬ 2: τгидр = 90 с, tгидр = 65 °С, с0 = 0,5 моль/л, tстар = 98 суток.
ЗОЛЬ 3: τгидр = 90 с, tгидр = 75 °С, с0 = 0,5 моль/л, tстар = 98 суток.
Характеристики золей и полученных из них образцов с η-TiO2
|
Характеристика золей |
ЗОЛЬ 1 |
ЗОЛЬ 2 |
ЗОЛЬ 3 |
|
d1, нм |
2,5(2) |
5,8(3) |
5,8(6) |
|
ξ1, % |
85 |
93 |
8 |
|
d2, нм |
110(15) |
142(20) |
2606(100) |
|
Характеристика образцов |
Образец 1 |
Образец 2 |
Образец 3 |
|
D, Å |
18,4(1) |
21,8(1) |
21,4(1) |
|
N, нм |
~10...~20* |
~10...~20 |
~10...~20 |
|
A, нм |
~30...100* |
~50...~70 |
~100...~150 |
Примечание. * Разделение на наночастицы – N и агрегаты – A условно.
Образцы 1, 2 и 3 получены коагуляцией золей 1, 2 и 3 соответственно (см. таблицу). По результатам, полученным методом МУРР, можно заключить, что наночастиц в образце 1 или нет или их немного. Наличие широких «аморфных» пиков скорее указывает на то, что образец является аморфным, и основная доля рассеивателей обладает размерами, превышающими разрешение прибора (частицы более 40 нм). Из отсутствия сколько-нибудь четкого прямолинейного участка на графике Гинье следует вывод о сильной полидисперсности образцов. Таким образом, наноразмерные неоднородности электронной плотности имеют очень широкое распределение по размерам, и основная их доля представлена частицами с размерами более 60 нм, хотя есть наночастицы и меньшего размера (~20 нм и меньше).
На рис. 5 представлены дифрактограммы образцов 1, 2 и 3 с нано- η-TiO2, полученных методом ШУРР.
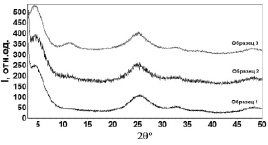
Рис. 5. Дифрактограммы образцов 1, 2 и 3 с нано-η-TiO2
Все образцы содержат фазу со структурой η-TiO2 (характерные отражения при 2Θ~5°, ~25°, ~33°) [3], а образец 3 дополнительно фазу с 2Θ~12°. Фазовый анализ не позволил по одному отражению уверенно определить примесную фазу, но тем не менее этот пик характерен для фаз H2TixOy (в частности, H2Ti3O7 (JCPDS № 47–0561), H2Ti2O5×H2O (JCPDS № 47–0124), TiO2×nH2O, TiO(OH)2, Ti4O7(OH)2×H2O (JCPDS № 48–1278) и титанатов (в дальнейшем будем называть эту фазу «гидролизный диоксид титана»).
Результаты СЭМ cвидетельствуют о присутствии агломератов наряду с агрегатами в образце 1 (рис. 6,а) и подтверждают его полидисперсность (см. таблицу).
 б)
б)  в)
в) 
Рис. 6. Микрофотографии СЭМ образца 1 (а), образца 2 (б) и образца 3 (в)
Образцы 2 (рис. 6,б) и 3 (рис. 6,в) больше напоминают фрактальные образования с заметно отличающимися размерами агрегатов – А (см. таблицу), но с их узким распределением по сравнению с образцом 1, и практически одинаковыми размерами наночастиц – N (см. таблицу).
Из оценочных значений величин областей когерентного рассеяния – D и сопоставление их с размерами наночастиц – N (таблица), данных МУРР и ШУРР следует, что в образцах 1–3 большая доля аморфной составляющей (N >> D): наночастица состоит из ядра (ОКР = D) и внешнего слоя – модель 2 (напомним, что мы не рассматриваем здесь модель 3) (см. рис. 1), а агрегат состоит из наночастиц и также аморфной прослойки, что подтверждается дифрактограммой образца 3 (см. рис. 5). В последнем образце присутствует аморфный гидролизный диоксид титана, который в образцах 1 и 3, вероятнее всего, рентгеноаморфный.
Таким образом, результаты работы свидетельствуют о том, что tгидр не оказывает влияние на величины D и N в отличие от tстар, причем величины D и d1 коррелируют друг с другом, так же как и величины A и d2. Отсюда следует возможность изменять размеры агрегатов в образцах, варьируя условиями синтеза, не применяя внешние воздействия на образцы (например, ультразвуковую обработку), которые могут оказывать отрицательное действие на свойства.
Исследование выполнено при поддержке Министерства образования и науки Российской Федерации, соглашение 14.B37.21.1621.
Рецензенты:
Киселева Н.Н., д.х.н., зав. лабораторией полупроводниковых материалов Федерального государственного бюджетного учреждения науки Института металлургии и материаловедения имени А.А. Байкова Российской академии наук, г. Москва;
Самойлович М.А., д.ф-м.н., профессор, начальник научно-исследовательской лаборатории наноструктур и фотонных кристаллов ОАО ЦНИТИ «Техномаш».
Работа поступила в редакцию 11.01.2013.
Библиографическая ссылка
Гайнанова А.А., Кузьмичева Г.М., Доморощина Е.Н., Серхачева Н.С., Садовская Н.В., Прокопов Н.И. ИССЛЕДОВАНИЕ ВЛИЯНИЯ УСЛОВИЙ ПОЛУЧЕНИЯ ЗОЛЕЙ НА МОРФОЛОГИЮ ОБРАЗЦОВ С НАНО-η-TiO2 // Фундаментальные исследования. 2013. № 1-3. С. 784-788;URL: https://fundamental-research.ru/en/article/view?id=31029 (дата обращения: 28.04.2026).



