Сердечная недостаточность (СН) осложняет течение сердечно-сосудистых заболеваний у 2–3 % населения развитых стран; при выраженной ее степени летальность в течение пяти лет достигает 75 %. Расходы на лечение СН составляют 1–2 % бюджета здравоохранения стран Западной Европы и США. Проблема хирургического лечения терминальной СН занимает одну из ведущих научных позиций в современной кардиологии. Перспективным методом хирургического лечения критической СН является использование механических систем вспомогательного кровообращения (ВК), полностью или частично замещающих функцию пораженного сердца. Под понятием «системы вспомогательного кровообращения» следует понимать механические системы, производящие перемещение крови с целью снижения работы миокарда и/или увеличения его энергоснабжения [1]. Исходя из этого задачи системы ВК сводятся к следующему: снижение работы миокарда (за счет подключения системы ВК) и увеличение снабжения его и других органов кислородом (за счет улучшения коронарной и системной перфузии, т.е. системный кровоток складывается из суммы естественного выброса сердца и выброса насоса).
Одним из вариантов систем ВК, выполненным в соответствии с подходами, описанными в работах [2, 3] является система, построенная на базе электромеханического привода (ЭМП) и мембранного насоса крови – искусственного желудочка сердца (ИЖС). Для регулирования режимов работы привода используется система управления (СУ), требуемое энергопотребление обеспечивают источники питания (основной и резервный). При этом ЭМП с насосом крови имплантируется в брюшную полость, а СУ с источником питания крепятся на поясе пациента для обеспечения его мобильности на время применения системы ВК.
Имплантируемый ЭМП (рис. 1) выполнен на базе реверсивного вентильного двигателя (ВД) с возбуждением от постоянных магнитов. Статор двигателя содержит пакет зубцового якоря с размещенной в пазах диаметральной сосредоточенной трехфазной обмоткой якоря c целью преобразования вращательного движения ротора в возвратно-поступательное движение толкателя, вал ротора выполнен полым с таким расчетом, чтобы ротор составлял единую интегральную конструкцию с преобразователем вида движения [4].
Коммутация фаз обмотки якоря осуществляется трехфазным мостовым инвертором, силовые ключи которого управляются сигналами от чувствительных элементов датчиков положения ротора (ДПР). В качестве таких элементов в ЭМП использованы датчики Холла, установленные на лобовых частях обмотки якоря и управляемые потоком рассеяния индуктора.
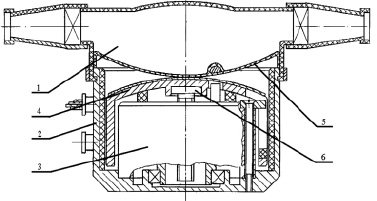
Рис. 1. Имплантируемый компонент системы ВК:1 – насос крови; 2 – корпус ЭМП; 3 – электродвигатель; 4 – толкатель;5 – мембрана насоса крови; 6 – винт РВМ
Напряжение питания к обмоткам якоря и элементам Холла подводится по кабелю, герметизированный ввод которого установлен на корпусе ЭМП. Для обеспечения циркуляции воздуха в герметичном рабочем объеме модуля кабель пропущен через тонкостенную трубку.
Преобразователь вида движения представляет собой роликовинтовой механизм (РВМ), состоящим из винта, резьбовых роликов и резьбовой гайки, запрессованной в полый вал ротора электродвигателя.
Рабочий конец винта через специальную муфту соединен с толкателем, воздействующим на мембрану насоса крови, жестко установленного на корпусе ЭМП. Применение РВМ в качестве преобразователя движения позволяет обеспечить требуемые передаточное отношение и плавность перемещения выходного звена, при высоком суммарном КПД, обеспечив минимальные осевые габариты модуля [5].
Выбор передаточного отношения РВМ рационально осуществлять по критерию минимума потребляемой мощности. Зависимость потребляемой мощности от шага РВМ при частоте перемещения мембраны f = 1 Гц, отношении времени выброса (систолы) к времени заполнения насоса крови (диастолы) β = tsys/tdia = 1/2 и ходом толкателя l = 20 мм представлена на рис. 2,а. Расчет проведен при непрерывном сигнале обратной связи с неизменным коэффициентом усиления регулятора. Из приведенных рисунков видно, что с увеличением шага РВМ с 1,125 до 3,7 среднеквадратичное значение потребляемой мощности за период сокращается более чем в 3 раза.
Составляющие мощности при шаге РВМ, равном 3,7 мм, затрачиваемой на разгон и торможение инерционной массы, а также преодоление толкателем кровяного давления представлены на рис. 2,б.
С увеличением угла подъема резьбы КПД РВМ увеличивается. Однако при этом происходит значительное уменьшение информации о реальном положении ротора, что может привести к росту пульсаций скорости и неустойчивой работе системы на малых частотах работы ЭМП. В связи с этим выбор шага РВМ необходимо производить с учетом дискретности сигнала обратной связи, а также величины коэффициента усиления. При этом должны выполняться требования по точности отработки задающего воздействия и пульсациям скорости.
а)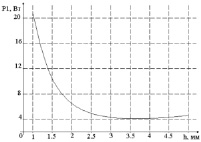 б)
б)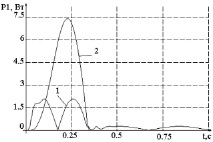
Рис. 2. Зависимость потребляемой мощности: а – от шага РВМ; б – от времени (шаг РВМ h = 3,7 мм): 1 – мощность, затрачиваемая на разгон-торможение инерционной массы ротора; 2 – мощность, затрачиваемая на преодоление толкателем давления крови
Точность отработки задающего воздействия в значительной степени зависит от количества информации о реальном положении ротора, поступающей с ДПР. Количество информации с ДПР задается углом поворота ротора, по прошествии которого подается очередной импульс сигнала обратной связи. Для повышения точности отработки задающего воздействия можно увеличить количество сигналов обратной связи путем увеличения числа ДПР или числа пар полюсов ВД; ввести систему коэффициентов усиления для различных режимов; использовать самонастраивающуюся систему; использовать иной принцип управления.
Наиболее рациональным решением является проектирование ВД с большим числом пар полюсов, при этом система управления двигателем и система обратной связи по положению мембраны насоса крови оказывается наиболее простой.
На основе приведенных выше рекомендаций была проведена серия расчетов ВД для создания макетного образца имплантируемой части системы ВК с целью проведения дальнейших экспериментальных исследований. При расчетах использована уточненная методика расчета ВД, в ее основе лежит классическая теория расчета электрических машин с постоянными магнитами [6]. Ее отличие от традиционных методик заключается в использовании при расчете магнитного поля аналитических решений полевых задач [6–8] и последующим решением системы дифференциальных уравнений, описывающих процессы в обмотке якоря на коммутационном интервале. Это позволяет более точно определять значения потока возбуждения и среднего и действующего значений тока, которые входят в выражения для определения момента, частоты вращения и потерь в обмотке.
В результате проведенных расчетов получены значения момента и частоты вращения, обеспечивающие требуемую номинальную мощность и позволившие реализовать требуемый закон выброса из камеры насоса крови.
Насос крови содержит корпус, мембрану, приводимую в движение толкателем ЭМП, два дисковых клапана типа «МИКС» с одинаковым проходным диаметром, и входной и выходной штуцера для присоединения канюль. Указанный насос крови спроектирован в соответствии с подходами, указанными в работе [9], и обладает требуемыми гемодинамическими характеристиками. Объединение решений, полученных в ходе проектирования ЭМП и насоса крови мембранного типа, позволило создать макетный образец имплантируемой части системы ВК (рис. 3) и приступить к ее экспериментальным исследованиям.

Рис. 3. Макетный образец имплантируемой части системы ВК: 1 – насос крови; 2 – корпус ЭМП; 3 – кабель подвода питания
Основные характеристики системы ВК:
1. Номинальная частота вращения n = 4200 мин–1;
2. номинальная мощность Р1 = 30 Вт;
3. напряжение питания U = 12 В;
4. Число пар полюсов электродвигателя р = 6;
5. Ход толкателя l = 20 мм;
6. Частота колебаний мембраны f = 1–2 Гц;
7. Соотношение «время систолы/время диастолы» β = 1/1, β = 1/2, β = 1/3;
8. Объем выброса 60 мл.
Экспериментальные исследования проводились в два этапа и включали стендовые испытания на установках, описанных в работе [10], и медико-биологические испытания. Стенд для гидродинамических испытаний макетного образца системы ВК (рис. 4,а) содержит два резервуара, один из которых заполняется дистиллированной водой (либо водно-глицериновым раствором), другой создает вакуум с целью обеспечения начального противодавления. Для визуального контроля процесса стенд выполнен из прозрачного материала (оргстекла). В состав стенда входят входная и выходная магистрали, длина и диаметр которых идентичны тем, которые применяются при шунтировании естественного сердца. Уменьшение или увеличение величины противодавления осуществляется за счет уменьшения или увеличения гидравлического сопротивления соответственно. Кроме того, стенд оснащен оборудованием для сбора и обработки данных.
а)  б)
б)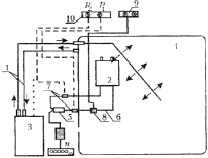
Рис. 4. Стендовые испытания макетного образца системы ВК: а – гидродинамические; 1 – блок насос-двигатель; 2 – источник питания; 3 – ЭВМ; 4 – гидродинамический стенд; б – гемолитические; 1 – резервуар подогрева; 2 – гепаринизированная кровь; 3 – нагреватель; 4, 6 – трубки; 5 – насос; 7, 10 – датчик; 8 – расходомер; 9 – регистратор
В ходе проведенных гидродинамических испытаний установлено, что исследуемая система ВК обеспечивает производительность 9 л/мин при противодавлении 120 мм рт. ст. и соотношении времен систола/диастола β = 1/3 [2]. Следующим этапом стендовых испытаний являлась оценка уровня гемолиза на гемолитическом стенде (рис. 4,б). Эксперименты подтвердили низкий уровень гемолиза и показателя нормализованного уровня гемолиза (NIH = 0,08 г/100 л), что свидетельствует об отсутствии заметного травмирующего влияния насоса на форменные элементы крови.
После проведения успешных стендовых испытаний системы и анализа полученных при этом данных были проведены медико-биологические испытания разработанной имплантируемой системы ВК.
Было выполнено 16 медико-биологических экспериментов на телятах черно-пестрой породы. Все эксперименты проводились в одной и той же операционной.
В процессе операции использовалась аппаратура для проведения электрокоагуляции в операционной ране, отсосы крови и т.д. При необходимости применялась аппаратура для проведения искусственного кровообращения аппаратом Штоккерт и мембранной оксигенацией крови. Через герметичную дверь операционная была связана с послеоперационным залом, куда животное переводилось после окончания операции и стабилизации параметров гемодинамики.
Система ВК имплантировалась по схемам «левый желудочек-аорта», «левое предсердие-аорта». Во всех случаях хирургическая методика подключения системы ВК была успешно завершена, и животное на фоне стабильных показателей гемодинамики при работающем насосе переводилося в стационарную клетку-станок, которая находилась в послеоперационном зале. Результаты применения имплантируемых систем ВК представлены в таблице.
Результаты применения имплантируемой системы ВК
|
Позиция имплантации насоса |
Суммарная длительность обхода, час |
Примечания |
|
Наружная ЛП – А |
39 |
ЛП – левое предсердие; А – аорта; ЛЖ – левый желудочек |
|
Наружная ЛЖ – А |
119 |
|
|
Интраабдоминально ЛЖ – А |
1059 |
Наиболее частым осложнением, явившимся основной причиной смерти животных и прекращения эксперимента (рис. 5), являлась дыхательная недостаточность, которая отмечалась в 4 случаях или в 20 % экспериментов, что связано с особенностями легких телят, которые очень чувствительны к наружному сдавливанию, а также проведению искусственной вентиляции легких, в том числе и во вспомогательном режиме [11].
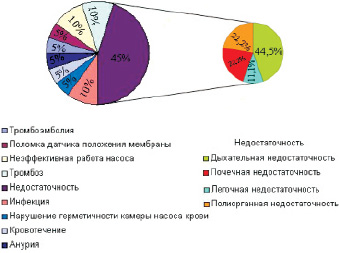
Рис. 5. Причины прекращения эксперимента при применении имплантируемой системы ВК
С ростом длительности работы системы в организме повышается число инфекционных осложнений. Во всех случаях отмечалась адекватная реакция организма на инфекцию, что проявлялось высоким лейкоцитозом со сдвигом формулы влево, повышением реакции оседания эритроцитов и т.д. Все три животных, прожившие на обходе более 100 часов, погибли от инфекции, причем во всех случаях входящими воротами инфекции являлись соединительные кабели, связывающие электродатчики с электрическими батареями, т.к. в этих местах имелись местные проявления инфекции. Этот факт свидетельствует о необходимости использования чрескожных методов передачи энергии, исключающих применение наружных электрических кабелей для подведения энергии от наружных электрических батарей к электродвигателю.
Осложнения, связанные с техническими дефектами, отмечались только на начальной стадии работы, и в последних 12 экспериментах, в том числе длительных, зафиксированы не были.
Работа выполнена в рамках государственного контракта ГК № 16.522.11.2007. от 6.04.2012.
Рецензенты:
Гоц А.Н., д.т.н., профессор кафедры тепловых двигателей и энергетических установок ФГБОУ ВПО «Владимирский государственный университет имени Александра Григорьевича и Николая Григорьевича Столетовых», г. Владимир;
Кульчицкий А.Р., д.т.н., профессор, заместитель главного конструктора по испытаниям ООО «ВМТЗ», г. Владимир.
Работа поступила в редакцию 28.11.2012.



