Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
OXIDATION – REDUCTION REACTIONS AT THE SYNTHESIS OF SILICATE CHARGE IN AN ELECTRIC ARC FURNACE
При синтезе камнелитых материалов важнейшим аспектом, определяющим качество отливок, является кристаллизационная способность расплава и процессы, происходящие в расплаве при его выплавке. Исследователями отмечается, что помимо состава и свойств самой шихты на кристаллизационную способность положительно влияет восстановительная атмосфера плавки. Как правило, она обеспечивается использованием дуговых плавильных агрегатов с графитовым электродом и подиной. Однако физико-химические процессы, происходящие в расплаве при плавлении шихты в таких агрегатах и роль окислительно-восстановительных реакций с участием углерода электрода, до настоящего времени не были полностью изучены.
Материалы и методы исследования
Настоящая работа преследует цель сформулировать реакции и физико-химические процессы, происходящие в шихте необходимые для получения камнелитых материалов, начиная с момента нагрева и до полного расплавления в электродуговых печах с графитовым электродом.
Объектом исследования является силикатная шихта, состоящая из горнблендита (90 %), хромовой руды (4 %), плавикового шпата (3 %) и кварцевого песка (3 %), содержащая оксиды SiO2, TiO2, Al2O3, FeO + Fe2O3, MnO, MgO, CaO, K2O + Na2O, Cr2O3, в большей степени перечисленные компоненты являются тугоплавкими, кроме того, содержатся примеси соединений серы и фосфора в незначительном количестве.
Результаты исследования
и их обсуждение
В твердом состоянии шихта не является электропроводной, поэтому для начала процесса плавления в электродуговой печи расплавляется небольшое количество предварительно увлажненной шихты. Образующееся небольшое количество расплава в свою очередь является уже электропроводным, и оно используется как затравочное, то есть постепенно к нему добавляют твердую шихту, и объем расплава доводится до требуемого.
В процессе плавки и варки расплава электрод погружен в расплав. В зоне контакта электрода и расплава температура достигает максимальных значений и именно в этой зоне концентрируется основная часть процессов взаимодействия углерода и расплава.
При температуре 1000–1250 °С расплав находится в вязко-подвижном состоянии, с повышением температуры возрастает жидкотекучесть, снижается вязкость, в полной мере в состояние расплава шихта переходит при температуре 1300–1700 °С, в данном температурном интервале и протекает основная часть восстановительных и окислительных процессов при плавке.
По ранее проанализированным данным термического анализа установлено, что [3] до момента образования жидкого расплава протекает ряд твердотельных реакций при температурах 635, 833, 1113 и 1210 °С.
При температуре 635 °С разлагается диаспор (AlOOH), который как примесь присутствует в горнблендите:
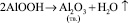 . (1)
. (1)
При температуре 833 °С происходит термическое разложение актинолита и его частичное взаимодействие с графитом электрода:
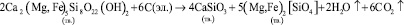 . (2)
. (2)
При температуре 1113°С происходит расплавление роговой обманки
((Na, K)0-1[(Ca, Fe2 + , Mn, Mg)2-1.34Na0-0,66] (Mg, Fe2 + , Mn, Al, Fe3 + , Ti)5 [Si7,5-5,3Al0,5-2,7] (O, OH)22(OH, F, Cl, O)2), входящей в состав горнблендита.
При температуре 1210 °С образуется расплав, представляющий собой смесь молекул оксидов, а также свободных ионов кислорода, металлов и неметаллов. В результате реакций, предшествующих расплавлению, из шихты удаляются все гидроксосоединения, а также выгорает большая часть примесей.
Основным компонентом расплава является диоксид кремния, причем кремнекислородные тетраэдры в расплаве имеют тенденцию к разной форме соединения, характерной для силикатов. Поэтому характер протекающих реакций может быть
различен:
SiO2 ж + 3Cэл = SiCтв + 2CO ↑, (3)
SiO2 ж + 2Cэл = Siмет + 2CO ↑, (4)
SiO2 ж + Cэл = SiOж + CO ↑. (5)
В результате представленных реакций вокруг электрода образуется область высокой концентрации СО, учитывая вязкость расплава, это приводит к тому, что в зоне около электрода возникает «вспененный» слой. С этого момента можно рассматривать расплав уже не как однородный, а зонированный материал.
Указанные выше реакции не являются конечными, оксид углерода взаимодействует с электродом и образуется вторичный оксид углерода:
CO2 ↑+ Cэл = 2CO ↑. (6)
Наличие вторичного оксида углерода предполагает постоянную и высокую концентрацию газа в верхних слоях расплава, что является фактором, поддерживающим зонированность расплава. Однако насыщение углекислым газом происходит и в нижнем слое расплава, а в присутствии углекислого газа оксид хрома, марганца и алюминия диссоциируют значительно быстрее [4], в процесс восстановления включается кислород и вторичные продукты реакций.
Рассмотрим поведение основных компонентов расплава.
Тугоплавкий оксид хрома взаимодействует с углеродом и образует небольшое количество свободного хрома и углекислый газ, практически сразу хром взаимодействует с кислородом (свободных ионов кислорода достаточно много, так как они освобождаются при диссоциации диоксида кремния) и переходит уже во вторичный оксид хрома или сразу же взаимодействует с углеродом, образуя карбид хрома. Карбид хрома взаимодействует с кислородом, образуя вновь оксид хрома (тоже вторичный) и оксид углерода, затем уже вторичный оксид хрома взаимодействует с оксидом железа (который присутствует в расплаве как продукт разложения магнетита), в результате образуется минералоподобные соединение – хромит. Разумеется, такое взаимодействие возможно при условии высоких температур и достаточной концентрации углекислого газа.
Cr2O3 тв + Cэл = 2Crтв + CO ↑, (7)
7Cr2O3 тв + 27Cэл = 2 Cr7C3 тв + 2CO ↑, (8)
Сr2O3 тв + FeOж = FeCr2O4 тв. (9)
В остальной массе расплава (средняя зона) более высокая концентрация ионов кислорода, она значительно выше, чем концентрация углекислого газ в верхних слоях расплава, а также присутствует оксид кальция, а потому имеет место быть реакция, при которой образуется хроматит:
2Cr2O3 тв + 4CaOж + 3O2↑ = 4CaCrO4, (10)
который также может разлагаться и образовывать вторичные оксиды кальция хрома, а вот уже вторичный оксид кальция вероятно образует волластонит:
CaOж + SiO2 ж = CaSiO3 тв (11)
Другой тугоплавкий компанент шихты – оксид титана. При взаимодействии с углеродом образуется новый оксид титана и углекислый газ, новый оксид титана взаимодействует с карбидом кремния, образуя вторичный диоксид кремния и опять же новый оксид титана. В итоге привзаимодействии уже со вторичным диоксидом кремния, образуется переходный оксид титана и монооксид кремния разумеется, монооксид нестабилен и, скорее всего, в результате других реакций он входит в состав других минеральных образований, как и переходный оксид титана. Ценно то, что данные оксиды не образуются в природе, а значит, физико-химические процессы при плавлении каменного литья хоть и похожи на магматические, но в целом имеют ряд весьма значимых отличий.
4TiO2 тв + Cэл = Ti4O7 тв + CO ↑, (12)
6Ti4O7 тв + SiCтв =
= 8Ti3O5 тв + SiOж + CO ↑, (13)
4Ti3O5 тв + SiO2 ж =
= 3Ti4O7 тв + SiO ↑(белая дымка). (14)
Достаточно активно себя в расплаве ведет оксид кальция, он взаимодействует практически со всеми основными компонентами расплава, образуя комплексные соединения, которые являются будущими составляющими компонентами минеральных фаз каменного литья, например, пироксена. В частности, в результате взаимодействия с оксидом титана образуется перовскит.
CaOж + TiO2 тв = (CaTi)O3 тв (15)
CaO ж + Al2O3 тв = Ca[Al2O4]тв (16)
CaOж + Fe2O3 тв = Ca[Fe2O4]тв (17)
Определенный интерес представляет поведение оксида алюминия, пожалуй единственная реакция, в которой данный компонент участвует, ‒ это как раз взаимодействие с оксидом кальция. Поскольку в остальных случаях оксид алюминия диссоциирует, освобожденные ионы кислорода взаимодействуют с другими свободными ионами в расплава, образуя вторичные оксиды и минеральные составляющие, а ионы алюминия изоморфно замещают ионы кремния.
Среди всех физико-химических процессов, сопутствующих плавлению шихты, для получения каменного литья следует выделить также поведение оксидов магния и марганца. Концентрация оксида магния в шихте, как правило, выше, чем оксида марганца, поэтому рассмотрим процессы, связанные с ним. При взаимодействии с углеродом электрода происходит восстановление с выделением углекислого газа. Затем восстановленный магний частично окисляется вторично, а частично вступает в реакцию с карбидом кремния, образуя силицид и карбид магния. В свою очередь карбид магния в условиях высоких температур разлагается, образуя магний и углерод, а силицид магния, взаимодействуя с волластонитом, образует диопсид. Однако это не все процессы, в которых участвует оксид магния, ‒ помимо диопсида на его основе образуются более сложные минералоподобные соединения, например, при взаимодействии с оксидами марганца или железа (пироксены, в частности, оливин).
MgOж + Cэл = Mgж + CO ↑, (18)
4Mgж + 2(SiC)тв = 2Mg2Siж + MgC2 тв, (19)
MgC2тв → Mg2C3 тв → Mgж + Cтв, (20)
Mg2Siж + 2CaSiO3 ж = 2CaMg(Si2O6)тв, (21)
Mg2Siж + 2MnOж + 3SiO2ж + 2O2 ↑ = 2MnMgSi2O6 тв, (22)
Mg2Siж + Fe2O3 тв + O2 ↑ = (Mg, Fe)2[SiO4]тв. (23)
Определенная двойственность поведения в процессе плавки свойственна и оксидам калия и натрия. Данный тип оксидов активно разрушает связи между кремнекислородными тетраэдрами в процессе плавления, но при этом сами они представляют собой достаточно устойчивые соединения, при термическом разложении сразу же образуются вторичные оксиды, но некоторые ионы калия и натрия, вынесенные на поверхность, образуют пероксид, которые в свою очередь могут взаимодействовать с карбидами кремния и насыщать «вспененный» слой минералоподобными соединениями:
2Naж + O2 ↑ = Na2O2 ж, (24)
SiCтв + 4Na2O2 ж = Na2SiO3 тв + Na2CO3 ж + 2Na2Oж. (25)
Указанные реакции, в которых не участвует углекислый газ, протекают в так называемом нижнем слое расплава, то есть под шапкой «вспененного» слоя.
Однако зонирование расплава не ограничивается этими двумя зонами в основном слое, помимо описанных процессов также происходят реакции с участием оксидов железа, их следует рассматривать отдельно, так как в результате таких реакций образуются нехарактерные продукты.
Огненно-жидкий расплав ‒ весьма агрессивная среда, а условия прохождения то-
ка ‒ агрессивные условия эксплуатации. Поэтому на определенном этапе плавки (примерно через 10‒15 мин после достижения максимальной температуры) графитовый электрод начинает постепенно разрушаться, чешуйки графита отслаиваются от его поверхности и попадают в расплав. Часть твердого свободного графита участвует во вторичном окислении углекислым газом, тем самым активизирует диссоциацию, а часть взаимодействует с компонентами расплава и в значительной степени с оксидами железа. Поскольку в расплаве присутствует сразу два типа оксидов, так как их источником в расплаве является магнетит, во взаимодействии участвуют как первичные оксиды, так и вторичные, являющиеся продуктами диссоциации первичных. Кроме того, часть твердого углерода активно взаимодействует и с ионами кремния, которых достаточно много, как уже отмечалось, причина тому ‒ нарушение кислородных связей в расплаве.
Возникают следующие процессы:
Fe2O3 тв + 3Cтв + O2 ↑ = 2FeOтв + 3CO ↑, (26)
FeOтв + 3Cтв + O2 ↑ = Feмет + 3CO ↑, (27)
SiO2 ж + 4Cтв + O2↑ = Siмет + 4CO ↑. (28)
Образуются капли расплава железа и кремния. Это является радикальным поворотом во всем процессе плавки, поскольку с этого момента в расплаве начинает формироваться третья зона, которая затем становится отдельной жидкой фазой. Однако рассмотрим процесс
подробно.
Из теории Флемингса известно [5], что мелкодисперсные капли одной жидкой фазы в другой стремятся к консолидации. Однако Флемингс рассматривал данную теорию применительно к неметаллическим включениям в металлическом расплаве, а рассматриваемый случай ‒ яркий пример ситуации обратной.
Итак, капли жидкого железа и кремния начинают стремится к консолидации между собой. В небольших обособленных скоплениях этих жидких капель протекает реакция, в результате которой образуется ферросилиций:
Feж + Siж = FeSiж. (29)
Капли образованного ферросилиция в значительной степени отличаются от камнелитого расплава по плотности, поэтому они погружаются и концентрируются на дне плавильного пространства, образуя там отдельный жидкий слой, имеющий четкие границы.
Продукты реакций не являются конечными, в дальнейшем, при снижении температуры следуют другие физико-химические процессы, отличающиеся от тех, что протекали при плавлении, однако они являются отдельным предметом изучения. Следует отметить, что при затвердевании образуются в основном 3–4 минеральные фазы сложного состава и степени упорядоченности (таблица).
Соотношение минеральных компонентов
в различных частях расплава после затвердевания
|
Слой расплава |
Состав |
|
«Вспененный» верхний слой |
Кварц (SiO2) – 98 % и примеси |
|
Средний слой |
Пироксен (Ca, Fe, Mg)2Si2O6 – 80 % Анортит (CaAl2Si2O8) – 9 %, Кварц (SiO2) – 8 %, Хромшпинелид (Fе, Мg) (Сr, Аl, Fе)2О4) – 3 % |
|
«Подовой» нижний металлический слой |
Fe – 4,5 %; Si – 90 %; Al – 3,5 %; Mn – 2 % |
Выводы
Таким образом, рассмотренные физико-химические процесс достаточно полно характеризуют начальную стадию процесса плавления камнелитых расплавов.
В расплаве можно выделить уже три характерные зоны (рисунок):
– «вспененный» верхний слой;
– средний слой;
– «подовой» нижний металлический слой.
Вспененный слой может использоваться для изготовления пеностекла и подобного ему пористого материала, средний слой ‒ для изготовления непосредственно каменного литья, а подовой является готовым продуктом для получения фер-
росплава.
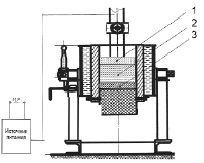
Схема строения расплава в плавильной печи:
1 – «вспененный» верхний слой;
2 – средний слой; 3 – «подовой» нижний металлический слой
Для процесса получения расплава каменного литья характерно образование большого числа вторичных соединений, этот механизм является ключевым в понимании физико-химических процессов при плавлении каменного литья. Именно благодаря их присутствию возникают условия для образования сложных минеральных фаз и объединения их в единый синтетический материал.
Рецензенты:
Беленький В.Я., д.т.н., профессор, зам. директора Западно-Уральского аттестационного центра, г. Пермь;
Кривоносова Е.А., д.т.н., профессор, ведущий специалист, Западно-Уральский аттестационный центр, г. Пермь.
Работа поступила в редакцию 26.10.2012.
Библиографическая ссылка
Игнатова А.М. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ ПРИ СИНТЕЗЕ СИЛИКАТНЫХ ШИХТ В ЭЛЕКТРОДУГОВЫХ ПЕЧАХ // Фундаментальные исследования. 2012. № 11-3. С. 604-608;URL: https://fundamental-research.ru/en/article/view?id=30581 (дата обращения: 13.05.2026).



