Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
EXTRAHEPATIC MANIFESTATIONS OF CHRONIC HEPATITIS C (A REVIEW)
HCV-инфекция относится к индикаторам социального и медицинского благополучия общества [7]. Вирусом гепатита С инфицировано около 3% (180 000 000 человек) населения Земли [39], что по масштабу в 5 раз превосходит расспространенность ВИЧ [40].
Гепатит С относится к инфекциям с неконтролируемыми путями передачи и распространяется среди людей почти исключительно путем абиогенной («кровяной») трансмиссии. Заражение HCV в 50-80% случаев ведет к персистенции вируса и развитию хронического гепатита, а также цирроза (20-30%) и гепатоцеллюлярной карциномы (1-4%) [22]. На долю HCV приходится около 40% всех случаев хронического гепатита. В большинстве это молодые люди в возрасте 15-29 лет [7].
Концепция системных поражений при хроническом вирусном гепатите С впервые была сформулирована Апросиной З.Г. [1]. Дальнейшие исследования [12, 25] показали, что при прогрессировании заболевания нередко развиваются внепеченочные осложнения, которые могут протекать как клинически латентно, так и в виде ярких клинических синдромов или самостоятельных заболеваний. Частота их, по результатам исследований больших групп больных, составляет в странах Европы 40-74% [12] и в Северной Америке - 38% [25], что превышает частоту внепеченочных осложнений при вирусном гепатите B (10-20%) [19, 24, 32].
Развитие внепеченочных осложнений происходит не у всех пациентов и определяется комплексом из трех факторов:
1. Длительная персистенция вируса (6-20 лет), что, как полагают, может быть связана с его высокой изменчивостью. Одной из ее возможных причин является высокая изменчивость последнего, так как генетический материал HCV представлен молекулой РНК, для которой в клетке не существует систем репарации [4, 22].
2. Стимуляция CD5+ В-лимфоцитов. Вирус связывается с В-лимфоцитами с помощью гликопротеина Е2 (входит в состав липидной оболочки HCV), который взаимодействует с СD81-рецепторами на поверхности В-лимфоцитов [26, 41]. CD81 экспрессируется практически на всех ядерных клетках и образует различные комплексы со многими поверхностными молекулами, такими как CD19, CD21, HLA-DR на В-лимфоцитах и с CD4, CD8 и СD82 на Т-лимфоцитах. На B-лимфоцитах CD81, как и другие члены этого суперсемейства рецепторов, является необходимым компонентом специфической сети, учавствующей в межклеточной сигнализации, антигенной презентации и клеточной адгезии [33]. Связывание HCV с CD81 на B-лимфоцитах в составе комплекса CD81/CD19/CD21, что понижает активационный порог, что вызывает клональную пролиферацию и продукцию различных аутоантител [37]. Направленная стимуляция В-клеток к клональной пролиферации и продукции аутоантител описана для вируса Epstein Barr [30], который активирует В-клетки, связываясь с CD21. Не исключено, что и HCV проводит активационный сигнал через тот же комплекс [9].
У части больных длительная пролиферация В-лимфоцитов с накоплением генетических мутаций при определенных средовых факторах может привести к развитию злокачественной В-клеточной пролиферации [9, 16, 42].
3. Прямое цитопатическое действие на другие органы и ткани. Доказана возможность репликации HCV в некоторых тканях нелимфоидного происхождения (эпителий слизистой оболочки рта и слюнных желез) [14, 20, 38].
Сообразно доказанности этиологической роли HCV в развитии многообразных ассоциированных осложнений [2, 10, 12, 25, 31, 36] они разделены на 3 группы [4]:
- Заболевания, при которых доказана роль HCV как основного этиологического фактора (смешанная криоглобулинемия).
- Заболевания, при которых НСV является одним из этиологических факторов (узелковый полиартериит, В-клеточная неходжкинская лимфома, иммунная тромбоцитопения, синдром Шегрена, поздняя кожная порфирия, красный плоский лишай и др.).
- Заболевания, при которых роль НСV как одного из этиологических факторов вероятна, но требует дополнительных доказательств (гигантоклеточный височный артериит, фиброзирующий альвеолит, полимиозит, миокардит, дерматомиозит и др.).
Смешанная криоглобулинемия характеризуется наличием специфических иммуноглобулинов, которые обратимо осаждаются (преципитируют) в сосудах при температуре ниже 37°С, образуя криопреципитаты [23]. Криоглобулинемия классифицируется по компонентам криопреципитата (рис. 1): I тип - в состав криопреципитата входят моноклональные иммуноглобулины только одного класса (наиболее часто - моноклональные IgM, редко - IgG и еще реже - IgA); II и III типы - криоглобулины состоят из иммуноглобулинов разных классов (II - поликлонального IgG и моноклонального IgM, III - поликлонального IgG и моноклонального IgM). При этом поликлональный IgG в обоих типах является антигеном, а IgM - антителом против Fc-фрагмента IgG [6].
Криоглобулинемию II и III типа обозначают как смешанную криоглобулинемию. Основную роль в ее развитии играет вирус гепатита С [5]. У большинства больных смешанной криоглобулинемией выявляется маркер репликации вируса гепатита - HCV РНК в сыворотке крови (70-86%) и в криопреципитатах (93-99%), причем концентрация HCV РНК в криопреципитатах в десятки тысяч раз превосходит таковую в сыворотке [8]. При других заболеваниях смешанная криоглобулинемия встречается значительно реже, например при ревматических болезнях - 6,4% [5].
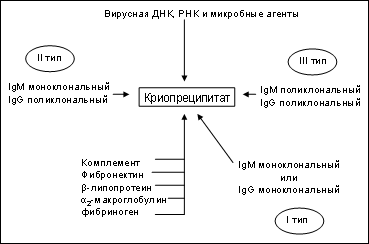
Рис. 1. Классификация криоглобулинов по J.Brouet [11] и состав криопреципитата
Факторами, способствующими образованию криопреципитатов являются: охлаждение, повышенное гидростатическое давление, а также стаз крови [35]. Криопреципитаты формируются in situ через фиксацию HCV на эндотелии с присоединением циркулирующих иммуноглобулинов. Развитие иммунного воспаления происходит в результате активации комплемента и привлечения лейкоцитов [6]. Клинически это проявляется различными формами поражения микрососудов (геморрагическая пурпура, синдром Рейно, периферическая полиневропатия, гломерулонефрит, легочный васкулит и т.д.).
Геморрагическая пурпура (67- 99%) - воспалительные пятна, до 5 мм в диаметре, (описать как в коже), локализующаяся преимущественно на коже нижних конечностях и нижней половины живота, с тенденцией к изъязвлению. Такие же кожные элементы могут появляться на других легко охлаждаемых участках тела: нос, уши. Отмечаются и другие кожные изменения - ретикулярное ливедо, уртикарная сыпь [6].
Летучие артралгии (40-56%) - мигрирующие суставные боли, провоцируемые переохлаждением, при отсутствии рентгенологических изменений в структуре сустава даже после повторных атак [6]. Наблюдается преимущественное поражение суставов кистей и стоп.
Синдром Рейно (25-50%) - проявляется приступообразными спазмами в периферийных частях тела - чаще всего кистей рук [6].
Периферинеская полиневропатия (20-56%) - симметричное, сенсорной, сенсорно-моторной. Проявляется парестезиями, онемением и двигательными нарушениями нижних конечностях и/или множественных мононевритов [6]. Механизм невропатии при смешанной криоглобулинемии связывают с развитием эпиневрального васкулита (поражение vasa nervorum) и нарушением микроциркуляции из-за интраваскулярного отложения криоглобуинов, что ведет к ишемии, дегенерации аксонов и демиелинизации. Отмечается корреляция между клиническими проявлениями и степенью поражения vasa nervorum. Некротизирующий васкулит ассоциируется с наиболее тяжелыми формами полинейропатии. При смешанной криоглобулинемии могут встречаться и другие поражения нервной системы в виде энцефалопатию или зрительную невропатию, однако среди неврологических симптомов криоглобулинемия ведущее место занимает периферическая невропатия.
Криоглобулинемический гломерулонефрит (20-30%) - характеризует поздние стадии заболевания, морфологически - мезангиокапиллярный гломерулонефрит. В 50% случаев проявляется умеренно выраженная протеинурия, 25% - тяжелый острый нефритический синдром и 25% - нефротический синдром. Для всех вариантов характерна тяжелая артериальная гипертензия [15]. Исход: ХПН в 30 % случаев [6].
Также могут наблюдаться легочные васкулиты (0,7-12%). Считается, что нет органа или системы, которые не могли бы быть вовлечены в патологический процесс при смешанной криоглобулинемии.
Осложнения с участием HCV в качестве одного из этиологических факторов - насчитывается около десятка заболеваний в развитии которых принимает участие HCV.
Узелковый полиартериит (12%) - показано, что HCV-инфекция выявляется у 5-12% больных узелковым полиартериитом и является одним из этиологических факторов этого васкулита, основную роль в этиологии которого, как известно, играет HBV [13, 34]. Узелковый полиартериит - второй по частоте системный васкулит, встречающийся при HCV-инфекции. Нередко наблюдается сочетание узелкового полиартериита и криоглобулинемическим васкулитом [4].
В-клеточная неходжкинская лимфома (13%) - обобщение большого числа эпидемиологических исследований показало, что частота HCV-инфекции среди больных В-клеточной неходжкинской лимфомой (в среднем около 13%) превышает среднюю частоту HCV-инфекции в популяции (около 1,5%) и среди больных другими формами лимфопролиферативных заболеваний (около 3%) [4, 17, 18, 38]. Считают, что риск развития В-клеточной лимфомы у больных смешанной криоглобулинемией составляет до 10% [25].
Иммунная тромбоцитопения - наиболее частое поражение системы крови, наблюдающееся при HCV-инфекции. В отсутствие гиперспленизма и сниженной продукции тромбопоэтина основными ее механизмами являются аутоиммунный (связанный с продукцией антитромбоцитарных аутоантител) и непосредственный ингибирующий эффект вируса, реплицирующегося в клетках-предшественниках гемопоэза, на продукцию тромбоцитов в костном мозге [4, 28, 29]. В пользу наличия аутоиммунного механизма тромбоцитопении свидетельствуют также развитие тяжелой тромбоцитопении вследствие терапии ИФН-α и положительный эффект терапии кортикостероидами [4].
Синдром Шегрена - высокая частота заболевания при HCV инфекции связана с доказанным тропизмом вируса к слюнным железам [4, 25, 36, 38].
Развитие внепеченочных осложнений влияет на тактику лечения и эффективность противовирусной терапии HCV-инфекции. Оно преследует две цели:
1) элиминацию вируса, что достигается с помощью этиотропного лечения;
2) подавление продукции аутоантител, образования и отложения в сосудах иммунных комплексов, а также уменьшение воспалительной реакции с помощью иммуносупрессивной терапии, плазмафереза. Современная противовирусная терапия интерфероном-γ, обладающая иммуностимулирующими эффектами, способна вызвать усугубление внепеченочных осложнений. С другой стороны, патогенетическая терапия, эффективная при активных формах васкулитов и аутоиммунных синдромах, способствует репликации вируса. С учетом разнонаправленности действия обоих видов терапии в отношении вирусной инфекции одновременное их назначение оказывается малоэффективным [21, 31]. Трудности лечения обосновывают тактику возможно более раннего лечения гепатита, еще до развития внепеченочных осложнений. Бессимптомную криоглобулинемию у больных хроническим гепатитом С следует рассматривать как предвестник тяжелых внепеченочных поражений [3].
СПИСОК ЛИТЕРАТУРЫ:
- Апросина З.Г. // М.: Медицина, 1981. - 190 c.
- Игнатова Т.М., Апросина З.Г., Серов В.В. // Росс. мед. журнал. - 2001. - T.2. - С. 13 - 18.
- Игнатова Т.М. // Врач. - 2005. - № 7. - С. 34 - 37.
- Игнатова Т.М. // Сучасна гастроентерологія. - 2006. - Т.3. №27. С. 20 - 29.
- Козловская Л.В., Горловская Н.Б., Малышко Е.Ю., и соавт. // Рос. мед. журнал. - 2003. - Т.4. - С. 11 - 15.
- Козловская Л.В., Милованова С.Ю., Тэгай С.В. // Гепатологически форум. - 2005. - Т.3. - С. 2 - 7.
- Маянский А.Н. и др. Вирусный гепатит С. / Методич. рекоменд. - Нижний Новгород, 2007. - 35 с.
- Мухин, Н.А., Козловская Л.В., Малышко Е.Ю. // Тер. Архив. - 2000. - №6. - С. 1 - 5.
- Оленина Л.В., Соболев Б.Н. // Вирусные гепатиты. - 1999. - №1. - С. 11 - 7.
- Agnello V., De Rosa F.G. // J Hepatol. - 2004. V. 40. - №2. - P. 341 - 52.
- Brouet J.C. et al. // Am J Med. - 1974. - V. 57. - №5. - P. 775 - 88.
- Cacoub P. et al. // Arthritis Rheum. - 1999. - V. 42. - №10. - P. 2204 - 12.
- Cacoub P. et al. // J Rheumatol. - 2005. - V. 32. - №11. - P. 2078 - 82.
- Carrozzo M. // Oral Dis. - 2008. - V. 14. - №3. - P. 217 - 28.
- D´Amico G. // Kidney Int. - 1998. - V. 54. - №2. - P. 650 - 71.
- Ferri C. et al. // Clin Exp Rheumatol. - 2003. - V. 21. - №(6 Suppl 32). - P. S78 - 84.
- Gisbert J.P. et al. // Gastroenterology. - 2003. V. 125. N - 6. P. 1723-32.
- Gisbert J.P. et al. // Eur J Gastroenterol Hepatol. - 2004. - V. 16. - №2. - P. 135 - 8.
- Hollinger F.B., Liang T.J. In Fields Virology, Knipe D.M., Editor. 2001, Lippincott Williams & Wilkins: Philadelphia. P. 2971-3036.
- Isaguliants M.G. // Curr Pharm Biotechnol. - 2003. V. 4. N - 3. P. 169-83.
- Kim J.D., Sherker A.H. // Gastroenterol Clin North Am. - 2004. V. 33. N - 3. P. 693-708.
- Lamps L.W., Washington K. In Surgical athology of the Gl tract, Liver, Billiary tract and Pancreas, Odze R.D., Goldblum J.R., Crawford J.M., Editors. 2004, W.B. Saunders Company: Philadelphia.P. 783-840.
- Lospalluto J. et al. // Am J Med. - 1962. V. 32. P. 142-7.
- Machoney F.J., Kane M. In Vaccines, Plotkin S.A., Orenstein W.A, Editors. 1999, W.B. Saunders Company: Philadelphia. P. 158-182.
- Mayo M.J. // Am J Med Sci. - 2003. V. 325. N - 3. P. 135-48.
- Nattermann J. et al. // J Viral Hepat. - 2004. V. 11. N - 6. P. 519-26.
- Negri E. et al. // Int J Cancer. - 2004. V. 111. N - 1. P. 1-8.
- Panzer S., Seel E. // Wien Med Wochenschr. - 2003. V. 153. N - 19-20. P. 417-20.
- Panzer S. et al. // Eur J Haematol. - 2006. V. 77. N - 6. P. 513-7.
- Pileri P. et al. // Science. - 1998. V. 282. N - 5390. P. 938-41.
- Ramos-Casals M. et al. // Rheumatology (Oxford). - 2003. V. 42. №7. P. 818-28.
- Robinson W.S. In Principles and Practice of Infectious Diseases Mandell G.L., Bennett J.E., and Dolin. R., Editors. 1995, Churchill Livingstone: New York. P. 1406-1439.
- Rubinstein E. et al. // Eur J Immunol. - 1996. V. 26. N - 11. P. 2657-65.
- Sabry A.A. et al. // Nephrol Dial Transplant. - 2002. V. 17. №11. P. 1924-30.
- Sansonno D., Dammacco F. // Lancet Infect Dis. - 2005. V. 5. №4. P. 227-36.
- Sene D., Limal N., Cacoub P. // Metab Brain Dis. - 2004. - V. 19. №3-4. - P.357-81.
- Theise N.D., Bodenheimer H.C., Ferrell L.D. In MacSween´s Pathology of the Liver, Burt A.D., Portmann B.C., Ferrell. L.D., Editors. 2007, Elseiver Science. P. 399-441.
- Toussirot E. et al. // J Rheumatol. - 2002. - V. 29. - №11. - P. 2382 - 5.
- WHO. Hepatitis C. 1997 [cited; Available from: http://www.who.int/inf-fs/en/fact164.html.
- WHO. AIDS and Sexually Transmitted Diseases. 2004 [cited; Available from: http://www.emro.who.int/asd/events-wac-2004-statistics.htm.
- Yamada E. et al. // J Gen Virol. - 2005. - V. 86. - № Pt 9. - P. 2507-12.
- Zignego A.L., Brechot C. // J Hepatol. - 1999. V. 31. N - 2. P. 369-76.
Библиографическая ссылка
П.Г. Мальков, Н.В. Данилова, Л.В. Москвина ВНЕПЕЧЕНОЧНЫЕ ОСЛОЖНЕНИЯ ХРОНИЧЕСКОГО ВИРУСНОГО ГЕПАТИТА С (ОБЗОР) // Фундаментальные исследования. 2009. № 5. С. 41-46;URL: https://fundamental-research.ru/en/article/view?id=1932 (дата обращения: 11.05.2026).



