Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE EFFECT OF THE ACTION OF THE EXTRACT FROM KUKUMARIA YAPONICA ON STRUCTURED-FUNCTIONAL CONDITION ADRENAL GLAND INTACTFUL AND STRESSFUL ANIMAL.
Известно, что стресс - реакция является необходимым звеном адаптации организма к многообразным факторам среды, и именно поэтому она была обозначена Г. Селье как «общий адаптационный синдром» (ОАС) [8]. Успешное развитие адаптации устраняет нарушения гомеостаза, первоначально возникшие под влиянием этих факторов. Однако в некоторых ситуациях стресс - реакция из звена адаптации может превращаться в общее звено патогенеза самых разных заболеваний организма (язвенной болезни желудка и двенадцатиперстной кишки, иммунодефицитных состояний, аллергических, кожных и психических заболеваний, ишемический повреждений сердца и др.) [6,9,10]. Непрерывное нарастание в современном мире стрессовых воздействий на человека, приводящих к развитию различных патологических процессов, расширяет задачи ученых в поисках средств, повышающих устойчивость организма в экстремальных условиях [3]. Как известно, состояние адаптации развивается в организме при непременном участии надпочечных желез - эффекторного звена важнейшей регуляторной гипоталамо - гипофизарно - надпочечниковой системы [6]. Особый интерес представляет проблема регуляции функционального состояния надпочечников, играющих ведущую роль в формировании адаптивной резистентности организма.
Цель настоящей работы
На базе ТИНРО - Центра г. Владивостока создана биологически активная добавка (БАД) «Тингол - 2» (спиртовый экстракт из внутренностей кукумарии японской), содержащая в своем составе тритерпеновые глигозиды (ТГ). ТГ голотурий проявляют широкий спектр биологической активности [1,4]. В настоящей работе исследовали влияние экстракта кукумарии японской (ЭКЯ) на развитие реакции стресса у животных с целью выявления стресс - протективного действия.
Материалы и методы
Опыты выполнены на 50 белых беспородных крысах - самцах массой 180 - 220 г, содержащихся в виварии при естественном световом режиме и свободном доступе к воде и пище. Животные были разделены на 5 групп: 1 - интактные; 2 - интактные + острый стресс (контроль); 3 - животные, получавшие экстракт из кукумарии японской (ЭКЯ) (содержание ТГ 650 мкг/мл) в виде одной ежедневной добавки к основному корму в количестве 0,03 мл на 1 кг веса тела + острый стресс; 4 - интактные + стресс 10 дней (контроль); 5 - животные, получавшие ЭКЯ + стресс 10 дней. Стресс моделировали опусканием животных в холодную воду при температуре 6+10С в течение часа однократно или многократно (до 10 дней по 1 разу в день) [2]. В настоящей работе исследовали эффект ЭКЯ на стадии тревоги (однократное пребывание в воде) и стадии истощения (10 дней стресс - воздействия). После легкого эфирного наркоза крыс декапитировали с одномоментным забором крови для определения уровня кортизола. После декапитации животных измеряли массу лимфоидных органов (тимуса, селезенки), надпочечников, состояние слизистой оболочки желудка. Для приготовления гистологических препаратов использовали левый надпочечник. Его извлекали тотчас после забоя, фиксировали в жидкости Карнуа. Серийные парафиновые срезы из средних слоев железы толщиной 7 мкм окрашивали гематоксилином и эозином. Учитывая, что по размерам ядер секреторных клеток можно оценивать функциональное состояние надпочечников [11], мы измеряли площадь ядер клеток пучковой и сетчатой зон надпочечников. Все цифровые данные обрабатывали статистически с использованием критерия Стъюдента.
Результаты исследования и их обсуждение
Исследования показали, что в условиях одночасового стресса (стадия тревоги ОАС) у животных, получавших БАД из кукумарии японской, масса лимфоидных органов снижается менее выражено, чем у контрольных животных. Уменьшение массы тимуса и селезенки у крыс, не получавших БАД из кукумарии японской, статистически значимо, тогда как при стрессировании у экспериментальных животных данные показатели имеют только тенденцию к снижению по сравнению с контрольными крысами. Масса надпочечников в стадию тревоги ОАС практически не отличается от контроля. Не отличается от него и изменения в состоянии слизистой оболочки желудка.
Нормализующий эффект ТГ кукумарии японской в большей степени наблюдался на 10 сутки от начала действия стресс факторов, т. е. на стадии истощения. Это выразилось в предупреждении снижения массы селезенки и тимуса, в менее выраженной гипертрофии надпочечников и изменений слизистой оболочки желудка по сравнению с контрольными животными, у которых отмечено выраженное снижение массы лимфоидных органов, а также значительная гипертрофия надпочечников и более выраженные изменения в слизистой желудка (изменения характерные для стадии истощения ОАС) (табл 1).
Таблица 1. Влияние экстракта из кукумарии японской на соматические проявления стрессовой реакции у крыс при холодовом стрессе
|
Группы |
Масса тимуса, мг |
Масса селезенки, мг |
Масса надпочечников, мг |
Состояние слизистой оболочки желудка |
|
1- интактные
|
424,20 + 22,8 |
437,0 + 14,8 |
29,00 + 2,44 |
Изменений нет |
|
2-(контроль) остр. стресс |
337,5+ 18,9* |
330,0 + 13,9* |
31,00 + 5,71 |
Изменений нет |
|
3 - ЭКЯ + остр. стресс |
370,0 + 25,7 |
368,0 + 27,6 |
30,40 + 2,24 |
Изменений нет |
|
4 - стресс 10 дней (контроль) |
269,0+ 7,5* |
274,0 + 29,5* |
38,50 + 1,86* |
Отек, гиперемия, множественные кровоизлияния * |
|
5 - ЭКЯ + стресс 10 дней |
314,0 + 9,5** |
333 + 19,0 ** |
33,00 + 1,0** |
Единичные кровоизлияния * |
Примечание. * - достоверность различий по сравнению с интактными, ** - достоверность различий по сравнению с контролем, р<0,05
Несмотря на то, что масса надпочечников при остром воздействии не изменялась, почти двукратное повышение уровня кортизола в плазме крови у контрольных животных (85,7 + 4,10 nmol|l, р < 0,05) по сравнению с интактными (45,0 + 1,83 nmol|l) свидетельствовало о резкой активации глюкокортикоидной функции. Достоверных отличий у интактных и кормленных ЭКЯ самцов не обнаружено, уровень кортизола у которых составил 48,0 + 2,34 nmol|l. Развитие стрессового состояния у кормленных крыс также сопровождалось напряжением функциональной активности надпочечников. Однако уровень кортизола существенно ниже концентрации гормона в крови контрольных крыс при стрессе. Уровень кортизола у опытных стрессированных самцов, получавших ЭКЯ составил 67,15 ± 3,32 nmol/l, р< 0,05 (рис. 1).
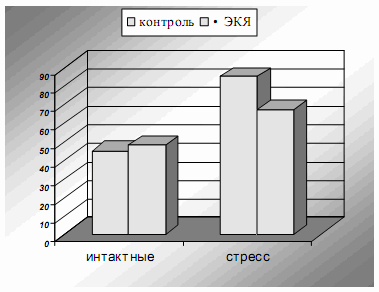
Рис.1. Показатели кортизола в крови интактных, стрессированных и получавших ЭКЯ животных
Морфометрическое исследование клеточных ядер пучковой и сетчатой зон коры надпочечников у крыс выявило, что пучковая зона активируется не только при многократных воздействиях, но и при однократном стрессовом воздействии [6]. Во время острой реакции в пучковой зоне отмечается гипертрофия клеток и их ядер, этот эффект выявляется уже через час после начала действия стрессора [5]. При гистологическом исследовании надпочечников имели место гипертрофия и утолщение пучковой зоны за счет истончения клубочковой и сетчатой зон.
При кариометрии обнаружено, что однократное стрессовое воздействие статистически достоверно увеличивает площадь ядер клеток пучковой зоны у контрольных животных, тогда как у крыс 3 группы достоверных изменений не обнаружено. Сетчатая зона оставалась в покое как у контрольных, так и у экспериментальных животных.
Многократно повторяющиеся стрессовые факторы достоверно увеличивают площадь ядер обеих зон у контрольных животных (табл 2), свидетельствуя тем самым об их значительной активации. В надпочечниках наблюдается истончение капсулы, расширение пучковой зоны, сужение клубочковой и сетчатой зон, стертость границ между зонами, резкое расширение просвета кровеносных сосудов. У экспериментальных животных реакция коры надпочечников на стресс была менее выражена, чем у контрольных.
Таблица 2. Морфометрические показатели секреторных клеток коркового
|
Группы животных |
Площадь ядер клеток пучковой зоны, мкм2 |
Площадь ядер клеток сетчатой зоны, мкм2 |
|
1 - интактные |
32,40 ± 1,92 |
26,60 ± 1,19 |
|
2 - острый стресс (контроль) |
41,60 ± 4,04* |
29,11 ± 2,26 |
|
3 - ЭКЯ + острый стресс |
33,00 ± 2,42 |
29,32 ± 2,71 |
|
4 - стресс 10 дней (контроль) |
53,30 ± 3,71* |
40, 80 ± 3,17* |
|
5 - ЭКЯ + стресс 10 дней |
44,66 ± 4,29** |
33,46 ± 2,78** |
Примечание. * - достоверность различий по сравнению с интактными, ** - достоверность различий по сравнению с контролем, р<0,05
Полученные данные свидетельствуют о наличии антистрессорного действия тритерпеновых гликозидов экстракта из кукумарии японской, о чем можно судить по нормализации соматических проявлений, вызванных стрессом, стабилизации глюкокортикоидной функции. Сохраняя резервные возможности секреторных клеток, экстракт из кукумарии японской повышает устойчивость коры надпочечников к действию экстремальных факторов и оказывает адаптогенный эффект на клеточном и органном уровне.
СПИСОК ЛИТЕРАТУРЫ
- Авилов С.А., Калинин В.И., Дроздова О.А. и др. // Химия природ. соедин. - 1993. -№2. - С. 49 - 52.
- Авакян А.Р., Лазарев А.И., Прокопенко Л.Г., Утешев Б.С. // Эксп. и кл.фарм. - 2002. - Т.65, №3. - С.50 - 53.
- Бондаренко О.Н., Бондаренко Н.А., Манухина Е.Б. // Бюл. эксп. биол. и мед. - 1999. - Т.128, №8. - С.157 - 160.
- Дроздова В.А., Авилов С.А., Калиновский А.И. и др. // Химия природ. соедин. - 1993. - №2. - С. 242 - 248.
- Кириллов О. И. Стрессовая гипертрофия надпочечников. - Москва: Наука, 1994. - 176с.
-
Кресюн В.И., Рожковский Я.В. // Пробл. эндокринологии. - 1992. - Т.38, №3. - С.41 - 44.
- Обут Т.А. // Физиол. ж. им. Сеченова. - 1992. - Т. 78, №4. - С.108 - 112.
- Судаков К.В. // Терапевт. арх. - 1997. - Т.69, №1. - С.70 - 74.
- Судаков К.В. // Патол. Физиолог. И экспер. Терапия. - 1992. - №4. - С.86 - 93.
- Хананашвили М.М // Вестн. Рос.АМН. - 1998. - №8. - С.13 - 16.
- Шапошников В.М. // Пробл.эндокринологии. - 1989. - Т.35, №4. - С.77 -80.
Библиографическая ссылка
Солодкова О.А., Каредина В .С ., Зенкина В.Г., Тимчишина Г.Н. ЭФФЕКТ ДЕЙСТВИЯ ЭКСТРАКТА ИЗ КУКУМАРИИ ЯПОНСКОЙ НА СТРУКТУРНО - ФУНКЦИОНАЛЬНОЕ СОСТОЯНИЕ НАДПОЧЕЧНИКОВ ИНТАКТНЫХ И СТРЕССИРОВАННЫХ ЖИВОТНЫХ // Фундаментальные исследования. 2006. № 11. С. 11-14;URL: https://fundamental-research.ru/en/article/view?id=6494 (дата обращения: 06.05.2026).



