Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
CRITICAL PARAMETERS AND CALCULATION OF DENSITY OF THE MELTED NITRITES AND NITRATES OF MONOVALENT METALS
С целью расчета плотности расплавленных галогенидов щелочных металлов (ГЩМ) в работе [2] мы модифицировали уравнение Л.П. Филиппова [5]
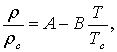 (1)
(1)
предложенное для расчета плотности органических жидкостей, которое в нашей записи имеет вид
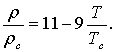 (2)
(2)
Уравнения (1) и (2) позволяют получить ряд простых расчетных соотношений для нахождения ![]() и
и ![]() , а также коэффициентов термического расширения (
, а также коэффициентов термического расширения (![]() ) расплавов:
) расплавов:
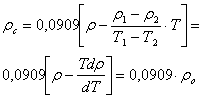 (3)
(3)
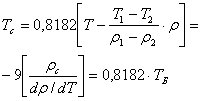 (4)
(4)
![]() . (5)
. (5)
В этих уравнениях A и B - постоянные, ![]() и
и ![]() - критические плотности и температуры, ρ и T - их текущие значения, ρ0 и TБ - плотность расплавов при 0, К и температура Бойля соответственно.
- критические плотности и температуры, ρ и T - их текущие значения, ρ0 и TБ - плотность расплавов при 0, К и температура Бойля соответственно.
В настоящей работе сделана попытка применить уравнение (2) для расчета плотности расплавленных нитритов и нитратов одновалентных металлов. Однако решение поставленной задачи требует прежде всего знаний критических параметров ![]() и
и ![]() , которые в литературе практически отсутствуют. В справочнике [1] приводятся эти значения для ГЩМ и нитратов щелочных металлов и таллия, вычисленные на основе закона соответственных состояний. Однако, сравнение с данными для ГЩМ, приведенными в [3,6,7,8], показывает, что
, которые в литературе практически отсутствуют. В справочнике [1] приводятся эти значения для ГЩМ и нитратов щелочных металлов и таллия, вычисленные на основе закона соответственных состояний. Однако, сравнение с данными для ГЩМ, приведенными в [3,6,7,8], показывает, что ![]() явно занижены, а
явно занижены, а ![]() - сильно завышены. Кроме того, если даже для ГЩМ опубликованные значения критических параметров до сих пор не получили прямого экспериментального подтверждения, то еще более сложная ситуация возникает для термически распадающихся солей, к каковым относятся нитриты и нитраты одновалентных металлов. Для этих расплавов критические параметры являются чисто гипотетическими. Поэтому применение уравнения (2) будет являться корректным только в случае термодинамического подобия рассматриваемых солей и галогенидов щелочных металлов, данные для которых были опубликованы нами ранее [2]. Одинаковые значения приведенных параметров
- сильно завышены. Кроме того, если даже для ГЩМ опубликованные значения критических параметров до сих пор не получили прямого экспериментального подтверждения, то еще более сложная ситуация возникает для термически распадающихся солей, к каковым относятся нитриты и нитраты одновалентных металлов. Для этих расплавов критические параметры являются чисто гипотетическими. Поэтому применение уравнения (2) будет являться корректным только в случае термодинамического подобия рассматриваемых солей и галогенидов щелочных металлов, данные для которых были опубликованы нами ранее [2]. Одинаковые значения приведенных параметров ![]() и
и ![]() будут определять соответственные состояния. Мы проверили реальность существования термодинамического подобия расплавов, рассчитав при соответствующих температурах значения
будут определять соответственные состояния. Мы проверили реальность существования термодинамического подобия расплавов, рассчитав при соответствующих температурах значения ![]() 0,4 и 0,6) по справочным данным [4] и установили факт их практического равенства с вычисленными по уравнению (2). В то же время, например, щелочные металлы не являются термодинамически подобными указанным солям и не подчиняются уравнению (2). Поэтому, вначале мы оценили параметры ρc (уравнение 3) и Tc (уравнение 4), а затем приступили к расчету температурной зависимости плотности расплавленных нитритов и нитратов.
0,4 и 0,6) по справочным данным [4] и установили факт их практического равенства с вычисленными по уравнению (2). В то же время, например, щелочные металлы не являются термодинамически подобными указанным солям и не подчиняются уравнению (2). Поэтому, вначале мы оценили параметры ρc (уравнение 3) и Tc (уравнение 4), а затем приступили к расчету температурной зависимости плотности расплавленных нитритов и нитратов.
В таблице 1 представлены вычисленные значения параметров ρc и Tc.
Таблица 1. Критические параметры расплавов нитритов и нитратов одновалентных металлов.
|
соль |
Tc,К |
ρc,г/см3 |
соль |
Tc,К |
ρc,г/см3 |
|
NaNO2 |
2441 |
0,2023 |
RbNO3 |
2567 |
0,2772 |
|
KNO2 |
2686 |
0,1970 |
CsNO3 |
2541 |
0,3291 |
|
LiNO3 |
3099 |
0,1880 |
AgNO3 |
3573 |
0,4049 |
|
NaNO3 |
2655 |
0,2109 |
TlNO3 |
2534 |
0,5276 |
|
KNO3 |
2598 |
0,2104 |
|
|
|
Таблица 2 иллюстрирует воспроизводимость экспериментальных данных [4] по плотности расчетным уравнением (2) при минимальной и максимальной температуре исследованного интервала. Из таблицы 2 видно, что расчетные и экспериментальные значения плотности в точности совпадают.
Таким образом, установленное термодинамическое подобие нитритов, нитратов и галогенидов одновалентных металлов позволило оценить критические параметры этих солей и описать данные по плотности единым уравнением в широкой области температур.
Таблица 2. Сравнение расчетных и экспериментальных значений плотности ρ (г/см3) расплавленных нитритов и нитратов одновалентных металлов.
|
Соль |
Интервал температур, К |
(расчет) |
(эксп.) |
(расчет) |
(эксп.) |
|
NaNO2 |
570 - 720 |
1,800 |
1,801 |
1,688 |
1,689 |
|
KNO2 |
710 - 750 |
1,698 |
1,698 |
1,672 |
1,672 |
|
LiNO3 |
550 - 690 |
1,768 |
1,768 |
1,691 |
1,691 |
|
NaNO3 |
590 - 700 |
1,898 |
1,898 |
1,819 |
1,820 |
|
KNO3 |
620 - 870 |
1,863 |
1,863 |
1,680 |
1,681 |
|
RbNO3 |
590 - 760 |
2,476 |
2,476 |
2,310 |
2,310 |
|
CsNO3 |
690 - 760 |
2,816 |
2,816 |
2,734 |
2,734 |
|
AgNO3 |
490 - 600 |
3,354 |
3,954 |
3,842 |
3,842 |
|
TlNO3 |
480 - 560 |
4,904 |
4,905 |
4,754 |
4,755 |
СПИСОК ЛИТЕРАТУРЫ
- Гороновский И.Т., Назаренко Ю.П., Некряч Е.Ф. // Краткий справочник по химии. Киев: Наукова думка. 1974. С. 991.
- Новожилов А.Л.. Поволоцкий А.В. // Журнал физической химии. 2004. Т. 78. № 5. С. 824.
- Скрипов В.П., Файзуллин М.З., Штейнерт А.В.// Журнал физической химии. 1987. Т. 61. №2. С.344.
- Справочник по расплавленным солям/Под ред. А.Г. Морачевского. Л.: Химия, 1971. Т. 1. - 168 с.
- Филиппов Л.П. // Физика и физико-химия жидкостей. М.: Изд-во МГУ, 1973. В. 2. С. 133.
- Kirshenbaum A.D., Chill J.A., Mc Gonigal P.J., Grosse A.V.//J. Jnorg. Nucl. Chem. 1962. V. 24. №10. Р. 1287.
- Kohler F.//Monatsh. Chem. 1972. B. 130. №13. S. 685.
- Mc Gonigal P.J.//J. Phys. Chem. 1963. V. 67. №9. р. 1931.
Библиографическая ссылка
Новожилов А.Л., Федотова Н.Н. КРИТИЧЕСКИЕ ПАРАМЕТРЫ И РАСЧЕТ ПЛОТНОСТИ РАСПЛАВЛЕННЫХ НИТРИТОВ И НИТРАТОВ ОДНОВАЛЕНТНЫХ МЕТАЛЛОВ // Фундаментальные исследования. 2006. № 9. С. 18-20;URL: https://fundamental-research.ru/en/article/view?id=5307 (дата обращения: 16.05.2026).



