Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
PATHOGENETIC BASIS OF THE USE EXPEDIENCY OF CYTOFLAVIN AT ISCHEMIC MYOCARDIAL DAMAGE
Ишемическое повреждение миокарда является одной из наиболее частых причин развития инфаркта миокарда, аритмий, острой или хронической сердечной недостаточности, приводя к развитию печального исхода болезни.
Естественно, что в многочисленных клинических и экспериментальных исследованиях предпринимаются попытки медикаментозной коррекции системных метаболических и функциональных расстройств, предшествующих и сопутствующих развитию коронарной недостаточности [9].
В клинической терапии ишемической болезни сердца давно утвердилось использование препаратов, улучшающих коронарный кровоток и соответственно доставку основных субстратов синтеза макроэргов в миокарде: жирных кислот, лактата, глюкозы, кислорода и др. В этих целях применяют коронародилататоры, антикоагулянты, антиагреганты. Одновременно подавляются энергетические потребности миокарда β - адреноблокаторами, обеспечивается нормализация липидного спектра крови, углеводного обмена [10]. Между тем, в ишемизированном миокарде возникают глубокие метаболические расстройства, приводящие к усугублению структурных изменений в предварительно ишемизированном миокарде на фоне его реперфузии при использовании вышеуказанных способов медикаментозной коррекции.
В последние годы широкое распространение в комплексной терапии ишемии миокарда получило использование цитофлавина [2,5,6,7,8]. Как известно, цитофлавин комплексный препарат, разработанный научно-технологической фармацевтической фирмой «Полисан» (Санкт-Петербург, 2000 г), включающий рибоксин, рибофлавин мононуклеотид, никотинамид, янтарную кислоту. Каждый из указанных препаратов довольно широко применяется в клинической практике при различных формах патологии. Естественно предположить, что использование указанных препаратов в комплексе может обеспечить новые метаболические эффекты в условиях ишемии.
Установлено, что рибоксин реализует свои метаболические эффекты на миокард, будучи агонистом пуринэргических рецепторов, при участии которых происходит активация гликолиза - важнейшего процесса для поддержания энергетического пула в миокарде в условиях гипоксии. Кроме того, рибоксин потенцирует эффекты аденозина, участвующего в образовании NO и развитии вазодилатации [1].
Другим компонентом цитофлавина является рибофлавина мононуклеотид, обеспечивающий высокую активность глютатионпероксидазы, а также ряда дыхательных ферментов митохондрий. Отметим, что флавиновые ферменты участвуют и в реализации активности сукцинатдегидрогеназы и потреблении сукцината через метаболические шунты [1].
Никотинамид - прекурсор коферментов дегидрогеназ (НАД+ и НАДФ+) (Gilman et al,.1985) [1], и тем самым обладающий эффектами антигипоксанта.
Последний компонент цитофлавина янтарная кислота - эндогенный субстрат клетки, метаболизируется в цикле трикарбоновых кислот (ЦТК), улучшает тканевое дыхание за счет усиления транспорта электронов в митохондриях, ускоряет оборот дикарбоновой части ЦТК (сукцинат - фумарат - малат) и тем самым усиливает энергообеспечение клетки [1].
В связи с этим целью настоящего исследования явилось патогенетическое обоснование целесообразности использования указанного препарата на основе изучения его метаболических эффектов в ишемизированном миокарде.
Материалы и методы. Эксперименты по изучению метаболических особенностей миокарда в норме и при патологии проведены на 60 беспородных белых крысах самцах массой 250-300 г.
В гомогенатах миокарда изучено содержание АТФ и креатинфосфата с помощью наборов Био-Ла-Тест чешской фирмы «Лахема». Одновременно проведена оценка активности ряда ферментов гомогенатов миокарда, участвующих в процессах энергообеспечения миокарда - сукцинатдегидрогеназы (СДГ), лактатдегидрогеназы (ЛДГ) [3,4], а также аспартатаминотрансферазы (АсАТ) (с помощью наборов Био-Ла-Тест чешской фирмы «Лахема»).
Сравнительные серии экспериментов проведены в группе интактных животных, ложнооперированных животных и:
● в группе животных с экспериментальной ишемией миокарда, достигаемой окклюзией коронарной артерии по методу H.Selye. в модификации Саидова А.Б. и соавторов [11,12] без медикаментозной коррекции;
● в группе животных с экспериментальной ишемией миокарда на фоне внутривенного введения цитофлавина сразу после окклюзии коронарной артерии в дозе 1.5 мл/кг и далее в течение трех суток наблюдения (1 раз в сутки внутривенно в указанной дозе).
Влияние гипоксии и соответственно цитофлавина на метаболизм миокарда исследовано в динамике: спустя 60 мин и 72 часа после окклюзии.
Результаты исследований были подвергнуты статистическому анализу с помощью программ Statistica 99 (Версия 5.5 А, «Statsoft, Inc», г. Москва, 1999); «Microsoft Excel, 97 SR-1» (Microsoft, 1997). Проведен расчет коэффициентов линейной корреляции (Реброва О.Ю., 2003).
Результаты и их обсуждение. Как оказалось в группе животных с экспериментальной ишемией миокарда возникали выраженные метаболические расстройства в миокарде в динамике патологии.
Так, спустя 60 мин с момента развития окклюзии коронарной артерии возникало снижение содержания в гомогенатах миокарда креатинфосфата примерно на 25 % и уровня АТФ - на 20 %. Полученные нами результаты соответствуют общепринятым представлениям нарушения энергообеспечения миокарда в условиях ишемии. Касаясь значимости выявленного феномена, следует отметить возможность одномоментного развития реакций адаптации и дезадаптации в условиях энергодефицита, требующих определенной медикаментозной коррекции. С одной стороны, в условиях ишемии усиливается дефосфорилирование АТФ при участии 5-нуклеотидазы с образованием аденозина, обеспечивающего при определенных условиях коронародилатирующий эффект. С другой стороны, дефицит АТФ и креатинфосфата в ишемизированном миокарде приводит к подавлению всех энергозависимых реакций: трансмембранного переноса ионов, сопряжения процессов возбуждения и сокращения актомиозинового комплекса в миокарде, всех этапов синтеза белка.
Высказывается точка зрения о том, что наименее чувствительной к развитию ишемии миокарда является система окисления янтарной кислоты (Г.Н. Копылов, 2005). В связи с эти представляется интерес сопоставить состояние активности ЛДГ и СДГ гомогенатов миокарда в динамике ишемии.
Результаты проведенных нами исследований свидетельствовали о том, что уже через 60 мин с момента развития ишемии возникало подавление активности СДГ гомогенатов миокарда (р<0.01, рис. 1а) в то время, как активность ЛДГ (р<0.001, рис. 3а) гомогенатов миокарда не отличалась от показателей контроля; одновременно отмечалось снижение активности АсАТ гомогенатов миокарда (р<0.001, рис. 2а).
Как известно, подавление активности трансаминаз может служить косвенным показателем нарушения окислительных процессов в цикле Кребса, поскольку необходимые для переаминирования альфа-кетокислоты (α-кетоглутаровая, щавелевоуксусная) обеспечиваются реакциями ЦТК. Прямым доказательством подавления цикла Кребса является угнетение активности СДГ - флавопротеина сукцината с образованием фумарата.
Сравнительная серия экспериментов по изучению влияния цитофлавина на энергетическое обеспечение миокарда в те же сроки наблюдения (60 мин с момента развития ишемии) позволила обнаружить положительные метаболические эффекты. Так, содержание креатинфосфата гомогенатов миокарда (р<0.01, рис. 4а) достоверно возрастало, а АТФ (р<0.01, рис. 5а) не изменялось по сравнению с соответствующими показателями группы контроля. Это свидетельствует об активации под влиянием цитофлавина креатинфосфокиназной реакции. Одновременно возрастала активность СДГ (р<0.01, рис. 1а) и АсАТ (р<0.001, рис. 2а) гомогенатов миокарда, что свидетельствует об активации окисления субстратов в цикле Кребса, усилении переаминирования аминокислот с α-кетокислотами - продуктами цикла Кребса.
Спустя 72 часа с момента развития ишемии миокарда возникало прогрессирующее снижение содержания АТФ (р<0.01, рис. 5б) и креатинфосфата (р<0.01, рис. 4б) в гомогенатах миокарда. При этом активность СДГ гомогенатов миокарда (р<0.01, рис. 1б) оставалась низкой, как и в предыдущий период наблюдения, а активность ЛДГ (р<0.01, рис. 3б) и АсАТ (р<0.001, рис. 2б) гомогенатов миокарда заметно снижалась по отношению к таковым показателям контрольной группы животных и более раннему периоду ишемии миокарда.
Сравнительные исследования с внутривенным введением цитофлавина, спустя 72 часа с момента развития ишемии миокарда, свидетельствовали о положительных метаболических эффектах указанного препарата. Наблюдалось резкое увеличение содержания АТФ (р<0.01, рис. 5б) и креатинфосфата (р<0.01, рис. 4б) гомогенатов миокарда по отношению к таковым показателям группы сравнения без медикаментозной коррекции в соответствующий период ишемии миокарда. При этом уровень указанных макроэргов достигали показателей нормы. Многократное применение цитофлавина в динамике ишемии миокарда приводило и к нормализации показателей активности СДГ (р<0.01, рис. 1б), ЛДГ (р<0.01, рис. 3б), АсАТ (р<0.01, рис. 2б) гомогенатов миокарда.
Таким образом, использование комплексного препарата цитофлавина обеспечивало ускорение нормализации энергетического обеспечения миокарда за счет активации гликолитической реакции и окисления субстратов в цикле трикарбоновых кислот, а также реакций перефосфорилирования с участием креатинфосфокиназы.
Выводы.
- В динамике экспериментальной ишемии миокарда возникает прогрессирующее снижение уровня АТФ и креатинфосфата в миокарде, сочетающееся с подавлением активности СДГ, ЛДГ, АсАТ.
- Подавление активности СДГ опережает по времени снижение активности ЛДГ. Последнее имеет место лишь на поздних стадиях ишемии миокарда.
- Достигнута положительная коррекция метаболических сдвигов в ишемизированном миокарде, более выраженная на поздних стадиях ишемии миокарда при использовании комплексного препарата цитофлавина, включающего янтарную кислоту, никотинамид, рибоксин и рибофлавин.
- Цитофлавин обеспечивает противоишемический эффект за счет активации сукцинатдегидрогеназного окисления, окислительно - восстановительных процессов, поскольку никотинамид является простетической группой ферментов - кодегидрогеназы I (НАД) и кодегидрогеназы II (НАДФ) - переносчиков водорода.
- Усиление энергообеспечения ишемизированного миокарда на фоне введения цитофлавина достигается и за счет рибоксина - предшественника АТФ, активатора ряда ферментов цикла Кребса, а также за счет рибофлавина мононуклеотида. Последний, как известно, входит в состав ферментов, регулирующих окислительно-восстановительные процессы.
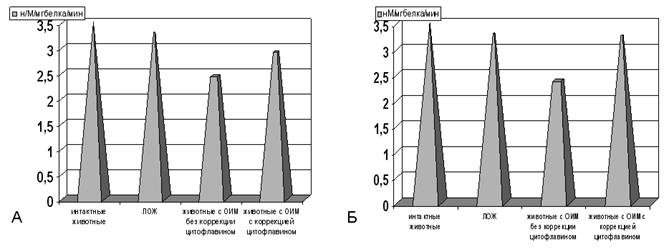
Рисунок 1. Содержание СДГ в гомогенатах миокарда на фоне острой ишемии миокарда с медикаментозной коррекцией цитофлавином.
Примечание: А - через 60 мин, Б - через 72 часа. ЛОЖ- ложнооперированные животные, ОИМ- острая ишемия миокарда. Степень достоверности полученных данных указана в тексте.
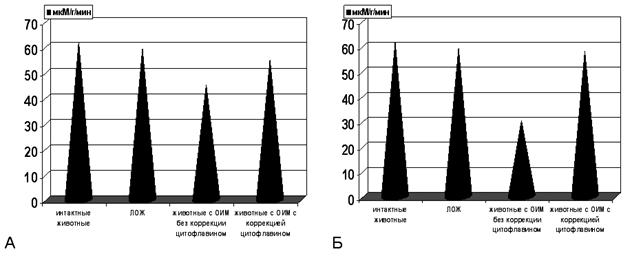
Рисунок 2. Содержание АсАТ в гомогенатах миокарда на фоне острой ишемии миокарда с медикаментозной коррекцией цитофлавином.
Примечание: А - через 60 мин, Б - через 72 часа. ЛОЖ- ложнооперированные животные, ОИМ- острая ишемия миокарда. Степень достоверности полученных данных указана в тексте.
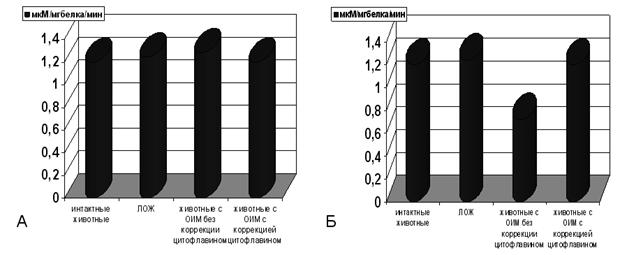
Рисунок 3. Содержание ЛДГ в гомогенатах миокарда на фоне острой ишемии миокарда с медикаментозной коррекцией цитофлавином.
Примечание: А - через 60 мин, Б - через 72 часа. ЛОЖ- ложнооперированные животные, ОИМ- острая ишемия миокарда. Степень достоверности полученных данных указана в тексте.
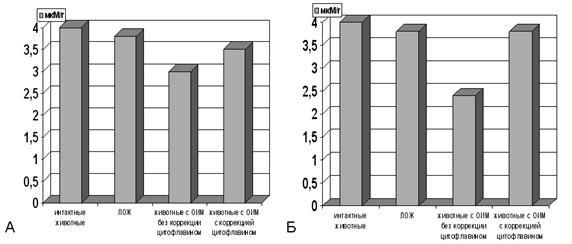
Рисунок 4. Содержание КФ в гомогенатах миокарда на фоне острой ишемии миокарда с медикаментозной коррекцией цитофлавином.
Примечание: А - через 60 мин, Б - через 72 часа. ЛОЖ- ложнооперированные животные, ОИМ- острая ишемия миокарда. Степень достоверности полученных данных указана в тексте.
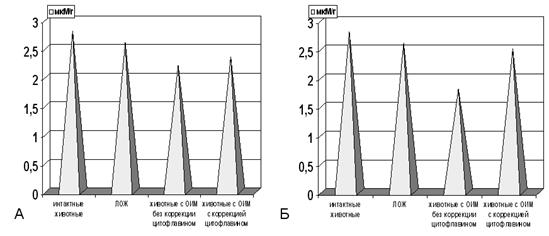
Рисунок 5. Содержание АТФ в гомогенатах миокарда на фоне острой ишемии миокарда с медикаментозной коррекцией цитофлавином.
Примечание: А - через 60 мин, Б - через 72 часа. ЛОЖ- ложнооперированные животные, ОИМ- острая ишемия миокарда. Степень достоверности полученных данных указана в тексте.
СПИСОК ЛИТЕРАТУРЫ
- Афанасьев В.В. Цитофлавин в интенсивной терапии: Пособие для врачей. - СПб. - 2005.- 36 с. - с. 9-30.
- Бульон В.В., Хныченко Л.К., Сапронов Н.С., Коваленко А.Л., Алексеева Л.Е. Использование цитофлавина для коррекции последствий ишемического повреждения миокарда //Экспериментальная и клиническая фармакология. - 2002. - Том 65, №1. с. 27-29.
- Ещенко Н.Д., Прохорова М.И. Методы биохимических исследований - ЛГУ, Ленинград, 1982. - с.224-226
- Ещенко Н.Д., Вольский Г.Г., Прохорова М.И. Методы биохимических исследований - ЛГУ, Ленинград, 1982. - с. 210-212.
- Коваленко А.Л., Белякова Н.В. Янтарная кислота - фармокологическая активность и лекарственные формы. //Фармацея. - 2000. - №5-6. - с. 40-44.
- Лычаков А.В., Шевчук М.К., Саватеева Т.Н., Колбасов С.Е., Коваленко А.Л. Эффективность цитофлавина при лечении экспериментальной алкогольной кардиомиопатии //Токсикологический вестник. - 2002.-№2. - с.21-25.
- Моисеева О.М., Селиванова Г.В., Власова Т.Д., Коваленко А.Л., Алексеева Л.Е., Семенова Е.Г. Изучение защитного влияния метаболических лекарственных препаратов на кардиомиоциты в их первичной культуре при острой и хронической ишемии //Цитология. - 1999. - №3-4. - с.294.
- Оболенский С.В., Николаев А.А., Аббясов И.Г., Сливин О.А., Николаев А.В., Еремина М.В. Интраоперационная защита миокарда в коронарной хирургии на работающем сердце //Вестник академии им И.И. Мечникова. - 2003. - № 4(4). с. 114-117.
- Окороков А.И. Диагностика болезней сердца и сосудов /А.И. Окороков //Диагностика болезней внутренних органов: Т. 6. - М.: Мед. лит., 2002. - 464 с.: ил. - с. 92-114.
- Окороков А.И. Лечение болезней внутренних органов: Т. 3, кн.1. Лечение болезней сердца и сосудов: - М.: Мед. лит., 2002 - 464.: ил. - с. 48 - 130.
- Саидов А.Б., Каримов Х.Я., Юлдашев Н.М., Саидов С.А. //Успехи современного естествознания. - 2006. - №3. с. 33-35.
- Selye H., Bayusz E., Crasso, and Mendell, Angiologia, 11, 1960. - 398-407.
Библиографическая ссылка
Бизенкова М.Н., Чеснокова Н.П., Романцов М.Г. ПАТОГЕНЕТИЧЕСКОЕ ОБОСНОВАНИЕ ЦЕЛЕСООБРАЗНОСТИ ИСПОЛЬЗОВАНИЯ ЦИТОФЛАВИНА ПРИ ИШЕМИЧЕСКОМ ПОВРЕЖДЕНИИ МИОКАРДА // Фундаментальные исследования. 2006. № 4. С. 20-24;URL: https://fundamental-research.ru/en/article/view?id=4924 (дата обращения: 15.05.2026).



