Титанат лития является перспективным электродным материалом для литий-ионных химических источников тока, используемых в устройствах современных средств связи, компьютерной техники, широкого круга оборудования гражданского и специального назначения [1–3]. Его использование позволяет в процессе интеркаляции – деинтеркаляции лития при эксплуатации источника тока избежать объемного изменения структуры материала, обеспечить повышенную взрыво- и пожаробезопасности всего устройства.
Главное преимущество титаната лития состоит в том, что рабочий потенциал такого электрода более, чем на 1 В положительнее потенциала литиевого электрода, что исключает образование дендритов и восстановление электролита. Вместе с тем, основным недостатком титаната лития состава Li4Ti5O12, как и ряда других используемых в литий-ионных аккумуляторах электродных материалов, является низкая электронная и ионная проводимость [4–6], что обусловливает недостаточную и нестабильную емкость аккумулятора и, как следствие, неудовлетворительную циклируемость при интеркаляции-деинтеркаляции ионов лития в режиме «заряд – разряд». Улучшение этих показателей может быть достигнуто разработкой методов синтеза высокодисперсных порошков, допирования гетеровалентными компонентами и создания композитов электродный материал – твердый электролит. В настоящее время проблема гетеровалентного допирования титаната лития далека от своего окончательного решения и требует накопления обширного экспериментального материала по методам синтеза. Для получения ультрадисперсных порошков титаната лития перспективен синтез в жидких средах, обеспечивающий высокую степень гомогенизации компонентов в системе. Золь-гель синтез сложных оксидов титана (IV) предполагает гидролиз солей с образованием оксогидроксокомплексов состава TiО2-x(ОН)2x·nН2О, взаимодействие которых с катионами металлов должно приводить к образованию соединений заданного состава. Однако характерные для оксогидроксосоединений титана (IV) процессы оляции и оксоляции нарушают стехиометрию синтезируемых целевых соединений, в результате чего наблюдается появление примесных фаз. Для предотвращения процессов оляции-оксоляции и сохранения ионообменных центров предложено использовать в качестве прекурсоров высокогидратированные соединения состава TiO1-x(ONH4)2+2x•aq с молярным отношением NH4+:Ti(IV), не меньшим, чем отношение катионов щелочного металла и титана в целевом продукте [7]. Такой прекурсор может быть получен гидролизом аммоний титанил сульфата состава (NH4)2TiO(SO4)2•H2O, являющегося продуктом переработки титанового сырья [8]. Замещение в продукте гидролиза аммоний титанил сульфата катионов аммония на катионы лития обеспечивает заданное соотношение металлов. Дегидратация и кристаллизация такого гидратированного литий-замещенного соединения после термообработки приводит к образованию соединения требуемого состава.
Целью исследования явилось изучение влияния легирования катионами лантана (III) высокогидратированного титанаммониевого прекурсора на дисперсность, фазовый состав и электрохимические свойства порошков титаната лития состава Li4Ti5O12. Выбор в качестве допанта лантана (III) обусловлен возможностью создания как дефектной структуры материала, так и композита с равномерно распределенным твердым электролитом состава Li3xLa2/3-xTiO3, обладающим высокой литий-ионной проводимостью [9–11].
Материалы и методы исследования
Титанат лития синтезировали в виде высокодисперных порошков согласно [7, 8]. Для синтеза использовали титанаммониевый прекурсор, который был получен гидролизом (NH4)2TiO(SO4)2•H2O при введении его раствора в концентрированный раствор аммиака. Отличительной особенностью исходных титансодержащих растворов является их технологичность: низкое концентрационное отношение H2SO4:TiO2 значительно сокращает расход реагентов на получение целевого продукта, а образующийся в результате гидролиза раствор сульфата аммония может быть возвращен на получение исходного сульфата титанила и аммония. Титанаммониевый прекурсор отмывали от избытка аммиака репульпированием в воде до pH 8–8,5. Замещение катионов аммония на катионы лития проводили при температуре 90–95 °С обрабаткой раствором гидроксида и нитрата лития при отношении Li:Ti(IV) 0,8–1,04 моль/моль. Допирование катионами лантана (III) осуществляли введением в суспензию раствора нитрата лантана при контролируемых значениях pH. Дальнейшая термообработка замещенного литием прекурсора обеспечивала получение целевого продукта. При анализе состава твердых фаз и растворов использовали атомно-адсорбционный спектрофотометр AAS 300 Perkin-Elmer, массспектрометрометр «ELAN 9000 DRC-e» фирмы PerkinElmer, спектрометр ICPS-9000 фирмы Shimadzu (Япония). Дифференциально-термическое и термогравиметрическое исследования проводили при 25–1000 °C на анализаторе NETZSCH STA 409 PC/PG Luxx. Значения pH водных растворов и суспензий, содержащих синтезированные соединения, измерены на иономере И-130.2М.1. Фазовый состав образцов синтезированных продуктов изучен на дифрактометре ДРОН-3 с CuKa-излучением и графитовым монохроматором. Для идентификации фаз использовали банк данных JCPDS. Контроль размера частиц, морфологии их поверхности и величины удельной поверхности твердых фаз проводили методом десорбции азота на приборе «FlowSorb II 2300» фирмы Micrometritics (США) и методом сканирующей электронной микроскопии с использованием SEM LEO-420. Измерения проводимости (s) выполняли методом спектроскопии электрохимического импеданса в двухэлектродной ячейке с использованием импедансметра Elins Z-2000 в диапазоне частот 102–2×106 Гц при амплитуде сигнала 50–100 мВ. Образцы таблет диаметром 10–12 мм и высотой 2–3 мм готовили по керамической технологии. Электроды наносили на торцы таблет натиранием мелкодисперсного графитового порошка. Гальваностатическое циклирование макетов аккумулятора при тестировании полуячейки в режиме заряд – разряд проводили в диапазоне от 3 до 1 В при скорости 0,05 и 0,2 С с использованием многоканального стенда LANDCT2001A и потенциостата-гальваностата MetrohmAutolab PGSTAT30. Электродную массу для электрохимических измерений получали смешиванием порошка титаната лития, ацетиленовой сажи и поливинилиденфторида в N-метилпирролидоне. Электролитом служил 1 М раствор LiBF4 в смеси с пропиленкарбонатом. В качестве противоэлектрода и электрода сравнения использовали металлический литий.
Результаты исследования и их обсуждение
Исследования показали, что, согласно [7, 8], замещение катионов аммония на катионы лития в высокогидратированном титанаммониевом прекурсоре обеспечивает получение рентгеноаморфного гидратированного сложного оксида титана и лития с отношением Li:Ti, равным 4:5. При его термолизе в интервале 50–300 °C наблюдается эндотермический эффект, отвечающий практически полной дегидратации. В интервале 320–350 °C завершается кристаллизация с образованием высокодисперсного монофазного порошка титаната лития. Содержание в продукте Li2О – 13,5 мас. % и TiO2 – 86,3 мас. % соответствует Li4Ti5O12. При повышении температуры и времени термообработки средний размер частиц порошков увеличивается (рис. 1). Введение на стадии формирования литий-титанового прекурсора до 4 мас. % La (III) не меняет кристаллическую структуру материала, однако при этом увеличивает дисперсность порошка (рис. 1). Дальнейшее увеличение содержания введенных в состав материала катионов лантана (III) позволяет получить композитный материал на основе титаната лития Li4Ti5O12 с равномерным распределением в нем твердого электролита Li0.5La0.5TiO3 (рис. 2).
Влияние легирования титаната лития лантаном (III) на дисперсность синтезируемого материала может быть связано с образованием структурных дефектов, которые создают микронапряжения и не позволяют формировать относительно крупные кристаллиты, а также со специфической адсорбцией катионов допанта и локализацией его преимущественно на межзеренных поверхностях, что обусловливает образование избыточных дефектов и в приповерхностной области формирующихся частиц порошка.
В соответствии со спектрами электрохимического импеданса (рис. 3) увеличение дисперсности порошков титаната лития, их легирование катионами лантана (III) и формирование композитов, содержащих твердый электролит Li3xLa2/3-xTiO3, существенным образом сказывается на электропроводности материала: позволяет повысить проводимость керамики синтезированного материала на 2–3 порядка – с 1,7•10-7 до 5•10-5 См·см-1.
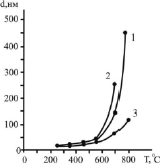
Рис. 1. Зависимость среднего размера частиц порошков титаната лития от температуры термообработки. Время термообработки (час.): 1 – 2; 2 – 8; 3 – 2, порошок легирован 0,5 мас. % лантана (III)
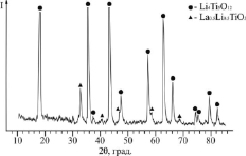
Рис. 2. Рентгенограмма порошка титаната лития (Li4Ti5O12) с равномерно распределенным в нем твердым электролитом (Li0.5La0.5TiO3). Температура обработки 800 °С
Повышение проводимости при модифицировании титаната лития катионами лантана (III) обусловливает улучшенные зарядно-разрядные характеристики и их стабильность при циклировании композита. Причина может состоять в том, что повышение дефектности структуры за счет встраивания ионов лантана (III) в кристаллическую решетку титаната лития уменьшает препятствия для диффузии Li+ и повышают его коэффициент диффузии.
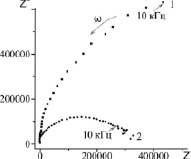
Рис. 3. Годографы электрохимического импеданса (Ом) при 25 °C титаната лития состава Li4Ti5O12 (1) и композита Li4Ti5O12, содержащего твердый электролит Li0.5La0.5TiO3 (2)
Результаты исследования электрохимического поведения полуячеек при скорости циклирования 0,05 и 0,2 С в диапазоне 3–1 В (рис. 4, а и б) показали, что ход зарядных и разрядных кривых практически идентичен. Образцы характеризуются схожим поведением, типичным для титаната лития, что говорит о едином реакционном механизме. При скорости циклирования 0,05 С процессы интеркаляции-деинтеркаляции протекают в широком диапазоне степеней превращения практически при постоянном потенциале, который на плато кривых составляет 1,5 В. Кривые имеют вид, характерный для процессов обратимого типа. Постоянство потенциала для процессов заряда-разряда показывает, что циклирование макета аккумулятора происходит практически без участия фаз переменного состава.
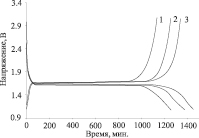
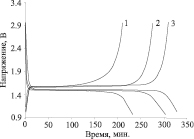
а) б)
Рис. 4. Зарядно-разрядные кривые макетов полуячеек при цклировании током 0,05 C (а) и 0,2 C (б). Анодный материал: 1 – титанат лития; 2 – титанат лития, легированный 0,5 мас. % La (III); 3 – титанат лития, легированный 4 мас. % La (III)
Хотя различие в генезисе материала не сказывается на значении потенциала интеркаляции-деинтеркаляции катионов лития, в целом легирование лантаном (III) на стадии синтеза прекурсора приводит к повышению емкости материала и стабилизации ее при циклировании. Апробация образцов порошков на основе титаната лития в качестве анодного материала показала хорошую циклируемость. Емкость макетов на первых циклах при 0,05 C близка к теоретической и составляет 175–190 мА·ч/г. После 40 циклов емкость легированных образцов практически не снижается, а нелегированный титанат лития показывает небольшую деградацию емкости, которая уменьшается до 170 мА·ч/г. При скорости циклирования 0,2 C наблюдается уже существенная деградация емкости нелегированного титаната лития: она уменьшается от 150 мА·ч/г на первых циклах до 120 мА·ч/г через 40 циклов. В ходе последующего многократного циклирования наблюдается снижение интенсивности деградации емкости. Для легированного лантаном (III) титаната лития наблюдается увеличение емкости материала и уменьшение ее деградации при многократном циклировании. Значение емкости образца 2 уменьшалась от 160 мА·ч/г на первых циклах до 140 мА·ч/г после 40 циклов. Деградации емкости образца 3 не наблюдалось: ее значение составляло 165–170 мА·ч/г при многократном циклировании. Полученные результаты позволяют сделать вывод о повышенной обратимости процесса интеркаляции-деинтеркаляции Li+ в структуре титаната лития при его легировании катионами лантана (III).
Выводы
Методом ионного обмена в водной среде синтезирован гидратированный прекурсор с отношением Li:Ti=4:5, его термообработка обеспечивает получение наноразмерных монофазных кристаллических порошков титаната лития состава Li4Ti5O12 со структурой кубической шпинели. Легирование титаната лития катионами лантана (III) до 4 мас. % не меняет кристаллическую структуру материала, но увеличивает дисперсность порошка. Такая зависимость может быть связана с образованием структурных дефектов, которые создают микронапряжения и не позволяют формировать относительно крупные кристаллиты, а также со специфической адсорбцией катионов допанта на межзеренных поверхностях, что обусловливает образование избыточных дефектов в приповерхностной области частиц порошка. Увеличение содержания введенных в состав материала катионов лантана (III) позволяет получить композитный материал титаната лития Li4Ti5O12 с равномерным распределением в нем твердого электролита Li0.5La0.5TiO3. Уменьшение размеров частиц порошков титаната лития состава Li4Ti5O12 при легировании катионами лантана (III) и формирование композитов, содержащих твердый электролит, увеличивает литий-ионную проводимость на 2–3 порядка, повышает и стабилизирует емкость, предотвращает деградацию материала при циклировании в режиме «заряд – разряд».
Исследования выполнены при финансовой поддержке Российского научного фонда (РНФ) в рамках научного проекта № 17-19-01522.
Библиографическая ссылка
Иваненко В.И., Маслова М.В., Куншина Г.Б., Агафонов Д.В., Владимирова С.В. ПОЛУЧЕНИЕ И СВОЙСТВА АНОДНОГО МАТЕРИАЛА НА ОСНОВЕ ЛЕГИРОВАННОГО ЛАНТАНОМ (III) ТИТАНАТА ЛИТИЯ // Фундаментальные исследования. 2018. № 12-1. С. 15-19;URL: https://fundamental-research.ru/en/article/view?id=42344 (дата обращения: 23.04.2026).
DOI: https://doi.org/10.17513/fr.42344



