Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE RESEARCH OF INFLUENCE OF BLOOD COMPONENTS ON THE TYPE OF DISEASE ON BASIS OF CLINICAL BLOOD ANALYSIS BY THE METHODS OF STRUCTURED SYSTEMS OF SYSTEMOLOGY
Системный подход распространился во многие научные сферы, и медицина не является исключением. Его применение в медицине сопряжено с рядом трудностей, связанных со сложной организацией, слабой структурированностью, недостаточной формализованостью и уникальностью биологических систем, все элементы которых тесно взаимосвязаны. Математические методы исследования биосистем должны предоставлять гибкость для анализа большого класса систем, учитывать их особенности, позволять выявить наиболее значимые элементы системы, корректировать и прогнозировать поведение системы. Зачастую статистические методы не справляются с решением поставленных задач, особенно в тех случаях, когда закономерности функционирования систем неизвестны и моделирование систем затруднено. На сегодняшний день сложилась ситуация, в которой математические модели подходят только для конкретных систем или небольшого класса систем, а системы поддержки принятия решений осуществляют поддержку в конкретной области знаний.
Методологический подход, направленный на разработку математических методов и моделей, общих для систем различной природы, реализует системология Дж. Клира, в частности методы структурированных систем [3]. Исследование системологии Дж. Клира показало, что методы структурированных систем обладают некоторыми недостатками [7, 8]. В рамках исследований, проводимых в ФГБОУ ВО КубГУ Т.И. Синельниковой, под руководством Н.А. Швецовой, методы структурированных систем были модифицированы, что сделало возможной их программную реализацию (свидетельство о государственной регистрации программы ЭВМ № 2015618132) и применение [5, 6, 9].
Человеческий организм – сложная биосистема, одной из подсистем которой является кроветворная система. Кроветворная система реагирует на изменения в организме количественными и качественными изменениями. Видом отражения хода пролиферации и дифференцировки клеток крови является клинический анализ крови – гемограмма. Благодаря анализу гемограммы может быть получена информация о функциональной системе кроветворения и о состоянии здоровья в целом.
Исследование имело целью показать, что количественные и качественные изменения компонентов крови указывают на определенный вид заболевания. Выбор формулировки «влияние компонентов крови на вид заболевания» подразумевает, что изначально неизвестно, имеется ли заболевание крови, и задача состоит в том, чтобы определить, как влияют качественные и количественные изменения компонентов крови, отраженные в гемограммах, на вид заболевания.
Исследование проводилось при помощи реконструктивного анализа данных гемограмм для больных хроническим лимфолейкозом (ХЛЛ) и эритремией.
Определим основные понятия системологии, используемые в данной работе.
Система объекта
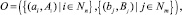 (1)
(1)
где ai – свойство; Ai – множество проявлений свойства; bj – база; Bj – множество элементов базы;
Nn = {1, 2, ..., n};
Nm = {1, 2, ..., m}.
Общая представляющая система I:
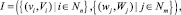 (2)
(2)
где vi – абстрактное значение конкретного свойства; Vi – обобщенное множество состояний абстрактной переменной; wj – абстрактное значение элемента базы; Wj – обобщенное множество базы;
Nn = {1, 2, ..., n};
Nm = {1, 2, ..., m}.
Система данных D:
D = (I, d), (3)
где d – функция, которая любому значению полного параметра из множества W ставит в соответствие одно полное состояние переменных из множества V:
d:W → V, (4)
где W = W1×W2×...×Wm;
V = V1×V2×...×Vn.
Структурированная система представляет собой набор систем данных, полученный модифицированным методом структурирования систем.
Для вероятностных систем информационное расстояние выражается формулой
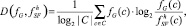 (5)
(5)
где fG(c), 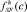 – значение вероятности для состояния c ∈ C в полной системе G и в реконструкции полной системы, полученной из гипотезы SF, соответственно; fG, – соответствующие распределения вероятности;
– значение вероятности для состояния c ∈ C в полной системе G и в реконструкции полной системы, полученной из гипотезы SF, соответственно; fG, – соответствующие распределения вероятности; 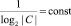 – нормирующий коэффициент, благодаря которому информационное расстояние обладает свойством
– нормирующий коэффициент, благодаря которому информационное расстояние обладает свойством
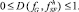
Исследовались данные гемограмм, предоставленные ГБУЗ «Клинический онкологический диспансер № 1» министерства здравоохранения Краснодарского края в рамках договора о научно-техническом сотрудничестве между ФГБОУ ВПО КубГУ и ГБУЗ «Клинический онкологический диспансер № 1» МЗ КК. Гемограммы исследуемой группы больных содержали данные о десяти компонентах крови, при этом данные о MPV (среднем объеме тромбоцита), СОЭ (скорости оседания эритроцитов) и лимфоцитах фактически не были в них представлены, и эти компоненты крови из рассмотрения были исключены. По этой причине исследовалась система объекта
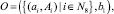 (6)
(6)
где a1 – заболевание; a2 – RBC (эритроциты); a3 – MCV (средний объем эритроцита); a4 – PLT (тромбоциты); a5 – WBC (лейкоциты); a6 – HGB (гемоглобин); a7 – MCH (среднее содержание гемоглобина в отдельном эритроците); a8 – MCHC (средняя концентрация гемоглобина в эритроцитарной массе); b1 – дата сдачи клинического анализа.
Для перехода к обобщенной представляющей системе I было принято следующее обобщенное множество состояний абстрактных переменных:
Заболевание: A1 = {ХЛЛ; эритремия}; V1 = {0, 1};
RBC: A2 = {[0, 4]; (4, 5], (5, 6], (6, 7], (7, 2000]}; V2 = {0, 1, 2, 3, 4};
MCV: A3 = {[0, 65]; (65, 75], (75, 85], (85, 95], (95, 2000]}; V3 = {0, 1, 2, 3, 4};
PLT: A4 = {[0, 100]; (100, 200], (200, 300], (300, 400], (400, 2000]}; V4 = {0, 1, 2, 3, 4};
WBC: A5 = {[0, 5]; (5, 10], (10, 15], (15, 20], (20, 2000]}; V5 = {0, 1, 2, 3, 4};
HGB: A6 = {[0, 12]; (12, 14], (14, 16], (16, 18], (18, 2000]}; V6 = {0, 1, 2, 3, 4};
MCH: A7 = {[0, 10]; (10, 20], (20, 30], (30, 40], (40, 2000]}; V7 = {0, 1, 2, 3, 4};
MCHC: A8 = {[0, 200]; (200, 250], (250, 300], (300, 350], (350, 2000]}; V8 = {0, 1, 2, 3, 4}.
Таблица 1
Результат реконструктивного анализа для 35 исходных систем
|
Номер исходной системы |
V1 |
V2 |
V3 |
V4 |
Влияние на заболевание |
|
1 |
заболевание |
RBC |
MCV |
PLT |
заболевание <–> PLT |
|
2 |
заболевание |
RBC |
MCV |
WBC |
заболевание <–> MCV |
|
3 |
заболевание |
RBC |
MCV |
HGB |
заболевание <–> MCV |
|
4 |
заболевание |
RBC |
MCV |
MCH |
заболевание <–> MCV |
|
5 |
заболевание |
RBC |
MCV |
MCHC |
заболевание <–> MCV |
|
6 |
заболевание |
MCV |
PLT |
WBC |
заболевание <–> PLT |
|
7 |
заболевание |
MCV |
PLT |
HGB |
заболевание <–> PLT |
|
8 |
заболевание |
MCV |
PLT |
MCH |
заболевание <–> PLT |
|
9 |
заболевание |
MCV |
PLT |
MCHC |
заболевание <–> PLT |
|
10 |
заболевание |
PLT |
WBC |
RBC |
заболевание <–> PLT |
|
11 |
заболевание |
PLT |
WBC |
HGB |
заболевание <–> PLT |
|
12 |
заболевание |
PLT |
WBC |
MCH |
заболевание <–> PLT |
|
13 |
заболевание |
PLT |
WBC |
MCHC |
заболевание <–> PLT |
|
14 |
заболевание |
WBC |
HGB |
RBC |
заболевание <–> WBC |
|
15 |
заболевание |
WBC |
HGB |
MCV |
заболевание <–> WBC |
|
16 |
заболевание |
WBC |
HGB |
MCH |
заболевание <–> MCH |
|
17 |
заболевание |
WBC |
HGB |
MCHC |
заболевание <–> WBC |
|
18 |
заболевание |
HGB |
MCH |
RBC |
заболевание <–> HGB |
|
19 |
заболевание |
HGB |
MCH |
MCV |
заболевание <–> MCH |
|
20 |
заболевание |
HGB |
MCH |
PLT |
заболевание <–> PLT |
|
21 |
заболевание |
HGB |
MCH |
MCHC |
заболевание <–> MCH |
|
22 |
заболевание |
MCH |
MCHC |
RBC |
заболевание <–> MCH |
|
23 |
заболевание |
MCH |
MCHC |
MCV |
заболевание <–> MCV |
|
24 |
заболевание |
MCH |
MCHC |
PLT |
заболевание <–> PLT |
|
25 |
заболевание |
MCH |
MCHC |
WBC |
заболевание <–> WBC |
|
26 |
заболевание |
RBC |
PLT |
HGB |
заболевание <–> PLT |
|
27 |
заболевание |
RBC |
PLT |
MCH |
заболевание <–> PLT |
|
28 |
заболевание |
RBC |
PLT |
MCHC |
заболевание <–> PLT |
|
29 |
заболевание |
RBC |
WBC |
MCH |
заболевание <–> MCH |
|
30 |
заболевание |
RBC |
WBC |
MCHC |
заболевание <–> WBC |
|
31 |
заболевание |
RBC |
HGB |
MCHC |
заболевание <–> HGB |
|
32 |
заболевание |
MCV |
WBC |
MCH |
заболевание <–> MCV |
|
33 |
заболевание |
MCV |
WBC |
MCHC |
заболевание <–> MCV |
|
34 |
заболевание |
MCV |
HGB |
MCHC |
заболевание <–> MCV |
|
35 |
заболевание |
PLT |
HGB |
MCHC |
заболевание <–> PLT |
Для исследования влияния компонентов крови на вид заболевания были приняты следующие параметры структурирования: отклонение для информационных расстояний равное 15 % и погрешность реконструкции равная 0,000002.
Произведен реконструктивный анализ для 35 исходных систем. Результаты представлены в сводной таблице (табл. 1).
Таким образом, наиболее значимыми для дальнейшего исследования компонентами крови являются: PLT (в 15 исходных системах), MCV (в 8 исходных системах), WBC (в 5 исходных системах), MCH (в 5 исходных системах). Компонент HGB (в 2 исходных системах) оказывает значительно меньшее влияние.
Проводился реконструктивный анализ методом структурированных систем четырех исходных систем, содержащих сочетания установленных компонентов, это системы 6, 8, 12 и 32 (табл. 1). В трех из них наибольшую значимость показали компоненты PLT и MCV в оставшейся.
Чтобы определить, какой из них оказывает наибольшее влияние на заболевание, была исследована соответствующая трехкомпонентная исходная система (Заболевание; MCV; PLT). Реконструктивный анализ и данные об информационных расстояниях для реконструктивных гипотез показали, что на вид заболевания у исследуемой группы наибольшее влияние оказывает компонент крови PLT (тромбоциты).
Таблица 2
Информационные расстояния заключительного реконструктивного анализа
|
Степень уточнения |
Наборы |
Расстояния |
|
2 |
12 / 13 / 23 |
0,001600 |
|
3 |
12 / 13 |
0,017030 |
|
3 |
12 / 23 |
0,036180 |
|
3 |
13 / 23 |
0,009720 |
|
4 |
13 / 2 |
0,037430 |
|
5 |
1 / 2 / 3 |
0,096530 |
Примечание. Элементы системы:
V1 – заболевание,
V2 – MCV (средний объем эритроцита),
V3 – PLT (тромбоциты).
Курсивом в табл. 2 отмечены реконструктивные гипотезы с минимальным информационным расстоянием от исходной системы.
Жирным шрифтом в табл. 2 обозначена ключевая реконструктивная гипотеза, указывающая на имеющееся влияние.
После анализа гемограмм для исследуемой группы больных методами структурированных систем показано, что уровень тромбоцитов оказывает наибольшее влияние на тип заболевания, в то время как значение среднего объема эритроцитов влияет значительно меньше.
Если выделить из имеющихся в гемограммах данных этот элемент, получим, что
при хроническом лимфолейкозе:
PLT со значением меньше 100•109 кл/л встречается в 57 гемограммах,
от 100 до 200•109 кл/л встречается в 86 гемограммах,
от 200 до 300•109 кл/л встречается в 5 гемограммах,
от 300 до 400•109 кл/л встречается в 1 гемограмме,
более 400•109 кл/л встречается в 4 гемограммах;
при эритремии:
PLT со значением меньше 100•109 кл/л встречается в 10 гемограммах,
от 100 до 200•109 кл/л встречается в 6 гемограммах,
от 200 до 300•109 кл/л встречается в 14 гемограммах,
от 300 до 400•109 кл/л встречается в 25 гемограммах,
более 400•109 кл/л встречается в 83 гемограммах.
Следовательно, для хронического лимфолейкоза характерно снижение уровня тромбоцитов относительно нормы [4] и для исследуемой группы его наиболее вероятное значение попадает в интервал от 100 до 200•109 кл/л. Для эритремии характерно повышение уровня тромбоцитов относительно нормы [4] и для исследуемой группы его наиболее вероятное значение превышает 400•109 кл/л.
Полученные выводы не противоречат выводам, полученным в медицине [1, 2]. Более того, получена новая информация о том, что наибольшее влияние на вид заболевания среди компонентов, указанных в гемограммах исследуемой группы, оказывает уровень тромбоцитов – PLT.
Библиографическая ссылка
Синельникова Т.И., Швецова Н.А., Онищук С.А. ИССЛЕДОВАНИЕ ВЛИЯНИЯ КОМПОНЕНТОВ КРОВИ НА ВИД ЗАБОЛЕВАНИЯ НА ОСНОВЕ КЛИНИЧЕСКОГО АНАЛИЗА КРОВИ МЕТОДАМИ СТРУКТУРИРОВАННЫХ СИСТЕМ СИСТЕМОЛОГИИ // Фундаментальные исследования. 2016. № 10-3. С. 566-570;URL: https://fundamental-research.ru/en/article/view?id=40896 (дата обращения: 05.05.2026).



