При протонировании 1,3-диоксанов - ценных в практическом отношении кислородсодержащих гетероаналогов циклогексана, – а также других 1,3- и 1,3,2-гетероциклов образуются циклические оксониевые ионы. Последние являются интермедиатами в многочисленных гетеролитических реакциях, катализируемых кислотами, в результате которых образуются сложные эфиры, 1,3-диолы, 5,6-дигидро-1,3-оксазины и другие ценные продукты органического и нефтехимического синтеза [1,2]. Вместе с тем в условиях эксперимента оксониевые ионы можно обнаружить лишь при температурах ниже -500С, что затрудняет использование физико-химических методов для определения тонких особенностей их структуры. В этой связи весьма актуальным становится изучение строения и конформационного поведения данных частиц с помощью квантово-химических методов. В частности, указанный подход оказался весьма плодотворным при анализе механизмов реакций 1,3-диоксанов и 1,3-диокса-2-гетероциклогексанов с нитрилами, где циклические оксониевые ионы образуются уже на первой стадии реакции [2-5].
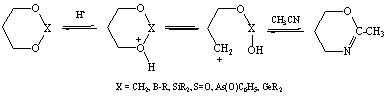
Полученные данные выявили необходимость оценки относительной стабильности протонированных форм замещенных 1,3-диоксанов, литературные сведения о которых весьма фрагментарны [6,7]. В этой связи целью настоящей работы является исследование минимумов на поверхности потенциальной энергии (ППЭ) оксониевых ионов 4-фенил-1,3-диок сана 1 и 2 с помощью полуэмпирического (АМ1) и неэмпирического (HF//STO-3G) методов в рамках программного обеспечения HyperChem [8].
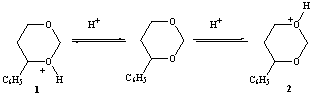
Известно [9,10], что наиболее стабильными минимумами на ППЭ самого 4-фенил-1,3-диоксана являются конформеры кресла с экваториальной (Ке - главный минимум) и аксиальной (Ка) ориентацией фенильного заместителя. В этой связи для оксониевых ионов 1 и 2 возможно существование восьми различных конформеров кресла (1а-б, 1а*-б*, 2a-б, 2а*-б*). Они могут превращаться друг в друга через промежуточные формы: 1,4-твист 3а-б и 4а-б, - также отвечающие минимумам на ППЭ. Относительные энергии всех рассматриваемых конформеров представлены в таблице.
Таблица 1. Относительная стабильность оксониевых ионов 1-4 (ккал/моль)
| Методы | 1a | 1a* | 3a | 1б | 1б* | 3б | 2а | 2а* | 4а | 2б | 2б* | 4б |
| АМ1 | 0 | 5.3 | 2.1 | 3.3 | 4.2 | 3.1 | 6.0 | 3.7 | 8.7 | 4.9 | 10.9 | 10.9 |
| STO-3G | 0 | 5.1 | 4.4 | 3.8 | 1.4 | 2.9 | 5.1 | 8.4 | 9.0 | 7.2 | 6.9 | 10.2 |
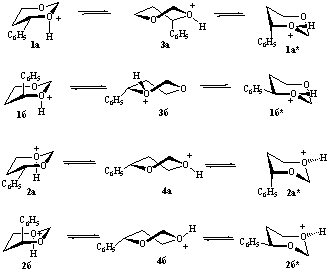
Полученные данные свидетельствуют об энергетической предпочтительности ио на 1а. Это соответствует ранее полученным результатам конформационного анализа оксониевого иона незамещенного 1,3-диоксана: наиболее устойчивым при прочих равных условиях является конформер с аксиальной ориентацией протона [7]. В нашем случае при наличии заместителей в кольце самым устойчивым является ион, несущий заряд на соседнем с замещенным углеродом атоме кислорода (1а по сравнению с 2а). Эти результаты согласуются с данными эксперимента о преимущественном раскрытии цикла 4-фенил-1,3-диоксана по связи С4-О3 в кислотно-катализи руемой реакции с нитрилами [2-5]..В то же время известно, что гидролиз, алкоголиз, а также реакции с тиолами и сероводородом протекают не столь однозначно [1].
Наиболее лабильны формы 2б*и 4б. Из остальных конформеров самыми устойчивыми являются 3а (АМ1) и 1б* (STO-3G). В этой связи представляет интерес оценить вероятность прямого внутримолекулярного протонного обмена между атомами кислорода кольца без изменения конформации цикла, то есть исследовать энергию активации равновесных процессов:
![]()
Результаты показывают, что первое из них проходит с относительно высоким активационным барьером:
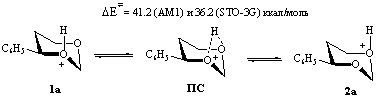
Учитывая, что само протонирование 1,3-диоксанов является практически безбарьерным [1,2], можно сделать вывод о малой вероятности протекания этого процесса даже при относительно небольшой концентрации протонов. Взаимопревращения 1а↔1б* [∆Е≠ = 8.0 (АМ1) и 3.1 ккал/моль (STO-3G)], а также 1а↔3а [[∆Е≠ = 3.1 (АМ1) и 6.9 ккал/моль (STO-3G)] и 3а↔1а* [∆Е≠ = 7.4 (АМ1) и 8.2 ккал/моль (STO-3G)] сравнимы по энергии и вполне могут конкурировать друг с другом. Можно предположить, что активационные барьеры остальных процессов: 1б↔1б*, 2а↔2а*и 2б↔2б* - практически не отличаются от установленных для превращения 1а↔1а*.В то же время результаты компьютерного моделирования свидетельствуют о невозможности прямого равновесия между формами 1а и 2б*.
Таким образом, детальный анализ конформационных превращений оксониевых ионов 1 и 2, образующихся на начальной стадии гетеролитических реакций, указывает на возможность неоднозначного раскрытия кольца 4-фенил-1,3-диоксана в кислотно-катализируемых процессах.
СПИСОК ЛИТЕРАТУРЫ:
- Итоги науки и техники. Технология органических веществ. Т.5. Химия и технология 1,3-диоксациклоалканов / Д.Л. Рахманкулов, Р.А. Караханов, С.С. Злотский и др. // М.: ВИНИТИ, 1979. - 288 с.
- Кузнецов В.В. Автореф. дисс. докт. хим. наук. – Уфа, 2002. – 47 с.
- Кузнецов В.В. // Журн. орг. химии. – 2000. - Т.36, вып. 7. - С.1097-1098.
- Кузнецов В.В. // Теорет. эксперим. химия. - 2000. - Т.36, № 3. - С.159-161.
- Кузнецов В.В. // Изв. АН. Сер. хим. – 2005. - № 7. – С.1499-1507.
- Курамшина А.Е., Мазитова Е.Г., Кузнецов В.В. // Современные наукоемкие технологии – 2006. - №2. – с.80-82.
- Мазитова Е.Г., Курамшина А.Е., Кузнецов В.В. // Журн. орг. химии. – 2004. – Т.40, вып.4. – С.615-616.
- HyperChem 5.02. Trial version. www.hyper.com.
- Кузнецов В.В., Цеплин Е.Е., Хвостенко О.Г. // ХХ Укр. конф. по орг. химии. Тез. докладов. Одесса, Астропринт, 2004. – Ч.1. – С.236.
- Внутреннее вращение молекул / под ред. В.Дж. Орвилл-Томаса. М.: Мир, 1975. – С.355.



