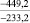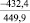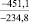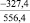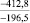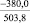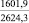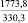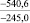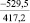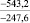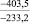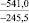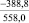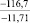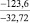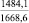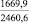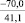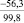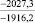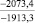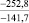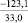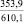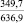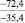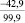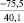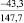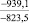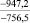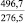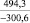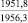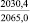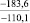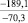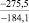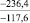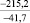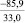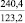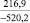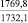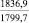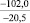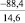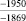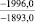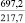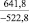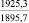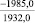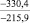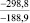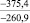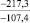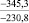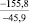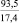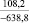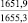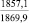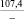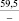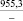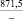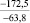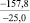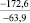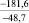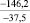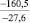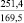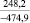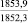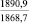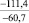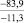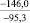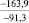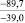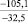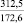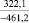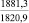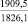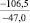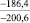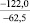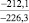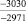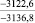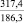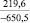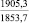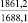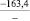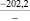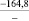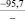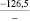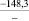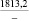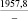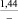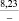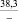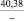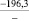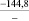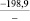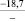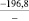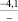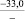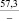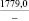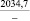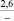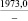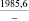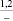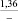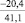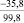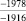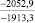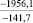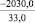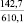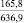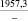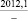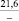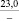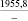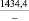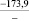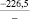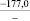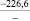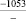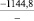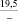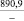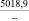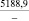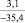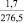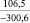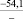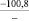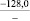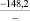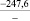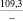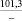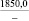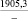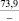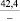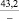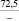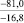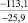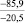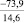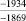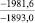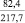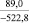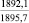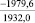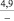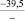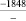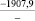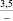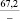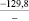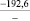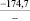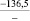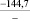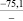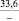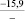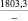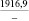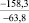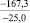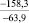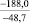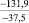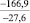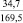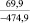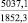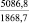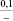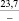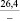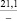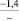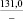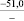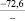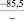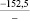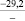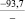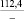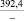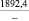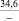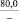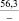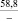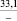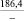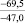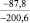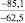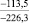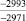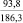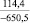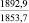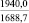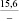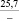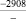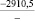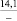Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE CHOICE OF FILLER FOR OBTAINING CHEMICALLY RESISTANT COMPOSITE ON THE BASIS OF SULFUR BINDER
Одной из приоритетных задач строительного материаловедения является проблема выбора и принятия решений. Поэтому при проведении системного анализа осуществляется формирование множества возможных способов достижения поставленной цели, то есть генерируется множество альтернатив, из которых осуществляется выбор. В настоящей работе с применением основных законов термодинамики научно обоснован выбор наполнителя для получения коррозионно-стойких серных композиционных материалов.
Серные композиционные материалы относятся к специальным видам композиционных материалов, при изготовлении которых в качестве вяжущего используются сера и серосодержащие отходы. Получают серные композиты путём смешения расплавленной серы с наполнителем, заполнителями и специальными добавками.
К положительным свойствам серных композиционных материалов относятся: технологичность серобетонных и растворных смесей; быстрый набор прочности, связанный только с периодом остывания и кристаллизации серы; относительно высокая прочность; стойкость к действию агрессивных сред, особенно к действию солевой и кислотной агрессии; низкое водопоглощение и, следовательно, высокая морозо- и водостойкость.
Серные композиты целесообразно использовать для изготовления конструкций, в период эксплуатации которых предъявляются повышенные требования по стойкости в агрессивных средах, морозо- и атмосферостойкости, проницаемости. К таким конструкциям относятся: элементы дорожных покрытий (тротуарные плитки, торцовые шашки, бортовые камни, дорожные ограждения), конструкции, подверженные солевой агрессии (полы, сливные лотки, фундаменты), инженерные сооружения (коллекторные кольца, канализационные трубы, очистные сооружения), футеровочные блоки.
Технологические, физико-механические и эксплуатационные свойства серных композиционных материалов (конечного продукта) зависят от различных рецептурно-технологических факторов, изменяя которые, можно получить материал с заданным комплексом необходимых свойств.
В теории композиционных материалов установлено, что на свойства композитов значительное влияние оказывают вид, дисперсность и количество наполнителя [2]. Зависимости структурно-чувствительных свойств композита от указанных факторов в большинстве случаев имеют экстремальный характер.
Для получения химически стойкого композита на основе серного вяжущего целесообразно использовать компоненты, которые являются устойчивыми в эксплуатационных средах. При этом высокой стойкостью должны обладать не только основные ингредиенты, но и соединения, образующиеся на границе раздела фаз.
Большинство породообразующих минералов, а также наиболее распространенные соединения, входящие в состав минералов, являются по отношению к сере химически активными, что во многих случаях приводит к образованию растворимых веществ, снижающих показатели эксплуатационных свойств. К химически активным наполнителям относятся вещества, которые способны вступать в химическое взаимодействие с вяжущим, в данном случае – серой, с образованием на границе раздела фаз «дисперсионная среда - дисперсная фаза» соединений различного состава. В результате образующиеся соединения оказывают значительное влияние на процессы формирования структуры материала и его физико-механические и эксплуатационные свойства.
В настоящей работе выбор наполнителя для изготовления серных композиционных материалов, стойких в различных средах, осуществляли с применением критериального подхода [1]. В качестве критерия использовали значение изобарно-изотермического потенциала (энергия Гиббса), рассчитываемого известными методами химической термодинамики. Термодинамический подход позволяет определить возможность протекания химического процесса. На практике в качестве критерия для оценки направленности процесса используют изобарно-изотермический потенциал ΔG:
ΔG = ΔH – TΔS,
где ΔH – энтальпия процесса; ΔS – энтропия процесса; T – температура.
Изменение энтальпии DН и энтропии ΔS реакции согласно закону Гесса (первое следствие из закона Гесса) равны [7]:
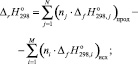
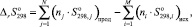
где 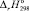 – стандартный тепловой эффект реакции при 298 К;
– стандартный тепловой эффект реакции при 298 К; 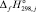 и
и 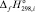 – стандартные тепловые эффекты образования продуктов реакции и исходных веществ соответственно;
– стандартные тепловые эффекты образования продуктов реакции и исходных веществ соответственно; 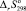 – энтропия реакции при 298 К;
– энтропия реакции при 298 К; 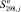 и
и 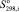 – стандартные энтропии образования продуктов реакции и исходных веществ соответственно; nj и ni – количество вещества продуктов реакции и исходных веществ соответственно.
– стандартные энтропии образования продуктов реакции и исходных веществ соответственно; nj и ni – количество вещества продуктов реакции и исходных веществ соответственно.
Тепловой эффект реакции при другой температуре (отличной от стандартной) согласно закону Кирхгофа равен
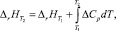
где 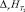 и
и 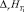 – тепловые эффекты реакции при Т2 и Т1 соответственно; ΔCp – изменение теплоёмкости системы реагирующих веществ в конечном и начальном состоянии.
– тепловые эффекты реакции при Т2 и Т1 соответственно; ΔCp – изменение теплоёмкости системы реагирующих веществ в конечном и начальном состоянии.
При расчёте ΔG возможны следующие варианты:
1) ΔG < 0;
2) ΔG = 0;
3) ΔG > 0.
Первый вариант означает, что при данных условиях (температуре, давлении, концентрации и т.д.) возможно самопроизвольное протекание исследуемого процесса. Второй вариант – созданных внешних условий недостаточно для проведения процесса, система находится в состоянии равновесия. Третий вариант – при данных условиях протекание процесса невозможно.
В данной работе термодинамический подход использовался для оценки возможности следующих химических взаимодействий:
1) между наполнителем и серой в процессе приготовления материала;
2) между наполнителем и агрессивной средой в процессе эксплуатации материала;
3) между сульфидами, образующимися на границе раздела фаз «сера - наполнитель», и агрессивной средой.
По результатам термодинамического анализа, которому были подвергнуты основные породообразующие минералы, а также наиболее распространенные соединения, входящие в состав минералов, осуществляли выбор дисперсной фазы (табл. 1). Основным критерием выбора наполнителя являлась его химическая инертность к взаимодействию с серой и к действию различных кислот и солей (для проведения расчетов и исследований были выбраны самые распространенные в промышленности кислоты и соли: соляная, серная и азотная кислоты, хлорид натрия и сульфат магния).
Таблица 1
Результаты термодинамических расчётов*
|
Компонент наполнителя |
Энергия Гиббса, кДж/моль |
||||||||||
|
Образование сульфида при температуре изготовления (Т = 160 °С) |
Эксплуатационные среды |
||||||||||
|
кислоты |
соли |
||||||||||
|
соляная |
серная |
азотная |
хлорид натрия |
сульфат магния |
|||||||
|
T = 25 °C |
T = 50 °C |
T = 25 °C |
T = 50 °C |
T = 25 °C |
T = 50 °C |
T = 25 °C |
T = 50 °C |
T = 25 °C |
T = 50 °C |
||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
Оксиды |
|||||||||||
|
NaO |
–287,9 |
|
|
|
|
|
|
– |
– |
|
|
|
K2O |
–499,3 |
|
|
|
|
|
|
|
|
|
|
|
MgO |
–161,7 |
|
|
|
|
|
|
|
|
– |
– |
|
CuO |
–162,2 |
|
|
|
|
|
|
|
|
|
|
|
CaO |
–66,3 |
|
|
|
|
|
|
|
|
|
|
|
ZnO |
–81,5 |
|
|
|
|
|
|
|
|
|
|
|
BaO |
–146,8 |
|
|
|
|
|
|
|
|
|
|
|
SiO2 |
302,3 |
|
|
– |
– |
– |
– |
|
|
– |
– |
|
PbO |
–108,6 |
|
|
|
|
|
|
|
|
|
|
|
MnO |
–21,1 |
|
|
|
|
|
|
|
|
|
|
|
FeO |
–36,92 |
|
|
|
|
|
|
|
|
|
|
|
Соли |
|||||||||||
|
Na2CO3 |
193,0 |
|
|
|
|
|
|
– |
– |
|
|
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
Na2SO4** |
242,4 |
|
|
– |
– |
|
|
– |
– |
– |
– |
|
K2CO3 |
149,7 |
|
|
|
|
|
|
|
|
|
|
|
K2SO4** |
256,3 |
|
|
– |
– |
|
|
|
|
– |
– |
|
MgCO3 |
–92,5 |
|
|
|
|
|
|
|
|
– |
– |
|
MgSO4** |
1915,7 |
|
|
– |
– |
|
|
|
|
– |
– |
|
CuCO3 |
680,5 |
|
|
|
|
|
|
|
|
|
|
|
CuSO4 |
–45,2 |
|
|
– |
– |
|
|
|
|
– |
– |
|
CaCO3 |
148,7 |
|
|
|
|
|
|
|
|
|
|
|
CaSO4 |
184,0 |
|
|
– |
– |
|
|
|
|
– |
– |
|
ZnCO3 |
–97,2 |
|
|
|
|
|
|
|
|
|
|
|
ZnSO4 |
22,8 |
|
|
– |
– |
|
|
|
|
– |
– |
|
BaCO3 |
207,9 |
|
|
|
|
|
|
|
|
|
|
|
PbCO3 |
–66,8 |
|
|
|
|
|
|
|
|
|
|
|
PbSO4 |
77,4 |
|
|
– |
– |
|
|
|
|
– |
– |
|
MnCO3 |
49,2 |
|
|
|
|
|
|
|
|
|
|
|
MnSO4** |
93,3 |
|
|
– |
– |
|
|
|
|
– |
– |
|
FeCO3 |
–10,6 |
|
|
|
|
|
|
|
|
|
|
|
FeSO4 |
61,4 |
|
|
– |
– |
|
|
|
|
– |
– |
Примечания: в числителе – значения энергии Гиббса для процесса взаимодействия наполнителя с агрессивной средой; в знаменателе – то же для процесса взаимодействия сульфидов, образующихся на границе раздела фаз «сера – наполнитель», с агрессивной средой; * – значения термодинамических величин взяты из справочной литературы [3…6]; ** – применение наполнителя возможно только после экспериментальной проверки в разбавленных растворах указанных солей и кислот.
Из анализа табл. 1 видно, что для изготовления серных материалов, стойких в растворах различных кислот и солей, целесообразно использовать кварцсодержащие наполнители (андезит, опоку, диабаз, кварц и др.), а также сульфаты натрия, калия, магния, кальция и марганца. Эти наполнители инертны к действию серы и агрессивных сред, на что указывает изобарно-изотермический потенциал (ΔG > 0).
Известно, что сульфаты натрия, калия, магния и марганца являются растворимыми в воде, поэтому их применение возможно только после экспериментальной проверки в разбавленных растворах указанных кислот и солей.
Поэтому в качестве наполнителя для изготовления химически стойких композитов на основе серного вяжущего предлагается использовать кварцевую муку с различной удельной поверхностью для установления оптимальных составов, полученную измельчением речного кварцевого песка (р. Сура). Кроме инертности, кварцевый песок является еще и доступным и широко распространенным сырьём в Пензенской области. Свойства данного наполнителя приведены в табл. 2.
Таблица 2
Характеристики кварцевого наполнителя (Мк = 1,4)
|
Средняя удельная поверхность, м2/кг |
Плотность, кг/м3 |
|
|
насыпная |
средняя |
|
|
180 |
1230 ± 20 |
2620 ± 20 |
|
300 |
960 ± 5 |
|
|
420 |
885 ± 10 |
|
Библиографическая ссылка
Самошина Е.Н., Шитова И.Ю. ВЫБОР НАПОЛНИТЕЛЯ ДЛЯ ПОЛУЧЕНИЯ ХИМИЧЕСКИ СТОЙКОГО КОМПОЗИТА НА ОСНОВЕ СЕРНОГО ВЯЖУЩЕГО // Фундаментальные исследования. 2016. № 4-1. С. 107-111;URL: https://fundamental-research.ru/en/article/view?id=40135 (дата обращения: 07.05.2026).