Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
ASSESSMENT OF TYPE INLET VALVE AND THE ANGLE OF ITS ORIENTATION ON HEMODYNAMIC SYSTEM PERFORMANCE CIRCULATORY SUPPORT PULSATING TYPE
Согласно данным статистики, ежегодно в России рождается около 10 000 детей с врожденными пороками сердца. На каждую 1000 новорожденных приходится 10 детей, которые нуждаются в операции на сердце. 50 % детей, не получивших вовремя оперативного лечения, умирают в возрасте до полугода. Еще 25 % детей, не получивших вовремя оперативного лечения, умирают до года [2]. Кроме того, уровень смертности детей в возрасте до 18 лет, находящихся в «листе ожидания», в несколько раз выше, чем для других возрастных групп, в значительной степени из-за отсутствия механических систем поддержки кровообращения длительного применения.
В России системы вспомогательного кровообращения пульсирующего типа с успехом применяются в качестве «моста для трансплантации» у пациентов старших возрастных групп. Кроме того, при применении систем ВК пациенты показывают стабильную положительную динамику по восстановлению их ослабленных желудочков сердца («мост к восстановлению»), что подтверждает потенциальную возможность применения этих систем в педиатрии.
Однако тромбоз является одной из основных причин смерти при применении аппаратов ВК, и улучшение их гемодинамических показателей на стадии проектирования является важной задачей. Гемолиз и кальцификация могут быть также уменьшены надлежащим дизайном системы. Высокие касательные напряжения, турбулентность, разделение потока и наличие застойных зон должны быть минимизированы в процессе проектирования.
Процесс проектирования педиатрических систем ВК является более сложной задачей, чем прямое масштабирование существующих систем с большим объемом выброса [1] в сторону его уменьшения. Большое внимание при проектировании пульсирующих систем ВК уделяется клапанному аппарату, т.к. применение механических клапанов сердца (МКС) осложняется их склонностью к гемолизу и тромбообразованию. Общеизвестно, что наличие высоких касательных напряжений в потоке, проходящем через МКС, связано с уровнем гемолиза [1, 14]. Осложнения из-за свертываемости могут возникать из-за плохого омывания внутренних стенок и наличия продолжительных застойных зон в камере насоса крови. В связи с этим целью настоящего исследования является определение влияния типа клапана и его ориентации на гемодинамические показатели работы системы ВК на основании результатов CFD-моделирования.
Моделирование потока внутри камеры насоса крови (рис. 1) проводилось на основании реалистичной 3D модели камеры крови. Расчетная модель представляет собой внутренний объем камеры крови с учетом реальной геометрии основного тела, клапанов, радиусов и переходов.
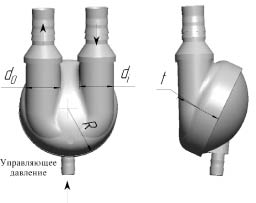
Рис. 1. Внешний вид системы ВК
Размеры насоса крови приведены в таблице.
Моделирование проводилось с двумя коммерчески доступными в России моделями механических клапанов сердца: двустворчатым модели «Мединж-2» (НПП МедИнж, Россия) [7] и одностворчатым модели «Микс» (ООО «Роскардиоинвест», Россия) [10]. Данные клапана имеют минимальный внешний диаметр – 17 мм, и площадь проходного отверстия 1,67 и 1,54 см2 соответственно (рис. 2).
Основные размеры системы ВК объемом 30 см3
|
Характеристики камеры системы ВК |
Размеры, мм |
|
Радиус камеры системы ВК (R) |
55 |
|
Диаметр митрального клапана (di) |
20 |
|
Диаметр выходного клапана (d0) |
20 |
|
Толщина камеры системы ВК (t) |
20 |


а б
Рис. 2. Примеры клапанов: а – одностворчатая модель «Микс»; б – двустворчатая модель «Мединж-2»
Начальная позиция митральных клапанов выбиралась следующим образом: дисковый клапан ориентировался таким образом, что его большая часть открывалась в сторону наружной стенки, а распорка была перпендикулярна диафрагме; двустворчатый клапан располагался таким образом, что открытые створки клапана были также перпендикулярны диафрагме. Поворот клапанов осуществлялся по часовой стрелке. Моделирование было проведено для положения клапанов 0, 30, 45 градусов. Положение аортального клапана не изменялось (рис. 3).
Движение клапанов не моделировалось. Они были фиксированы в полностью открытом или полностью закрытом положениях, в зависимости от фазы сердечного цикла. Во время фазы систолы аортальный клапан был открыт, а митральный клапан был закрыт, а во время диастолы митральный клапан открыт и аортальный клапан был закрыт.
Для решения уравнений Навье ? Стокса в нестационарной постановке использовалась система конечно-элементного анализа ANSYS Workbench (ANSYS, Inc., USA). Параметры конечно-элементной модели были следующими: количество узлов 298224, количество конечных элементов 1669390, вид элемента tetrahedral, минимальная длина ребра 10–5 мм, максимальная длина ребра 7·10–4. Для получения более точного решения разбиение происходило с учетом геометрической сложности объема. В зонах клапана, патрубка, входа в камеру насоса крови выполнено сгущение сетки. Кровь моделировалась как ламинарная, несжимаемая Ньютоновская жидкость с плотностью 1060 кг/м3 и динамической вязкостью 0,0032 Па·с. Объем ударного выброса системы составляет 30 мл. Частота сердечных сокращений – 75 уд/мин. В этом исследовании, K (кинетическая энергия турбулентности) – E (вязкая скорость диссипации) модель турбулентности была выбрана, чтобы решить дополнительные напряжений Рейнольдса терминов из усреднения по времени процедуру для уравнений Навье – Стокса, которая была использована в наших предыдущих исследованиях и другими исследовательскими группами для CFD-моделирования пульсирующих и непульсирующих систем [4, 8, 9, 12, 13]. Временные интервалы фаз диастолы и систолы были приняты одинаковыми, а именно 0,4 с. В процессе решения интервал разбивался на 200 шагов. Со стороны мембраны задавалось изменение управляющего давления, деформация стенок не учитывалась. Моделирование было проведено при условии отсутствия скольжения на границе.
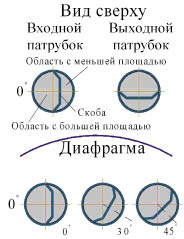
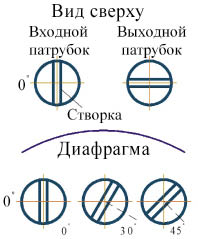
Рис. 3. Примеры расположения клапанов при моделировании
Все расчеты проводились на ПК с ОС Windows с процессором Pentium i5 процессором 2,9 ГГц, 24 Гб оперативной памяти требует 2 часа для решения данной задачи. Моделированием оценивали гемодинамические параметры, такие как скорость и давление потока внутри насосной камеры, и сдвиговые напряжения Рейнольдса. Результаты моделирования обрабатывались в постпроцессоре CFX-Post.
Выводы
Наибольший интерес представляют результаты моделирования, отображающие изменение скоростных потоков в кровяной камере системы ВК. Их анализ позволяет сделать предварительные выводы о наличии застойных зон, локальных зон закручивания и отрыва потока. Результаты представлены в виде векторных диаграмм. На диаграммах цветом показана величина изменения скорости, а стрелки указывают направление движения потока.
Для оценки влияния типа митрального клапана и угла его ориентации на поведение потоков внутри кровяной камеры системы ВК проведено сравнение полей скоростей в фазу диастолы (рис. 1). При использовании дискового клапана «МИКС наблюдается минимальное число зон с низкими значениями скорости потока. Так же размер самих зон значительно меньше, чем при использовании двустворчатого клапана «МедИнж-2». При установке дискового клапана под углом 45 градусов наблюдается практически полное отсутствие зон с низким значением скорости потока. Максимальная скорость потока наблюдается при его прохождении через клапан и снижается, попадая в камеру крови. Установка клапана под указанным углом обеспечивает максимальное омывание внутренних стенок камеры крови за счет «направления» входящего потока на стенку камеры. При использовании клапана «МИКС», установленного под 45 градусов, наблюдается максимальный эффект закручивания потока жидкости внутри камеры крови в сторону противоположного патрубка.
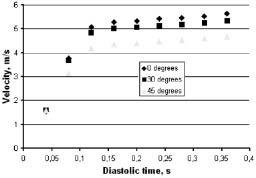
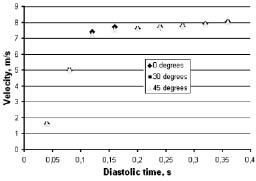
Рис. 4. Изменение максимальной скорости в фазу диастолы: слева для одностворчатого клапана «МИКС»; справа для двустворчатого клапана «МедИнж-2»
Изменение скорости потока в фазу диастолы для дискового клапана «МИКС», расположенного под 45 градусов, представлено на рис. 2. Значения максимальной скорости в фазу диастолы для заданных положений дискового клапана «МИКС» составляют 5,63; 5,32 и 4,67 м/с соответственно. Большие скорости характерны для двустворчатого клапана «МедИнж-2» – 8,04; 8,06; 8,02 м/с, однако их значения не изменяются при изменении угла поворота клапана (рис. 3). В фазу диастолы скорость достигает максимального значения в конце фазы. В начале фазы диастолы наблюдается резкое возрастание скорости потока, но к 0,1 секунде фазы диастолы значение выравнивается и до конца цикла меняется незначительно. Ориентации дискового клапана под углом в 45 градусов соответствуют меньшие значения скорости потока.
Изменение скорости потока в конце фазы систолы показано на рис. 4. Максимальное значение скорости наблюдается при движении жидкости через клапан. Большее значение характерно для дискового клапана «МИКС», чем для двустворчатого клапана «МедИнж-2».
Большие скорости сдвига наблюдаются при использовании дискового клапана «МИКС». В начале фазы диастолы наблюдается нарастание скорости сдвига, но уже на 0,1 секунде фазы они выравниваются и изменяются незначительно. При использовании двустворчатого клапана «МедИнж-2» диапазон скоростей сдвига является одинаковым для всех угловых положений клапана.
Исследование выполнено при финансовой поддержке гранта Президента Российской Федерации для государственной поддержки молодых ученых в рамках проекта МК-5860.2015.8 «Разработка теоретических основ и алгоритмов прогнозирования гемодинамических параметров систем вспомогательного кровообращения и искусственного сердца пульсирующего типа на базе мехатронных модулей»
Рецензенты:
Гоц А.Н., д.т.н., профессор кафедры тепловых двигателей и энергетических установок, ФГБОУ ВПО «Владимирский государственный университет имени Александра Григорьевича и Николая Григорьевича Столетовых», г. Владимир;
Житников Б.Ю., д.т.н., профессор ка федры специальной техники и информационных технологий, ФКОУ ВПО «Владимирский юридический институт Федеральной службы исполнения наказаний» России, г. Владимир.
Библиографическая ссылка
Беляев Л.В., Жданов А.В., Волкова И.В. ОЦЕНКА ВЛИЯНИЯ ТИПА ВХОДНОГО КЛАПАНА И УГЛА ЕГО ОРИЕНТАЦИИ НА ГЕМОДИНАМИЧЕСКИЕ ПОКАЗАТЕЛИ РАБОТЫ СИСТЕМЫ ВСПОМОГАТЕЛЬНОГО КРОВООБРАЩЕНИЯ ПУЛЬСИРУЮЩЕГО ТИПА // Фундаментальные исследования. 2015. № 11-4. С. 654-658;URL: https://fundamental-research.ru/en/article/view?id=39480 (дата обращения: 12.05.2026).



