Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
FEATURES MICROBIOCENOSIS SKIN AND MUCOUS MEMBRANES OF UPPER RESPIRATORY TRACT IN PATIENTS WITH ATOPIC DERMATITIS
Атопический дерматит (АД) – хроническое воспалительное заболевание кожи, которое поражает до 25 % детей и 1–3 % взрослых во всем мире и негативно отражается на качестве жизни пациентов [7]. Патогенез АД имеет мультифакториальную природу, включающую взаимодействие между генетической предрасположенностью, дисфункцией эпидермального барьера, нарушением врожденного и приобретенного иммунитета и влиянием факторов окружающей среды, что приводит к выраженному воспалению, интенсивному зуду, проникновению аллергенов и предрасполагает к развитию вторичных инфекций на коже, вызванных бактериальными, вирусными и грибковыми агентами [1,7].
Основными представителями нормальной микрофлоры на коже человека являются грамм-положительные бактерии, представленные Staphylococcusspp., микрококками и коринебактериями. Грамотрицательные бактерии рода Acinetobacter встречаются редко и могут присутствовать в области крупных складок [6]. Видовой и количественный состав микробиоты кожи меняется со временем и зависит от локализации, местной температуры, влажности [3]. У больных АД видовой состав микробиоты кожи меняется в зависимости от стадии процесса (обострения или ремиссии) [5]. Кроме того, у больных АД снижена продукция кератиноцитами, антимикробных пептидов – кателицидинов (LL-37) и β-дефензинов (HBD – 1, 2, 3), дермицидинов экзокринными потовыми железами, которые обладают противомикробной и иммуномодулирующей активностью, что способствует снижению резистентных свойств кожи к микробной колонизации [4]. Наиболее значимая роль в развитии обострений, поддержании и утяжелении кожного процесса отводится S. aureus, который обнаруживается у 93 % с пораженной и у 76 % больных с непораженной кожей АД, а также способен колонизировать слизистую рото- и носоглотки [1, 2].
Целью исследования явилось изучение видового и количественного состава микрофлоры, выделяемой как с очагов пораженной кожи, так и с видимо здоровой кожи, потенциальных очагов носительства хронической инфекции (крупных складок, носоглотки) у больных АД в период обострения кожного процесса
Материалы и методы исследования
В клинике ФГБУ «Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии» Минздрава России (г. Екатеринбург) проведено обследование 90 больных АД в возрасте от 13 до 49 лет (средний возраст 26 (20; 31) лет). Из них 51 (56,7 %) – женского пола и 39 (43,3 %) – мужского. Клинически пациенты были распределены на 2 группы: I группа (n = 60) – больные тяжелым АД, осложненным вторичной бактериальной инфекцией (индекс SCORAD 67,2 (12,2) балла) и II группа (n = 30) – больные тяжелым АД, клинически не имеющих признаков вторичной инфекции(индекс SCORAD 64,2 (10,9) балла). Обе группы были сопоставимы по полу, возрасту, длительности заболевания и тяжести кожного процесса (р > 0,05).
Для изучения видового состава микрофлоры кожи производилось микробиологическое исследование, включающее забор материала стерильным ватным тампоном с пораженной, клинически непораженной кожи, крупных складок, полости носа и слизистой зева. Первичный посев производился на плотные дифференциально-диагностические питательные среды с последующим инкубированием материала в течение 24 часов при температуре 37 °С. После инкубирования отбирали изолированные колонии с учетом их морфологических особенностей при росте на питательных средах. Количественный анализ, показывающий диагностическую значимость выросших колоний, выражали вlg КОЕ/мл от среднего количества микроорганизмов. Идентификацию выросших суточных культур проводили методом времяпролетной масс-спектрометрии по технологии MALDI-TOFMS (BioMerieux, VITEK MS, France).Подготовку материала перед идентификацией микроорганизмов проводили согласно инструкции производителя. Интерпретация полученных результатов проводилась с использованием базы данных VITEK MS.
Анализ полученных данных производился в программах MicrosoftExcel 2007, MedCalc 15.2.2. Оценка характера распределения данных производилась с помощью критерия Шапиро-Уилка. Параметрические данные представлены в виде среднего и стандартного отклонения – M (SD), непараметрические данные в виде медианы и межквартильных интервалов – Me (LQ25; UQ75). При сравнении двух независимых групп, имеющих ненормальное распределение, использовался U-критерий Манна-Уитни. Анализ качественных данных проводился с помощью критерия χ2с поправкой Йейтса (при необходимости). Наличие связи между изучаемыми признаками и явлениями выборочных данных устанавливали с использованием коэффициентов ранговой корреляции Спирмена (rs). Статистически значимыми различия данных и корреляционных связей между признаками считали при р < 0,05.
Результаты исследования и их обсуждение
При анализе культурального исследования больных АД I группы с очага вторичной инфекции у 83,3 % больных, складок – у 80,0 % и с непораженной кожей – у 66,7 % чаще выделялся S. aureus, при этом в подавляющем числе случаев он был выделен в монокультуре. Рост S. aureus в ассоциации с другими условно-патогенными (УП) микроорганизмами (S. epidermidis, S. hominis, S. haemolyticus) в исследуемых локализациях отмечался у 13,3 % больных из очага вторичной инфекции, у 10,0 % с кожи складок, и у 18,3 % с непораженной кожей больных АДI группы. У одного больного наблюдался ассоциативный рост S. aureus и S. pyogenes. Рост другой УП флоры, представленный микроорганизмами семейств Streptococcaceae и Micrococcaceae, ассоциированных друг с другом или выделенных в монокультуре, чаще встречался у пациентов данной группы на непораженной коже (рис. 1).
Проведенный анализ культурального исследования больных АД II группы до лечения показал, что удельный вес S. aureus на пораженной коже составил 66,7 %, на коже складок 60,0 % был S. aureus, который в подавляющем большинстве также выделялся в монокультуре. На непораженной коже S. aureus встречался только в 43,3 %. Другие представители УП флоры, входящие в состав нормобиоты кожи (S. epidermidis, S. capitis, S. haemolyticus, C. aurimucosum) выделялись в монокультуре или в ассоциации из 2 вышеперечисленных видов у 40,0 % больных. Стоит отметить, что у 10,0–16,7 % больных не было отмечено роста флоры (рис. 2).
Изучение видового микробного пейзажа слизистых ЛОР-органов у больных I группы показал, что частота выделения S. aureus в исследуемом материале как со слизистой зева, так и со слизистой носа составляла 75,0 %. При этом со слизистой зева преобладал рост ассоциаций S. aureus с другой УП флорой (73,3 %), представленной резидентными и транзиторными видами (Neisseriaspp., alpha-hemolytic Streptococcus, R. mucilaginosa, C. albicans), а со слизистой носа чаще выделялись монокультуры S. aureus (58,3 %), и только в 20 % случаев со слизистой носа он выделялся в ассоциации с другой УПфлорой (S. epidermidis, Serratiamarcescens, C. pseudodiphtheriticum). Среди других УП микроорганизмов, полученных в исследуемом материале со слизистой зева, наиболее встречаемыми были резидентные бактерии рода Neisseria и alpha-hemolytic Streptococcus (S. viridians, S. salivariusи др.), которые, как правило, выделялись в ассоциации друг с другом (20,0 %). Со слизистой носа частота выделений монокультур других УП микроорганизмов, составила 18,3 % (S. epidermidis), а в ассоциации 6,7 % (рис. 3).
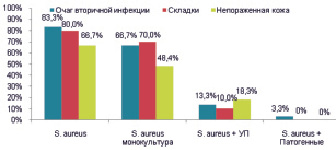
Рис. 1. Спектр выделенных микроорганизмов с кожи больных АД, осложненным вторичной инфекцией
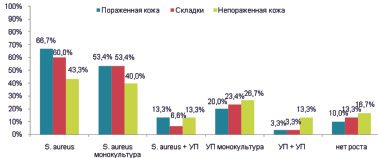
Рис. 2. Спектр выделенных микроорганизмов с кожи больных неосложненным АД
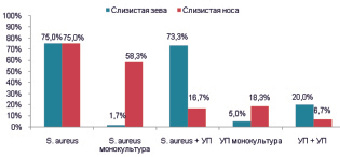
Рис. 3. Спектр выделенных микроорганизмов со слизистой ЛОР-органов больных АД, осложненным вторичной инфекцией
В отличие от I группы больных во II исследуемой группе, в микробиологическом материале со слизистой зева преобладал рост резидентных и транзиторных УП микроорганизмов (50,0 %) – Neisseriaspp., alpha-hemolytic Streptococcus (Str. viridans, Str. salivarius и др.), S. epidermidis, H. haemolyticus, Acinetobacterspp., H. alvei, C. albicans, которые были выделены в ассоциации у 36,7 % больных и в монокультуре у 13,3 % больных. S. Aureus был высеян только у 43,3 % больных, что в 1,6 раза меньше, чем у больных I группы (р < 0,05). У 1 (3,3 %) пациента был отмечен рост патогенной флоры (Histophylussomni). Со слизистой полости носа у больных АД II группы частота выделения культур S. aureus составила 63,3 %, причем у 46,6 % больных он был выделен в монокультуре. Кроме того, со слизистой носа был выделен большой спектр других УП бактерий (S. epidermidis, S. hominis, C. pseudodiphtheriticum, H. influenzae, K. pneumoniae, E. aerogenes, P. mirabilis, C. koseri) среди которых чаще всего встречался S. epidermidis (в 30,0 %). У 1 (3,3 %) больного не был получен рост в исследуемом материале. Значимых различий в частоте выделения S. aureus и другой УП на слизистой носа между группами установлено не было (рис. 4).

Рис. 4. Спектр выделенных микроорганизмов со слизистой ЛОР-органов больных неосложненным АД
При анализе видовой структуры выделенных микроорганизмов не было установлено значимых различий между группами в частоте выделения монокультур и ассоциаций, а также количестве выделенных изолятов. Отмечено, что удельный вес выделенных монокультур превалировал в очаге вторичной инфекции (в I группе), с пораженной кожи (во II группе), c кожи складок, непораженной кожи, а также со слизистой носа, тогда как при микробиологическом исследовании со слизистой зева наблюдалась противоположная картина, отражающая преобладание ассоциаций из 3 и более видов.
При анализе степени обсемененности S. Aureus у больных АД, осложненным вторичной инфекцией, отмечено, что плотность колонизации S. Aureus в очаге вторичной инфекции (7 (4; 9) lg КОЕ/мл), на коже складок (9 (4; 9) lg КОЕ/мл) и слизистой полости носа (7 (4; 9) lg КОЕ/мл) была статистически значимо выше, чем на непораженной коже (4 (4; 6,5) lgКОЕ/мл, р < 0,05) и на слизистой зева (4 (4; 6,5) lg КОЕ/мл, р < 0,05). Несмотря на более высокие медианные показатели плотности колонизации в очаге вторичной инфекции) и кожи складок у больных АД, осложненным вторичной инфекцией, по сравнению с больными с неосложненным АД не было установлено значимых различий между группами (р > 0,05).
Установлено, что увеличение плотности колонизации на пораженной коже у пациентов обеих групп сопровождается увеличением степени колонизации S. aureus на коже складок (rs = 0,646, р < 0,0001 для обеих групп), непораженной кожи (rs = 0,355, р = 0054 для обеих групп), слизистой носа (rs = 0,499, р < 0,0001 для обеих групп), зева (rs = 0,384, р = 0,0024 для обеих групп). У больных с осложненным АД установлена прямая дозозависимая реакция плотности колонизации S. aureus, выделенного с кожи складок (rs = 0,256, p = 0,0488), слизистой зева (rs = 0,265, p = 0,0411) и слизистой носа (rs = 0,259, p = 0,0456) и утяжелении кожного процесса, оцениваемого по индексу SCORAD.
Таким образом, анализ результатов культурального исследования показал, что типичным представителем микробной колонизации кожи больных АД независимо от наличия бактериального осложнения является S. aureus, который при микробиологическом обследовании в подавляющем большинстве случаев выделяется в монокультуре с пораженной кожи (с очага вторичной инфекции) у 53,4–66,7 %, с кожи складок у 53,4–70,0 %, с клинически непораженной кожи у 40,0–48,0 %, со слизистой носа у 46,6–58,3 %. Плотность колонизации S. aureus у больных АД, осложненным вторичной пиогенной инфекцией, значимо выше в очаге вторичной инфекции, чем на клинически непораженной коже. Увеличение плотности колонизации S. aureus на коже складок, слизистых зева и носа, рассматриваемых с позиции потенциальных очагов хронического носительства, утяжеляет течение кожного процесса.
Рецензенты:
Сырнева Т.А., д.м.н., профессор кафедры кожных и венерических болезней, ГБОУ ВПО «Уральский государственный медицинский университет» Минздрава здравоохранения Российской Федерации, г. Екатеринбург;
Евстигнеева Н.П., д.м.н., руководитель экспериментально-лабораторного отдела, ФГБУ «Уральский научно-исследовательский институт дерматовенерологии и иммунопатологии» Минздрава России, г. Екатеринбург.
Библиографическая ссылка
Стукова Е.И., Кохан М.М., Кениксфест Ю.В., Юровских Л.И. ОСОБЕННОСТИ МИКРОБИОЦЕНОЗА КОЖИ И СЛИЗИСТЫХ ЛОР-ОРГАНОВ У БОЛЬНЫХ АТОПИЧЕСКИМ ДЕРМАТИТОМ // Фундаментальные исследования. 2015. № 8-1. С. 42-46;URL: https://fundamental-research.ru/en/article/view?id=38843 (дата обращения: 27.04.2026).



