Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE INFLUENCE OF INDOLE-3-ACETIC ACID PRODUCING BACTERIA AZOTOBACTER CHROOCOCCUM 66 AND PSEUDOMONAS PUTIDA NBR9 ON THERMOTOLERANCE OF WHEAT SEEDLING (TRITICUM AESTIVUM L.)
Общепризнанно, что многие симбиотические бактерии, в частности представители родов Azotobacter и Pseudomonas, способны регулировать рост растений-хозяев посредством экскреции ряда биологически активных веществ, прежде всего индол-3-уксусной кислоты (ИУК), а также фиксации атмосферного азота [5, 9]. Создание высокоэффективных биопрепаратов с использованием живых культур ассоциативных микроорганизмов является одним из приоритетных на сегодняшний день направлений в рамках концепции экологизации сельского хозяйства. Однако следует помнить, что в естественных местообитаниях оптимальные условия существования, легко воспроизводимые в лаборатории, являются скорее исключением, чем правилом, как для микроорганизмов, так и для растений, не способных, подобно животным, уйти (в прямом смысле этого слова) от действия неблагоприятного фактора. Следовательно, эффективность биопрепаратов, разработанных без учета особенностей устойчивости микроорганизмов, может оказаться невысокой. В связи с вышесказанным при разработке бактериальных удобрений направленного действия, на наш взгляд, целесообразно экспериментальное моделирование условий среды, являющихся стрессовыми и для бактерий, и для их растений-хозяев (например, действие высокой температуры).
В формировании мутуалистических взаимоотношений ризобактерий и растений наиболее важным соединением-посредником служит ИУК, к экскреции и/или утилизации которой способны многие ризосферные микроорганизмы [8, 9]. Вполне справедливо «бактериальную» ИУК рассматривать в качестве аллелохимиката, полезного и для организмов-продуцентов (бактерий) – алломона, и для организмов-реципиентов (растений-хозяев) – кайромона.
По мнению большинства исследователей, изменяя концентрацию ИУК в прикорневой зоне и соответственно в клетках корней, ризосферные микроорганизмы тем самым «вмешиваются» не только в развитие корневой системы, но и растения в целом [9]. В том числе можно предполагать участие бактерий, экскретирующих и/или потребляющих ИУК, в формировании устойчивости растений к меняющимся условиям внешней среды за счет модификации их гормонального баланса и, следовательно, исходного физиологического состояния. При этом нельзя исключить, что изменения устойчивости растений, спровоцированные присутствием бактерий, разнонаправленно влияющих на гормональный баланс своих хозяев, также могут оказаться неравнозначными.
Настоящая работа посвящена выявлению особенностей влияния на термоустойчивость проростков пшеницы штамма-гиперпродуцента ИУК – Azotobacter chroococcum 66 и микроорганизма, способного использовать ИУК в качестве универсального ростового субстрата – Pseudomonas putida NBr9.
Материал и методы исследования
Объектами исследований служили проростки яровой пшеницы (Triticum aestivum L.) сорта «Московская-35», а также бактерии Azotobacter chroococcum 66 (штамм из коллекции Музея микробиологии МГУ, Москва) и Pseudomonas putida NBr9 (штамм из коллекции Института физиологии и биохимии микроорганизмов РАН, Пущино). A. chroococcum 66 обладает высокой ИУК-экскретирующей активностью; P. putida – наряду с продуцированием способен использовать ИУК как источник углеродного и азотного питания [1].
Семена пшеницы обрабатывали 0,1 % раствором KMnO4 и после промывания, экспонирования в стерильной водопроводной воде (4 ч) проводили инокуляцию бактериями A. chroococcum 66 либо P. putida NBr9 (опытный вариант). Контролем служили семена, которые оставались стерильными. Бактерии для инокуляции выращивали в течение 24 ч на соответствующих питательных средах: A. chroococcum 66 на твердой элективной среде Эшби; P. putida NBr9 на жидкой среде М-9. Концентрация микроорганизмов в инокуляте составляла 109 мл–1.
Колонизированные бактериями и контрольные семена проращивали в стерильных влажных чашках Петри при 26 °С. На вторые сутки после оценки всхожести проростки переносили в сосуды, содержащие 25 мл стерильной водопроводной воды и покрытые крышками из фольги (15 проростков на сосуд). Проростки культивировали в климатокамерах при 26 °С и 14-часовом фотопериоде. На 3-и, 7-е сутки проводили контроль эффективности бактериальной колонизации поверхности корней и околокорневого раствора.
Тестирование термоустойчивости (прогрев при 42 °С, 15 мин) 7-суточных проростков пшеницы проводили по методике, разработанной сотрудниками кафедры биофизики ННГУ им. Н.И. Лобачевского для диагностики воздействия на растения химических веществ [4]. Метод основан на сравнении отношений амплитуд и скоростей импульсных биоэлектрических реакций.
Побеги контрольных и опытных проростков закрепляли в кюветах так, чтобы корни сохраняли контакт с околокорневым раствором. После фиксации растения выдерживали на свету в течение времени, существенно превышающего рефрактерный период. Первое тестирующее охлаждение (до гипертермического воздействия) осуществляли быстрым внесением в кювету ледяной воды, при этом измерительный электрод (ЭВЛ-1М3) контактировал с поверхностью охлаждаемого участка побега, а электрод сравнения – с околокорневым раствором. Прогрев зафиксированных в кюветах проростков осуществляли в термостате через 45 мин после первого тест-воздействия. Повторное тестирующее воздействие проводили через 30 мин после окончания действия стрессора (нагревание).
Результаты представлены в виде отношений: А2/А1, где А1 – амплитуда первой деполяризации (до гипертермического воздействия), А2 – амплитуда второй деполяризации (после прогрева); V2/V1, где V1 – скорость первой деполяризации (до гипертермии), V2 – скорость второй деполяризации (после нагрева). Если эти отношения больше 1,0 (или 100 %), то можно говорить о повышенной устойчивости объекта к действию стрессора, если же отношения менее 1,0 (или 100 %), то это свидетельствует об угнетении жизнедеятельности растения. Биологическая повторность опытов 15-кратная. Статистическую обработку результатов проводили с помощью стандартного программного пакета «STATISTICA 6.0».
Результаты исследования и их обсуждение
В настоящее время есть вполне достаточные основания полагать, что роль электрогенеза в формировании адаптационного синдрома клеток высших растений при неблагоприятных воздействиях окружающей среды может быть весьма значительной [2]. Неслучайно, что биоэлектрическая активность используется как довольно удобный диагностический показатель функционального состояния растений [6, 4].
В наших исследованиях удалось показать, что тест-воздействие (охлаждение), наносимое на участок побега проростков экспериментальных вариантов (рис. 1) до гипертермического прогрева и через 30 мин после действия стрессора, вызывало различную по амплитуде и скорости первичную деполяризацию плазмалеммы (ПМ) клеток в зоне охлаждения. Амплитуда (А, мВ) и скорость (V, с) деполяризации ПМ клеток побега до стресс-воздействия (нагревания) у проростков пшеницы контрольной группы выше, чем у проростков, корни которых контаминированы бактериями A. chroococcum 66 или P. Putida NBr9. Возможно, данный эффект обусловлен снижением исходного уровня мембранного потенциала, а следовательно, энергизованности ПМ клеток растений при взаимодействии их с ризосферной микрофлорой. Высказанное предположение выглядит небезосновательным на фоне данных T. Ersek et al. [7], Y. Bashan, Н. Levanony [7], убедительно свидетельствующих о влиянии ризобактерий на мембранный потенциал клеток корней растений-хозяев.
Данные, полученные при сравнении амплитуд и скоростей первичной деполяризации ПМ клеток побега в зоне тест-воздействия до (А1, V1) и после нагревания (А2, V2) у инокулированных и неинокулированных растений, свидетельствуют об инициированном бактериями повышении устойчивости проростков пшеницы. Так, отношение А2/А1 достоверно превышало 1,0 у проростков, зараженных A. chroococcum 66 или P. putida NBr9, особенно в варианте с псевдомонадами (рис. 2). У растений, контактирующих с P. putida NBr9, также достоверно возрастало отношение V2/V1.
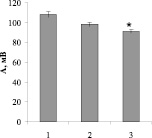
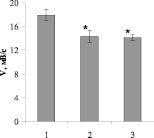
а б
Рис. 1. Амплитуда (а) и скорость (б) деполяризации проростков пшеницы до нагревания: * – различия статистически достоверны по сравнению с контролем (P < 0,05); 1 – без инокуляции; 2 – инокуляция A. chroococcum 66; 3 – P. putida NBr9
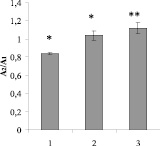
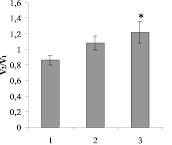
а б
Рис. 2. Отношение амплитуды (а) и скорости (б) деполяризации проростков пшеницы после нагрева (A2, V2) к исходным значениям (A1, V1); различия статистически достоверно отличались от 1,0: * – P < 0,05; ** – Р < 0,01; 1 – без инокуляции; 2 – инокуляция A. chroococcum 66; 3 – P. putida NBr9
Таким образом, как показали результаты электрофизиологических исследований, инокуляция A. chroococcum 66 и P. putida NBr9 увеличила термоустойчивость проростков пшеницы. Неинокулированные проростки проявляли пониженную устойчивость к нагреванию – А2/А1 было менее 1,0, а отношение V2/V1 имело тенденцию к снижению.
Однако в каждом экспериментальном варианте можно было выделить растения, у которых отношения А2/А1 и V2/V1 превышали 1,0 и были менее 1,0, т.е. растения с повышенной устойчивостью к нагреванию при 42 °С (15 мин) и не устойчивые к этой дозе воздействия соответственно. Тем не менее, вычислив долю растений, у которых оба отношения превышали 1,0 (N), можно говорить о том, что среди инокулированных проростков доминировали высокоустойчивые индивиды, тогда как доля устойчивых растений в контрольной группе довольно мала (рис. 3). Кроме того, количество устойчивых растений несколько преобладало в варианте с P. putida NBr9 по сравнению с группой проростков, инокулированных A. chroococcum 66.
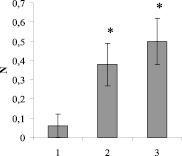
Рис. 3. Доля проростков пшеницы, у которых A2/A1 и V2/V1 превышали 1,0; * – различия статистически достоверны по сравнению с контролем (Р < 0,05); 1 – без инокуляции; 2 – инокуляция A. chroococcum 66; 3 – P. putida NBr9
Заключение
Полученные данные позволяют говорить о повышении устойчивости проростков пшеницы к нагреванию при сосуществовании с бактериями A. chroococcum 66 и P. putida NBr9. Защитный эффект P. putida NBr9 при данных условиях эксперимента оказался более выраженным, чем эффект A. chroococcum 66. Это проявлялось более значительным влиянием P. putida NBr9 на амплитуду первичной деполяризации плазматической мембраны клеток побега проростков после нагревания, достоверным увеличением скорости этой первичной биоэлектрической реакции, а также преобладанием в группе доли устойчивых растений. Одна из вероятных причин неодинаковой устойчивости проростков пшеницы в присутствии P. putida NBr9 или A. chroococcum 66 может заключаться в разнонаправленном влиянии исследованных микроорганизмов на гормональный баланс растений-хозяев. Это предположение открывает перспективы для дальнейшего углубленного исследования механизмов вмешательства бактерий в работу гормональной сигнальной системы эукариотических организмов.
Исследования термоустойчивости проростков пшеницы поддержаны проектом № 2575 Задания № 2014/134 на выполнение государственных работ в сфере деятельности в рамках базовой части государственного задания.
Рецензенты:
Постнов И.Е., д.б.н., профессор кафедры «Водные ресурсы и аквакультура», ФГБОУ ВПО «Нижегородская государственная академия», г. Нижний Новгород;
Смирнов В.Ф., д.б.н., профессор, руководитель лаборатории НИИ Химии, ФГАОУ ВО «Нижегородский государственный университет им. Н.И. Лобачевского», г. Нижний Новгород.
Библиографическая ссылка
Мацкова Ю.А., Олюнина Л.Н., Сухов В.С., Неруш В.Н., Синицына Ю.В., Веселов А.П. ВЛИЯНИЕ ПРОДУЦИРУЮЩИХ ИНДОЛ-3-УКСУСНУЮ КИСЛОТУ БАКТЕРИЙ AZOTOBACTER CHROOCOCCUM 66 И PSEUDOMONAS PUTIDA NBR9 НА ТЕРМОУСТОЙЧИВОСТЬ ПРОРОСТКОВ ПШЕНИЦЫ (TRITICUM AESTIVUM L.) // Фундаментальные исследования. 2015. № 7-4. С. 682-686;URL: https://fundamental-research.ru/en/article/view?id=38801 (дата обращения: 13.05.2026).



