Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
MORPHOFUNCTIONAL CHARACTERISTIC OF THE REPARATIVE HISTOGENESIS IN LIQUIDATION RIGID RESIDUAL PLEURAL CAVITY USING A COMPOSITE MATERIAL «LITAR»
Эмпиема плевры остается значительной медицинской проблемой на сегодняшний день из-за значительной заболеваемости, длительной госпитализации и повышенного риска смертности.
У большей части больных эмпиема плевры возникает из-за воспалительных процессов в легких на фоне острой пневмонии – 4 %, абсцесса легкого – 9–11 %, при гангрене легкого – 80–95 % и как следствие ранений и травм органов грудной клетки – 6–12 % [11, 12].
При неэффективности лечения эмпиема плевры приобретает хроническое течение [8], создается ригидная остаточная полость в которой сохраняется гнойный процесс. Задачи хирургического лечения сводятся к устранению очага инфекционного процесса и ликвидации стойкой остаточной плевральной полости [10, 13]. Декортикация легкого и плеврэктомия в чистом виде могут быть выполнены очень ограниченному контингенту больных при отсутствии значительной деструкции легкого и бронхо-плевральных свищей. Чаще всего эту операцию необходимо сочетать с дополнительными вмешательствами; резекцией пораженных отделов легкого, реампутацией культи бронха, корригирующей торакопластикой [4, 5]. А после необратимых изменений в коллабированных отделах легкого оно теряет способность к расправлению даже после декортикации. В таких случаях ликвидировать остаточную полость можно лишь торакопластикой или мышечной пластикой [2].
В связи с этим заслуживают внимания попытки ликвидации стойкой остаточной плевральной полости с помощью пломбирования различными материалами [3, 9]. В реконструктивной хирургии хронической эмпиемы плевры, для ликвидации остаточной полости, по нашему мнению, может быть применен гидроксоапатитколлагеновый композит «ЛитАр», используемый для ликвидации остаточных полостей печени [6, 7]. Сведения о применении препарата для ликвидации ригидной остаточной полости плевры отсутствуют. Также в последние годы в схемы местной антибактериальной терапии при различных инфекционно-воспалительных процессах стали вводить окситоцин [1].
Таким образом, очевидна необходимость изучения возможности использования композита «ЛитАр» для пломбировки остаточной плевральной полости. а также выяснения роли окситоцина в регуляции репаративных процессов после имплантации «ЛитАр».
Цель – изучение репаративных гистогенезов при ликвидации ригидной остаточной полости плевры с использованием композитного материала «ЛитАр».
Материалы и методы исследования
Объектом исследования были лабораторные белые крысы – самцы линии Вистар массой 280–300 г. Число наблюдений – 39. Содержание и выведение животных из эксперимента соответствовало «Правилам проведения работ с использованием экспериментальных животных», утвержденным Приказом МЗ СССР № 755 от 12.08.77 г., а также положениям «Европейской конвенции по защите позвоночных, используемых для экспериментальных и иных научных целей». Проведение исследований разрешено локальным этическим комитетом ГБОУ ВПО ОрГМА МЗ России от 01.10.2014 г.
Гидроксоапатитколлагеновый композит под названием «ЛитАр» представляет из себя смесь гидроксоапатита и ксеноколлагена с высоким уровнем взаимной структурной интеграции. Данный композит является цитоактивным наноразмерным материалом, предназначенным для восполнения дефектов тканей. Средние размеры кристаллов апатита в материале «ЛитАр» – 43–45 нм. Фирма-изготовитель ‒ ООО НПП «СердоЛит» (Самарская область, г. Самара, ул. Гагарина, д. 48). На данный материал выдано регистрационное удостоверение 11 июня 2010 года № ФСР 2010/07994 и сертификат соответствия № 9398-001-64938703-2010. Извлечение упакованного в полиэтилен материала производили после вскрытия пакета стерильным инструментом (пинцетом) непосредственно перед имплантацией в плевральную полость. Стерильный материал перед имплантацией нарезался стерильными ножницами.
Было проведено 3 серии опытов. В первой серии опытов на 9 животных создали модель асептической ограниченной полости в правой половине грудной клетки путем имплантации в нее латексного шарика. Из медицинского силикона вырезались шарики диаметром 6-9 мм. Силиконовые шарики хранились в растворе 0,5 % хлоргексидинового спирта. Перед операцией шарик вынимали из спирта, отмывали стерильным физиологическим раствором и имплантировали в правую половину плевральной полости экспериментального животного. На них изучили структурно-функциональные особенности формирования остаточной полости при экспериментальной имплантации в грудную клетку силиконового объекта.
Во 2-й серии полость, сформированная по вышеописанной методике, на стадии 20 суток эксперимента заполнялась композитом «ЛитАр», другого лечения не проводилось. В 3-й серии опытов сформированная таким же образом полость на стадии 20 суток опыта заполнялась композитом «ЛитАр» пропитанным раствором окситоцина (1 МЕ), при этом после пломбировки в течение 10 дней экзогенно (пункционно) к месту имплантации ежедневно подводился раствор окситоцина (1МЕ).
Все операции проводили под эфирным масочным наркозом при соблюдении правил асептики и антисептики. Рану грудной клетки зашивали наглухо. Животных выводили из опыта путем передозировки эфира: 1-й серии на 7, 14 и 21 сутки; 2 и 3 серии – на 3, 7, 14 и 30 сутки с момента имплантации «ЛитАр». Полученный материал исследовали с использованием обзорных гистологических методов (гематоксилин Майера и эозин, по Ван Гизону).
Результаты исследования и их обсуждение
Анализ гистологических препаратов 1-й серии экспериментов показал, что введение в плевральную полость латексного шарика для формирования ограниченной остаточной полости приводит к возникновению воспалительного процесса в тканях лёгкого, прилежащих к области расположения шарика. В первые трое суток в тканях, контактирующих с латексным шариком, отмечаются явления отека и формирования демаркационно-некротического вала, ограничивающего формирующуюся полость. В зону, окружающую формирующуюся полость, происходит миграция лейкоцитов из сосудов микроциркуляторного русла в результате резкой вазодилятации и усиления экстравазации плазмы и форменных элементов из них. Клеточные элементы, наблюдаемые здесь, представлены в эти сроки гранулоцитами (в основном нейтрофилами и эозинофилами), макрофагами, лимфоцитами.
Наличие зоны некротически изменённой ткани и очаговых кровоизлияний отмечалось в течение первой-второй недель.
К концу первой недели происходило формирование соединительнотканной капсулы вокруг латексного шарика. Наиболее активно процессы фибриллогенеза в формирующейся капсуле отмечались в течение 2-й и 3-й недель. К концу 4-й недели вокруг латексного шарика была сформирована хорошо выраженная соединительнотканная фиброзная капсула (рис. 1).
Анализ гистологических препаратов 2-й серии экспериментов, в которой использовали композитный материал «ЛитАр» для закрытия остаточной полости, показал, что уже к концу третьих суток композитный материал набухает и заполняет всю остаточную полость.
К концу первой недели в пространстве заполненным композитным материалом «ЛитАр» обнаруживаются врастающие кровеносные сосуды и мигрирующие клеточные элементы соединительной ткани (рис. 2). Этому способствовал пористый характер материала, а также описанное ранее наличие у этого материала свойств индукции ангиогенеза и стимуляции гистиотипической репаративной регенерации, пористая структура «ЛитАр» способствовала обеспечению газообмена и обмена жидкости и обеспечивала оптимальное существование мигрирующих клеток фибробластического дифферона соединительной ткани [6, 7].
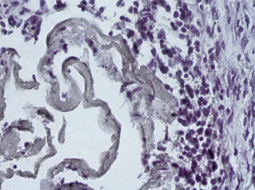
Рис. 1. Фрагмент ригидной остаточной полости плевры крысы через 14 суток после начала ее формирования. Окраска: гематоксилин Майера и эозин; увеличение окуляр×10, объектив ×40
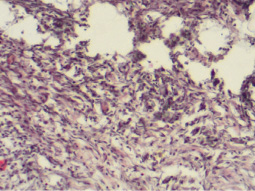
Рис. 2. Фрагмент ригидной остаточной полости плевры крысы, заполненной композитным материалом «ЛитАр». Стадия 7 суток эксперимента. Окраска: гематоксилин Майера и эозин; увеличение окуляр×10, объектив ×20
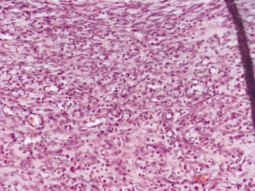
Рис. 3. Фрагмент ригидной остаточной полости плевры крысы, заполненной композитным материалом «ЛитАр», пропитанным окситоцином. Стадия 7 суток эксперимента. Окраска: гематоксилин Майера и эозин; увеличение окуляр×10, объектив ×20
На фоне формирований соединительной ткани отмечается биодеградация композитного материала «ЛитАр», которая полностью завершается к концу первого месяца.
Анализ препаратов третьей серии экспериментов показал, что при имплантации композитного материала «ЛитАр» с одновременным применением окситоцина в сформированной полости, заполненной композитным материалом, наблюдалось более длительное существование малодифференцированной соединительной ткани. При введении окситоцина пролиферативная активность малодифференцированных клеточных элементов соединительной ткани отмечается в течение более длительных сроков.
Если при использовании «ЛитАр» без окситоцина уже на второй неделе в образовавшейся в остаточной полости соединительной ткани возрастает содержание фибриллярных компонентов (, коллагеновых волокон), то в случае применения окситоцина более длительное время в соединительной ткани сохраняется значительное содержание и активная пролиферация малодифференцированных клеточных элементов фибробластического дифферона (рис. 3). То есть процесс дифференцировки клеточных элементов фибробластического дифферона соединительной ткани отодвигается в этом случае на более длительные сроки.
Подсчёт лейкоцитов в формирующейся соединительной ткани показал, что в случае пломбировки остаточной полости препаратом «ЛитАр» с одновременным применением окситоцина содержание лейкоцитов в формирующейся соединительной ткани в остаточной полости существенно снижено в сравнении с экспериментом по пломбировке остаточной полости только композитным материалом «ЛитАр» без применения окситоцина. Подобное состояние отмечается на всех стадиях эксперимента (3,7 и 14,21 м 28 суток).
При этом в эксперименте с использованием окситоцина в формирующейся соединительной ткани более длительное время наблюдается процесс активного васкулогенеза, вследствие чего количество сосудов микроциркуляторного русла на единицу площади соединительной ткани в этом случае превышает таковое при формировании соединительной ткани в зоне введения «ЛитАра» без использования окситоцина.
Следует отметить, что замедленное созревание соединительной ткани отмечается не только в остаточной полости, заполненной композитным материалом «ЛитАр», но также и в соединительнотканной капсуле, ограничивающей остаточную полость.
Заключение
Полученные результаты свидетельствуют о том, что использование композитного материала «ЛитАр» в комплексе с окситоцином оптимизирует процессы пролиферации и дифференцировки малодифференцированных клеточных элементов фибробластического дифферона, что приводит к ликвидации остаточной полости и формированию на ее месте рыхлой неоформленной соединительной ткани.
Рецензенты:
Валов С.Д., д.м.н., профессор кафедры гистологии, цитологии и эмбриологии, ГБОУ ВПО «Оренбургский государственный медицинский университет» Минздрава России, г. Оренбург;
Тарасенко В.С., д.м.н., профессор, заведующий кафедрой госпитальной хирургии и урологии, ГБОУ ВПО «Оренбургский государственный медицинский университет» Минздрава России, г. Оренбург.
Библиографическая ссылка
Мухаммедов Х.Б.М., Шевлюк Н.Н., Третьяков А.А., Стадников А.А. МОРФОФУНКЦИОНАЛЬНАЯ ХАРАКТЕРИСТИКА РЕПАРАТИВНЫХ ГИСТОГЕНЕЗОВ ПРИ ЛИКВИДАЦИИ РИГИДНОЙ ОСТАТОЧНОЙ ПОЛОСТИ ПЛЕВРЫ С ИСПОЛЬЗОВАНИЕМ КОМПОЗИТНОГО МАТЕРИАЛА «ЛИТАР» // Фундаментальные исследования. 2015. № 1-10. С. 2065-2069;URL: https://fundamental-research.ru/en/article/view?id=38598 (дата обращения: 14.05.2026).



