В настоящее время всё больше внимания уделяется своевременному, адекватному лечению предраковых заболеваний слизистой оболочки (СО) рта и красной каймы губ, в частности лейкоплакии (Л) [1, 9].
Лейкоплакия продолжает оставаться одной из наиболее распространенных нозологий в структуре заболеваемости слизистой оболочки рта и красной каймы губ, поэтому вопросы ранней диагностики, лечения и понимание процессов патогенеза, в том числе нарушение свободнорадикального окисления (СРО), остаются актуальными [10].
В настоящее время доказано значение свободнорадикального окисления (СРО) в патогенезе воспалительных заболеваний пародонта и слизистой оболочки рта [8, 11]. Радикалы кислорода вырабатывают клетки, обладающие фагоцитарной активностью. Они обеспечивают их микробицидность. При острых и обострении хронических воспалительных процессов количество активных форм кислорода (АФК) в биологических жидкостях увеличивается, что может стать причиной инициирования свободнорадикального перекисного окисления липидов [2, 4].
Свободные радикалы кислорода, азота и хлора, перекиси и другие продукты обладают высокой реакционной способностью, инициируя цепные реакции перекисного окисления липидов (ПОЛ). Свободные радикалы повреждают белки, нуклеиновые кислоты, вызывают «оксидативный стресс» – процесс повреждения клетки в результате окисления [2, 5, 7].
Из всего многообразия эффектов, составляющих синдром оксидативного стресса, наиболее важным является повреждение биологически важных молекул, структуры и функций биологических мембран. Это приводит к нарушению тканевого дыхания во внутренней мембране митохондрии, процессов гидроксилирования в микросомах, выходу лизосомальных ферментов, повреждению важных транспортных путей и т.д. [3].
Защита от избытка свободных радикалов в ротовой жидкости осуществляется антиоксидантной системой, в том числе ферментами: супероксиддисмутазой, каталазой, глутатионпероксидазой и т.д.
В то же время недостаток активных форм кислорода, которые участвуют в обмене веществ, обеспечивают защитные функции, в частности вырабатываются фагоцитирующими клетками и обеспечивают микробицидные свойства ротовой жидкости, способствуют микробной инвазии. Поэтому как ускорение СРО, так и его подавление в ротовой жидкости может играть определенную роль в развитии воспалительных заболеваний слизистой оболочки рта [2, 3, 5].
Был разработан метод исследования хемилюминесценции (ХЛ) ротовой жидкости, основанный на регистрации ХЛ биологического материала – свечения, возникающего при взаимодействии радикалов. Это единственный метод, не нуждающийся в особых лабораторных условиях, дополнительной подготовке материала к анализу, отвечающий всем требованиям экспресс-анализа, что представляет особую ценность. К достоинствам этого метода относится высокая чувствительность и выявление наиболее реакционноспособных, короткоживущих радикалов, которые другими способами не регистрируются [6].
Целью исследования было изучение состояния СРО ротовой жидкости у пациентов с плоской формой лейкоплакии.
Материалы и методы исследования
В протокол исследования ротовой жидкости методом хемилюминесценции были включены 64 женщины (основная группа) без вредных привычек, с диагнозом плоская форма Л, с сопутствующей гастроэнтерологической патологией (эзофагиальная болезнь, гастрит, хронический холецистит) вне обострения. Длительность заболевания лейкоплакией составила от 1 до 3 лет. Возраст пациентов был от 43 до 57 лет (средний возраст 50,2 ± 3,9).
Контрольную группу пациентов составили 15 женщин, без патологии СОР, без выраженной соматической патологии, средний возраст которых составил 49,4 ± 2,7 лет.
Хемилюминесценцию (ХЛ) ротовой жидкости измеряли на приборе ХЛ-003 (рис. 1). В качестве наиболее информативного показателя ХЛ была взята светосумма излучения – S и ее максимальное значение – I max за время исследования. Весь процесс измерения ХЛ и обработка результатов проводились в автоматическом режиме, что повышало точность и объективность получаемой информации. Определение ХЛ ротовой жидкости всем пациентам исследуемых групп проводили натощак до чистки зубов. Забор ротовой жидкости проводили через 20 минут после предварительного ополаскивания полости рта физиологическим раствором.
Статистическую обработку данных проводили с использованием пакета прикладных программ Statistica 10 и электронных таблиц Exel 2007. Для сравнения полученных данных использовался критерий Стьюдента. Уровень достоверной значимости был принят р < 0,01.
Результаты исследования и их обсуждение
Было изучено состояние свободнорадикального окисления ротовой жидкости контрольной группы пациентов. Величина спонтанного свечения ротовой жидкости в этой группе колебалась от 2,2 до 6,1 усл. ед., в среднем составляла 3,1 ± 0,4 усл. ед., светосумма свечения S от 3,4 до 8,3 усл. ед., в среднем 6,01 ± 1,44 усл. ед., максимальная интенсивность свечения I max от 1,1 до 3,4 усл. ед., в среднем 2,42 ± 0,77 усл. ед. В качестве наиболее информативных показателей были взяты светосумма излучения и ее максимальная интенсивность, которые в дальнейших исследованиях послужили в качестве контроля (рис. 2).

Рис. 1. Прибор ХЛ-003
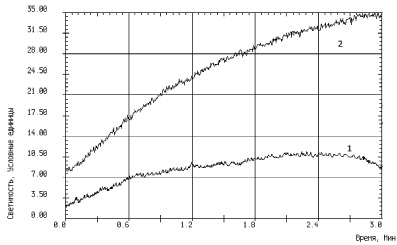
Рис. 2. Типичная запись хемилюминесценции ротовой жидкости пациентов: 1 – контрольной группы; 2 – пациентов с плоской формой лейкоплакии СОР
Хемилюминесценция ротовой жидкости (усл. ед.) у пациентов с плоской формой лейкоплакии и контрольной группы
|
Показатели ХЛ ротовой жидкости |
Хемилюминесценция ротовой жидкости |
|
|
Контрольная группа (n = 15) |
Основная группа (n = 64) |
|
|
S – светосумма |
6,01 ± 1,44 |
29,3 ± 4,4* |
|
I max – максимальная интенсивность |
2,42 ± 0,77 |
10,1 ± 1,65* |
Примечание. Отличие достоверно с контролем р < 0,01*.
Исследование ХЛ ротовой жидкости у пациентов с плоской формой лейкоплакии выявило следующие результаты: величина спонтанного свечения ротовой жидкости в этой группе колебалась от 5,5 до 8,4 усл. ед., в среднем составляла 6,1 ± 0,8 усл. ед., светосумма свечения S в среднем 29,3 ± 4,4 усл. ед., максимальная интенсивность свечения I max в среднем 10,1 ± 1,65 усл. ед. (таблица).
Выводы
Выявлены значения нормы показателей ХЛ ротовой жидкости женщин, без патологии СОР, без выраженной соматической патологии, возрастной группы 49,4 ± 2,7 лет: значение S (светосумма) составило 6,01 ± 1,44; значение I max (максимальная интенсивность) составило 2,42 ± 0,77.
У пациентов с лейкоплакией СОР показатели ХЛ ротовой жидкости отличались от показателей нормы. Как значение светосуммы (S), так и значение максимальной интенсивности (I max) достоверно были выше по сравнению с контрольной группой.
Полученные данные ХЛ свидетельствуют о нарушении процессов СРО у пациентов с плоской формой Л при сопутствующей гастроэнтерологической патологии. Достоверное отличие в сторону увеличения значений СРО в ротовой жидкости пациентов основной группы создает оксидативный стресс с повреждением биологических мембран, и это поддерживает хронический характер течения лейкоплакии, способствует микробной инвазии и аллергизации организма. Таким образом, при Л необходим выбор метода лечения, учитывающий состояние СРО.
Рецензенты:
Кабирова М.Ф., д.м.н., профессор кафедры терапевтической стоматологии с курсом ИДПО, ГОУ ВПО «Башкирский государственный медицинский университет», г. Уфа;
Блашкова С.Л., д.м.н., доцент, заведующая кафедрой терапевтической стоматологии, ГБОУ ВПО «Казанский государственный медицинский университет» Минздрава России, г. Казань.
Библиографическая ссылка
Герасимова Л.П., Чемикосова Т.С., Вильданов М.Н. ПОКАЗАТЕЛИ ХЕМИЛЮМИНЕСЦЕНЦИИ РОТОВОЙ ЖИДКОСТИ У ПАЦИЕНТОВ С ЛЕЙКОПЛАКИЕЙ СЛИЗИСТОЙ ОБОЛОЧКИ РТА // Фундаментальные исследования. 2015. № 1-10. С. 2027-2030;URL: https://fundamental-research.ru/en/article/view?id=38590 (дата обращения: 22.04.2026).



