Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE EFFECT OF DIOCTAHEDRAL SMECTITE ON THE COXSACKIE A VIRAL MYOCARDITIS IN EXPERIMENT
В настоящее время большинством исследователей признан факт высокой распространенности воспалительных изменений миокарда. В некоторых группах больных на фоне тяжелого течения инфекций частота сердечно-сосудистых нарушений, по клиническим симптомам, данным электрокардиографии, эхокардиографии, повышению активности кардиоспецифичных ферментов и тропонина достигает 33–45 % [6]. На практике миокардит диагностируется редко. Патологоанатомически воспалительные признаки в миокарде регистрируют в 4–9 % случаев [1]. Основным этиологическим фактором считаются вирусы [7, 10]. Затруднения при диагностике на практике связаны в первую очередь с недостаточной изученностью возбудителя. Считается, что тяжелое течение Коксаки А вирусной инфекции с миокардитом характерно для лиц с ослабленным иммунитетом, особенно для новорожденных детей [9]. Эффективная этиотропная терапия в настоящее время отсутствует. Снизить степень вирусемии возможно с помощью энтеросорбентов, создающих барьер на поверхности эпителия кишечника. Среди них одно из первых мест занимает диоктаэдрический смектит, внесенный в стандарты терапии инфекционных диарей [3, 4, 5, 11]. Однако действие его на внекишечные проявления инфекции не изучено.
Цель исследования – определить влияние диоктаэдрического смектита на вероятность развития миокардита, его выраженность и летальность при Коксаки А вирусной инфекции в эксперименте.
Материалы и методы исследования
В исследование было включено 45 самцов мышей ВАLB/с в возрасте 2 недель, массой 6–7 грамм. Животные перед включением в исследование наблюдались 7 дней. При обнаружении каких-либо отклонений от нормы особей выбраковывали. В опытную группу вошло 40 мышей, которые были заражены перорально вирусом Коксаки А № 2046 из Государственной коллекции вирусов РГБУ НИИ вирусологии имени Д.И. Ивановского в дозе LD70. Методом случайного распределения они были распределены на 2 группы. Группу А составили 20 животных, которые спустя 3 часа после заражения начали получать перорально диоктаэдрический смектит в дозе 50 мкл/мышь в сутки в течение 3 дней. В группу В вошло 20 животных, которым лечения не назначали. Контрольную группу составили 5 здоровых особей.
Содержание, питание, уход за животными и выведение их из эксперимента проводили согласно требованиям «Правил проведения работ с использованием экспериментальных животных» (Приложение к приказу МЗ СССР от 12.08.1977 г. № 755).
Визуально ежедневно оценивали состояние особей. Исследовали срезы миокарда желудочков и предсердий 35 мышей на 3-и, 7-е, 14-е и 21-е сутки от момента заражения. Погибшие животные (7 из опытной группы В) не подвергались морфологическому исследованию по техническим причинам. После выведения животного из эксперимента препараты промывали, фиксировали с помощью забуференного нейтрального формалина (рН = 7,0) и заливали парафином. С помощью микротома проводили срезы толщиной 5 мкм, затем окрашивали гематоксилином и эозином. Полученные препараты исследовали при помощи оптической световой микроскопии с увеличением 280х, 400х и 630х (окуляры 7х или 10х; объективы 40х и 90х).
Оценку состояния миокарда и кардиомиоцитов проводили по гистологическим параметрам, отражающим состояние кардиомиоцитов, стромы и сосудов на основании имеющихся в литературе рекомендаций [2] с уточнением, по результатам собственных наблюдений. Определяли состояние мембраны, цитоплазмы и форму кардиомоцита; форму ядер клеток; исчерченность миофибрилл; наличие инфильтрации соединительнотканной пластинки; состояние кровеносных сосудов. Полуколичественную оценку изменений проводили по предложенной нами методике [8]. За 1 принимали картину, соответствующую контрольной группе. Умеренным изменениям присваивали 2 балла, выраженным – 3.
Результаты исследования и их обсуждение
У контрольных мышей в миокарде была выявлена картина, соответствующая адаптационной норме (1 балл по всем критериям).
На 3-и сутки после заражения вирусом Коксаки А у животных обеих опытных групп были отмечены сходные изменения, соответствующие умеренно выраженному или выраженному миокардиту, что представлено на рис. 1.
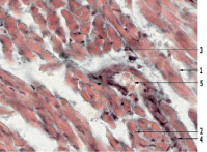
Рис. 1. Миокард мыши на 3-и сутки после заражения вирусом Коксаки А, окраска гематоксилином и эозином, 280х: 1 – нечеткость мембраны кардиомиоцита; 2 – вакуольная дистрофия цитоплазмы кардиомиоцита, отсутствие поперечно-полосатой исчерченности; 3 – гипохромное ядро кардиомиоцита; 4 – инфильтрация межмиокардиальной стромы лимфоцитами, фиброцитами, фибробластами; 5 – полнокровие сосуда
Клеточная мембрана контурировалась нечетко (2); цитоплазма была в состоянии зернисто-вакуольной дистрофии (2). Кардиомиоциты были вытянутой или округлой формы (1, 2), ядра нормохромны, округлы, у особей группы А расположены беспорядочно (1, 2), а в группе В смещены центрально (2). Поперечно-полосатая исчерченность четко не визуализировалась (2). Межмиокардиальная соединительно-тканная пластинка была умеренно отечна с инфильтрацией фиброцитами, фибробластами, лимфоцитами (2). Кровеносные сосуды в группе А были обычного диаметра, иногда не заполнены (1, 2), в группе В – полнокровны (2). Средняя оценка в группе А составила 1,79 ± 0,1 балла, а в группе В – 1,93 ± 0,07 балла, что не имело статистически достоверной разницы (р > 0,05).
На 7-е сутки после заражения у животных обеих групп выявляли нарастание изменений, что соответствовало картине выраженного миокардита. Однако на фоне лечения диоктаэдрическим смектитом отклонения были достоверно менее значительны. На срезах миокарда наблюдали нечеткость мембраны кардиомиоцитов (2); у животных, не получавших лечения, цитолемма местами отсутствовала (2, 3). Цитоплазма находилась в состоянии зернисто-вакуольной дистрофии (2). Большинство кардиомиоцитов имели овально-вытянутую форму (1, 2). Нормохромные ядра у особей группы А были чаще округлыми, располагались в центре или субламеллярно (1, 2), в группе В гиперхромные округлые ядра были смещены к центру цитоплазмы кардиомиоцитов (3). В цитоплазме животных, получавших лечение, поперечно-полосатая исчерченность была нечеткой (2), а у особей без лечения – отсутствовала (3). Соединительнотканная пластинка была отечной и инфильтрированной фиброцитами, фибробластами и единичными лимфоцитами (2). Сосуды были умеренно полнокровны и расширены (2). Средний балл в группе А составил 1,86 ± 0,09, а в группе В – 2,29 ± 0,21 (р < 0,05).
На 14-е сутки от момента заражения в группе А, получавшей диоктаэдрический смектит, в миокарде опытных животных выявляли картину умеренно выраженного миокардита (рис/ 2).
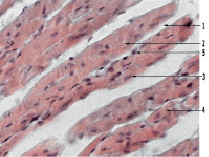
Рис. 2. Миокард мыши на 14-е сутки после заражения вирусом Коксаки А, на фоне лечения диоктаэдрическим смектитом, окраска гематоксилином и эозином, 280х: 1 – отсутствие мембраны кардиомиоцита; 2 – вакуольная дистрофия цитоплазмы кардиомиоцита; 3 – округлое, смещенное к центру ядро кардиомиоцита; 4 – отсутствие поперечно-полосатой исчерченности; 5 – инфильтрация межмиокардиальной стромы лимфоцитами, фиброцитами, фибробластами
Клеточная оболочка кардиомиоцитов была нечеткой (2), разрыхленной. Цитоплазма кардиомиоцитов находилась в состоянии зернисто-вакуольной и вакуольной дистрофии (2, 3); форма кардиомиоцитов была вытянутой (1) или округлой (2); нормохромные ядра были смещены периламеллярно (1). Цитоплазма кардиомиоцитов была с участками нечеткой поперечно-полосатой исчерченности (2) или её отсутствия (3). Соединительнотканная строма миокарда была умеренно отечной и инфильтрированной фибробластами, фиброцитами и единичными лимфоцитами (2). Сосуды умеренно расширены, полнокровны (2). Изменения, в среднем, составили 1,93 ± 0,20 балла.
На 14-е сутки Коксаки А вирусной инфекции в миокарде у животных опытной группы В были выявлены максимальные изменения, что соответствовало картине выраженного миокардита (рис. 3).

Рис. 3. Миокард мыши на 14-е сутки после заражения вирусом Коксаки А, без лечения, окраска гематоксилином и эозином, 280х: 1 – отсутствие мембраны кардиомиоцита; 2 – вакуольная дистрофия цитоплазмы кардиомиоцита; 3 – гипохромное, смещенное к центру ядро кардиомиоцита; 4 – отсутствие поперечно-полосатой исчерченности; 5 – инфильтрация межмиокардиальной стромы лимфоцитами, фиброцитами, фибробластами
Клеточная оболочка не имела четких границ (2). Цитоплазма находилась в состоянии вакуольной дистрофии (3). Форма кардиомиоцитов чаще была овальная (1, 2). Гипохромные ядра располагались в центре цитоплазмы (3). Поперечно-полосатая исчерченность отсутствовала (3). Соединительнотканная пластинка была отечной и инфильтрированной фиброцитами, фибробластами и лимфоцитами (2, 3). Сосуды были полнокровны или неравномерного наполнения (2, 3). Средний балл составил 2,50 ± 0,22 (р < 0,05).
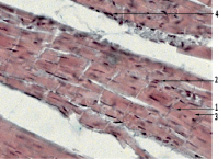
Рис. 4. Миокард мыши на 21-е сутки после заражения вирусом Коксаки А, на фоне лечения диоктаэдрическим смектитом, окраска гематоксилином и эозином, 280х: 1 – мембрана кардиомиоцита; 2 – вытянутое смещенное субламеллярно ядро; 3 – поперечно-полосатая исчерченность; 5 – инфильтрация стромы фиброцитами и фибробластами
На 21-е сутки после заражения в группе А, получавшей диоктаэдрический смектит (рис. 4), отмечали отечность стромы без лимфоцитарной инфильтрации, что можно отнести к остаточным проявлениям миокардита. Клеточная оболочка имела четкие контуры (1). Цитоплазма была в состоянии зернистой дистрофии (1). Большинство кардиомиоцитов имели вытянутую (1) форму. Нормохромные овальные ядра располагались субламеллярно (1). Цитоплазма имела четкую поперечно-полосатую исчерченность (1). Строма была слегка отечной, инфильтрирована фиброцитами и фибробластами (1). Сосуды не были расширены, умеренно полнокровны (2). Средняя оценка изменений составила 1,14 ± 0,14 балла.
В группе В на 21-е сутки лимфоцитарная инфильтрация сохранялась, но была менее выражена, чем на 14-е сутки. Мембрана контурирована (1). Цитоплазма была в состоянии зернистой дистрофии (1). Клетки имели овальную или вытянутую форму (1, 2). Нормохромные ядра располагались в центре цитоплазмы (2). Поперечно-полосатая исчерченность четко визуализировалась (1). Строма была умеренно отечна (1) и минимально инфильтрирована фиброцитами, фибробластами и единичными лимфоцитами (2). Сосуды были полнокровны (2). Средняя оценка составила 1,5 ± 0,19 балла (р < 0,05).
Динамика выраженности изменений схематично представлена на рисунке 5.
Во всех образцах миокарда животных, зараженных вирусом Коксаки А перорально, в дозе LD70, на сроках от 3-х до 14-х суток присутствовали признаки миокардита. Однако степень его выраженности на фоне лечения диоктаэдрическим смектитом была достоверно меньше начиная с 7-х суток. На 21-е сутки Коксаки А вирусной инфекции при применении диоктаэдрического смектита лимфоцитарная инфильтрация в миокарде отсутствовала, тогда как у животных, не получавших лечения, сохранялась. Это, наиболее вероятно, связано с барьерной функцией диоктаэдрического смектита, обеспечивающей снижение количества поступающих в кровоток вирусов.

Рис. 5. Динамика выраженности (в баллах) изменений миокарда у линейных мышей, зараженных вирусом Коксаки А
Выводы
1. При пероральном заражении Коксаки А вирусной инфекцией в дозе LD 70, несмотря на лечение, у всех опытных мышей в сердце выявляется картина миокардита.
2. Степень выраженности поражения миокарда при лечении диоктаэдрическим смектитом линейных мышей, зараженных Коксаки А вирусной инфекцией в эксперименте, достоверно меньше, чем в отсутствии терапии.
Рецензенты:
Макашова В.В., д.м.н., ведущий научный сотрудник клинического отдела инфекционной патологии, Центральный НИИ эпидемиологии, г. Москва;
Усенко Д.В., д.м.н., ведущий научный сотрудник клинического отдела инфекционной патологии, Центральный НИИ эпидемиологии, г. Москва.
Библиографическая ссылка
Руженцова Т.А., Плоскирева А.А., Щербаков И.Т., Исаева Е.И., Бондарева А.В., Горелов А.В. ЭФФЕКТИВНОСТЬ ДИОКТАЭДРИЧЕСКОГО СМЕКТИТА ПРИ КОКСАКИ А ВИРУСНОМ МИОКАРДИТЕ В ЭКСПЕРИМЕНТЕ // Фундаментальные исследования. 2015. № 1-9. С. 1916-1920;URL: https://fundamental-research.ru/en/article/view?id=38453 (дата обращения: 17.05.2026).



