Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
DYNAMICS OF TEMPERATURE CHANGE OF THE SKIN OVER CRANIAL WINDOW BEFORE AND AFTER THE CLOSED IMPLANT
Одним из главных этапов хирургического лечения пациентов с черепно-мозговой травмой является краниотомия, представляющая собой операцию образования отверстия в костях черепа с целью обеспечения доступа к мозговым оболочкам и головному мозгу. Однако сформированное отверстие, позволяющее хирургу провести операцию и сохранить пациенту жизнь, может быть причиной появления патологических неврологических симптомов у пациентов в послеоперационном периоде. Известны такие жалобы пациентов после перенесенной краниотомии, как головная боль, судороги, снижение активности органов чувств, зависимость самочувствия от изменений погоды. Причем такой симптом, как головная боль, может встречаться у 91 % пациентов [12]. Данные осложнения ухудшают состояние здоровья пациентов и качество их жизни, создают необходимость дополнительного приема ими анальгетических, противосудорожных и других сильнодействующих лекарственных средств. Одной из причин появления указанных осложнений может быть изменение локальных температурных показателей гомеостаза головного мозга. Сегодня известно, что температура является самым сильным физическим фактором, способным существенно изменить активность функционирования как всего теплокровного организма человека или животного, так и отдельных его органов и тканей [5, 6, 8, 11]. Однако проведенные в последнее время в экспериментах на животных исследования состояния мозга в области трепанационного отверстия с применением инвазивных методов не ставили задачу исследовать температурные показатели, а касались лишь изучения состояния локальной перфузии мозга и его микроскопических характеристик [10].
В последние годы были убедительно показаны информативность и безопасность инфракрасной термографии и термометрии в изучении изменений локальной температуры поверхности тела теплокровных животных и человека. Данный метод показал высокую чувствительность в диагностике гипоксии и ишемии, в оценке безопасности лекарственных средств и медицинских изделий in vivo [2, 3, 4, 7, 9]. Кроме того, появились результаты исследований, свидетельствующие о возможности изучения инфракрасного излучения головного мозга у новорожденных через щели и роднички в черепе, а у взрослых – через трепанационные отверстия [1, 13, 14, 15]. Таким образом, изучение спектра инфракрасного излучения и динамики температуры кожи головы пациентов, перенесших краниотомию, может помочь в оценке эффективности и безопасности оказанной медицинской помощи.
Цель исследования – изучение температурных изменений кожи человека над костным дефектом черепа после краниотомии и последующей установки титанового импланта.
Материалы и методы исследования.
Проспективные исследования в 2014–2015 гг. были проведены у 10 здоровых добровольцев (контрольная группа) и 5 пациентов с трепанационным окном в теменной области черепа до и после установки им титанового импланта (группа наблюдения). Термографическое исследование проводили через 5 минут после расположения исследуемого в горизонтальное положение лежа на спине в помещении с температурой окружающего воздуха + 25 °С в симметричных точках теменной области с правой и левой сторон.
Измерение температуры и спектра инфракрасного излучения проводили с помощью тепловизора марки ThermoTracer TH9100XX (NEC, USA) в диапазоне температур +25...+36 °С. Количественные данные представлены в виде M ± m, медианы (50-й процентиль), минимального – максимального значений.
План исследований был одобрен этическим комитетом Ижевской государственной медицинской академии на основании принципов, которые изложены во Всемирной медицинской декларации в Хельсинки.
Результаты исследования и их обсуждение
Средний возраст исследуемых в контрольной группе (n = 10) составил 38 ± 10 лет (8 – мужчины), в группе наблюдения (n = 5) – 46 ± 12 лет (4 – мужчины).
Результаты исследований показали, что температура кожи над неповрежденным мозговым черепом как у здоровых добровольцев, так и у пациентов после краниотомии была в пределах 31,8–33,0 °С (таблица).
Показатели средних температур (°С) кожи в симметричных точках теменно-височной области головы исследуемых обеих групп
|
Контрольная группа (n = 10) |
Группа наблюдения (n = 5) |
||
|
справа |
слева |
справа |
слева (над трепанационным окном) |
|
Среднее значение температур, °С |
|||
|
32,7 ± 0,1 |
32,5 ± 0,2 |
32,4 ± 0,2 |
35,4 ± 0,1 |
|
Минимальные-максимальные значения температур, °С |
|||
|
32,0–33,0 |
31,8–33,1 |
32,0–33,0 |
35,1–36,0 |
|
Медиана, °С |
|||
|
32,8 |
32,5 |
32,3 |
35,3 |
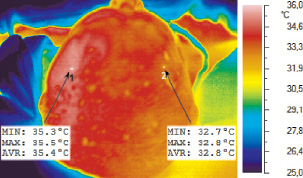
Снимок инфракрасного изображения головы пациента с указанием минимальной (MIN), максимальной (MAX) и средней (AVR) температур кожи в зоне 1 – над трепанационным окном и зоне 2 – над интактной костью
Из представленных в таблице данных следует, что средняя температура кожи над трепанационным окном может превышать аналогичные температурные показатели в симметричной точке здоровой стороны на 3,0 °С. На экране тепловизора трепанационное окно было представлено в виде очага локальной гипертермии и гиперемии (рисунок).
Полученные данные могут свидетельствовать о том, что кости черепа несут теплоизоляционную функцию, предназначенную для обеспечения температурного гомеостаза головного мозга. Проведенные наблюдения за температурой кожи головы пациентов после установки им титанового импланта подтвердили наши предположения. Было выявлено, что установка титанового импланта уменьшала разницу температур и спектра инфракрасного излучения кожи в симметричных участках головы пациентов только при неизменной температуре окружающей среды. Так, в помещении с температурой окружающего воздуха +25...+26 °С показатель средней температуры кожи над имплантом составил +33,2 ± 0,2 °С, а в симметричной точке здоровой стороны головы +33,6 ± 0,1 °С. Важно отметить, что в условиях изменения внешней температуры, в частности после принятия душа пациентами с прохладной или горячей водой, обдувания тела холодным или теплым воздухом, регистрировалось достоверное увеличение разницы температур кожи над участками интактной кости и титанового импланта.
Поскольку локальное изменение температуры мозга играет для него роль раздражающего фактора, который рефлекторно изменяет тонус кровеносных сосудов мозга, вызывая их спазм или паралич, приводящий к нарушению интенсивности локального кровоснабжения мозга и развитию таких клинических симптомов, как головная боль и парестезии, то создание условий для поддержания температурного гомеостаза мозга пациентов является важной задачей. Однако исследований, посвященных изучению теплопроводящих свойств металлов и других искусственных материалов, предназначенных для изготовления вживляемых в организм теплокровных животных и человека имплантов, в современной литературе представлено недостаточно [16].
В связи с этим было предложено стабилизировать температуру мозга, применив имплант с ячеистым строением, выполненный в виде сетки, покрытый слоем из примыкающих друг к другу симметричных полых шестигранных контейнеров, с округлыми гранями, полость каждого контейнера заполнена пеной и герметично закрыта. Данная конструкция импланта может снизить его теплопроводящие свойства и защитить мозг от колебаний температуры окружающей среды и кожи над ними. Для оценки эффективности применения нового импланта необходимы дальнейшие исследования.
Таким образом, краниотомия с формированием у пациента трепанационного окна приводит к нарушению температурного гомеостаза головного мозга за счет удаления участка кости, выполняющего роль теплоизолятора. Трепанационное окно в инфракрасном спектре излучения представляет собой очаг локальной гипертермии, который может быть выявлен с помощью тепловизора. Титановые импланты, устанавливаемые пациентам для устранения костного дефекта, не обладают эффективными теплоизоляционными свойствами. Создание нового импланта с теплоизоляционными свойствами, близкими к костной ткани, может помочь стабилизировать температуру мозга и улучшить результаты реабилитации пациентов.
Авторы выражают благодарность доктору медицинских наук, профессору, академику РАЕ, заслуженному изобретателю РФ, заведующему кафедрой общей и клинической фармакологии ГБОУ ВПО «Ижевская государственная медицинская академия» Александру Ливиевичу Уракову за всестороннюю поддержку и помощь в проведении научных исследований.
Рецензенты:
Ураков А.Л., д.м.н., профессор, заведующий кафедрой общей и клинической фармакологии, ГБОУ ВПО «Ижевская государственная медицинская академия» Минздрава России», г. Ижевск;
Варганов М.В., д.м.н., доцент кафедры факультетской хирургии, ГБОУ ВПО «Ижевская государственная медицинская академия» МЗ РФ, г. Ижевск.
Библиографическая ссылка
Касаткин А.А., Исрафилов Р.Р. ДИНАМИКА ИЗМЕНЕНИЙ ТЕМПЕРАТУРЫ КОЖИ НАД ТРЕПАНАЦИОННЫМ ОТВЕРСТИЕМ ДО И ПОСЛЕ ЕГО ЗАКРЫТИЯ ИМПЛАНТОМ // Фундаментальные исследования. 2015. № 1-8. С. 1596-1599;URL: https://fundamental-research.ru/en/article/view?id=38255 (дата обращения: 01.05.2026).



