Мультифакториальный характер хронического аденоидита (ХА) обуславливает мультисистемный спектр субъективных и объективных симптомов [5]. Однако неспецифичность клинических проявлений не позволяет установить прогноз течения заболевания. Чаще оториноларинголог имеет дело с функциональным исходом ХА в виде сопряженных и коморбидных состояний/заболеваний в форме отитов, синуситов, синдрома апноэ/гипопноэ сна, неврологической патологии и прочих нарушений, что диктует необходимость однозначного принятия решения об оперативном вмешательстве. В то же время возможен превентивный подход к решению прогноза течения заболевания: благоприятного или неблагоприятного с точки зрения эффективности консервативной терапии и риска оперативного вмешательства [1, 2]. Подход состоит в изучении нарушений физиологических иммунных процессов при ХА у детей, что убедительно продемонстрировано на примере других нозологий [3].
Цель – изучение разнофазного реагирования в системе провоспалительных и противовоспалительных цитокинов вследствие аддитивного вклада гомозиготных и гетерозиготных генотипов по полиморфным аллельным вариантам генов интерлейкина-1β и интерлейкина-4.
Материалы и методы исследования
В нашем исследовании у 388 детей мы проанализировали клинические проявления заболевания. Критериями включения являлись:
1) дети-пробанды с верифицированным диагнозом ХА (обоего пола, в возрасте от 3 до 10 лет,
2) проживание на территории определяемого для проведения исследования региона с рождения – г. Красноярск;
3) европеоидная расовая принадлежность;
4) состояние ремиссии при сопутствующих заболеваниях;
5) отсутствие терапии в течение предшествующего месяца;
6) подписанное родителями пациента информированное согласие на участие в исследовании и обработку персонифицированных данных;
7) способность пациента выполнять процедуры Протокола исследования.
Клиническое обследование включало анализ жалоб, анамнестических данных с уточнением давности заболевания и причин, способствующих развитию ХА, включая причины наследственной предрасположенности. Диагноз ХА устанавливался оториноларингологом по традиционным субъективным и объективным признакам. В обследовании участвовали аллерголог, педиатр. Дополнительно оценивали концептуальные субъективные и объективные признаки: дебют и стаж заболевания, возраст ребёнка на момент верификации диагноза, тяжесть течения, частоту и длительность манифестации ХА, характер осложнёний; степень гипертрофии глоточной миндалины, проявления аллергии, степень повышения температуры тела при ХА и/или ОРВИ, распространённость гипертрофии шейных лимфатических узлов.
В качестве факторов врождённого иммунитета было изучено распределение частот генотипов IL-1β и IL-4 во взаимосвязи с клиническими проявлениями и исходом ХА.Молекулярно-генетические исследования проведены 317/388 (81,7 %) детям с ХА.
Молекулярно-генетический метод включал 2 ДНК-маркёра 2-х генов: IL-1β (3954C → T), IL-4 (589С → T). Генотипирование проводили методом полимеразной цепной реакции в реальном времени с последующей амплификацией с использованием меченых флуоресцентными агентами олигонуклеотидных проб, комплиментарных участку ПЦР-продукта (технология TaqMan) ДНК образца крови больного ребёнка с использованием методов автоматической детекции. В каждый эксперимент включали отрицательный контроль, где ДНК-матрицу для ПЦР заменяли дистилированной водой (dH2О). Амплификация была выполнена в 50 µл объёме, содержащем 300 нг ДНК, 0,1 µл праймера, содержащего 16–25 пар нуклеотидов (Applied Biosystem part of Life Technologies, США). Используемые структурные дизайны праймеров для описания характеристик генов представлены согласно данным National Centerfor Biotechnology Information по референсу ОНП (rs – reference SNP, англ.) в соответствии с протоколом, прилагаемым к праймеру [4]:
1) для гена IL-1β (IL-1β +3954С/Т, rs1143634) –
CTCCACCTTTCAGAACCTATCTTCTT [C/T] GACACATGGGATAACGAGGCTTATG
2) для гена IL-4 (IL-4 -589C/T, rs2243250) –
AACACCTAAACTTGGGAGAACATTGT [C/T] CCCCAGTGCTGGGGTAGGAGAGTCT
ПЦР проводили в амплификаторе Rotor-Gene 6000 (Corbet Life Science, Австралия).
Молекулярно-генетическое обследование проводилось на базе Межкафедральной научно-исследовательской лаборатории медицинской генетики (заведующая – профессор, доктор медицинских наук Н.А. Шнайдер) кафедры медицинской генетики и клинической нейрофизиологии Института последипломного образования КрасГМУ.
Было проведено изучение ассоциированной с генотипом цитокинопродукции по уровню концентрации в сыворотке крови IL-1β, IL-4 методом твёрдофазного ИФА с применением пероксидазы хрена в качестве индикаторного фермента на базе сертифицированного Регионального лабораторно-диагностического центра иммуно-химических методов исследования г. Красноярска (директор – кандидат биологических наук А.В. Светлаков). Использовали сертифицированные тест-системы IL-1β, IL-4 (BioChemMackDiagnostics, Россия).
Статистическая обработка полученных данных выполнялась при помощи компьютерной программы «SPSS v. 22.0 for Windows». Статистический анализ включал сравнение зависимых и независимых рядов переменных и методы описательной статистики. Оценивался вид распределения. При нормальном распределении показатели представленысредними значениями истандартной ошибкой среднего (M ± m), при асимметричном распределении – медианой и интерквартильным размахом. Различия считали статистически значимыми при р ≤ 0,05.
Исследование проводилось в рамках реализации научно-исследовательской комплексной темы кафедры ЛОР-болезней с курсом последипломного образования «Трансляционная оториноларингология» (Государственная регистрация № 01201001212).
Каждый из трёх возможных вариантов генотипов ассоциировался с высокой, повышенной (условно адекватной) или низкой продукцией кодируемого цитокина.
Результаты исследования и их обсуждение
Наличие у индивида гомозиготных или гетерозиготных генотипов С/С и Т/Т гена IL-1β в локусе 3954 и гена IL-4 в локусе 589 характеризовалось генетически детерминированной цитокинопродукцией, формирующей фенотипический полиморфизм (табл. 1).
Для понимания разнофазного реагирования в системе оппозитных цитокинов при ХА у детей исходили из оценки наличия баланса или дисбаланса вариантов генотипов.Под балансом понимали факт равновесия между противоположными вариантами у здорового индивида для адекватного функционирования цитокиновой системы.
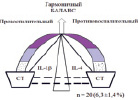
Наиболее сбалансированным являлось гетерозиготное носительство, которое всеобъемлюще было представлено в популяции в целом и позволяло индивидам приспосабливаться к условиям внешней среды. Так, комбинированное носительство гетерозиготных генотипов цитокинов IL-1β и IL-4 было выявлено лишь в 6,3 ± 1,4 % случаев у 20 больных детей (рисунок, А). Это можно было отнести к сбалансированному провоспалительному и противовоспалительному цитокиновому ответу в пределах возрастного референсного коридора, что согласовывалось с результатами лабораторного исследования цитокинопродукции.
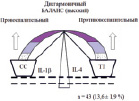
Несколько чаще у наблюдаемых детей регистрировался дисгармоничный баланс провоспалительного и противовоспалительного цитокинового ответа, который мы назвали высокий. Он заключался в комбинировании гомозиготного генотипа (СС) по высокопродуцирующему варианту провоспалительного цитокина IL-1β, приводящему к повышенной экспрессии гена и продукции данного интерлейкина, и гомозиготного генотипа (ТТ) по высокопродуцирующему варианту противовоспалительного цитокина IL-4, что сопровождалось повышенной экспрессией гена и продукции противовоспалительного IL-4. При этом мог достигаться определённый баланс между провоспалительным и противовоспалительным ответом. Однако с позиции полигенного взаимодействия и взаимного влияния мутаций генов других цитокинов, участвующих в этом ответе, такой баланс правильно считать дисгармоничным, поскольку он находится на верхней границе референсного коридора реактивности организма. При этом комбинированное носительство по высокопродуцирующим вариантам других провоспалительных цитокинов, например ИЛ-6, ИЛ-8 и т. д., привело бы к быстрому нарушению нестойкого дисгармоничного баланса и резкому повышению провоспалительного ответа, а также рецидивирующему или тяжёлому течению ХА. С другой стороны, такую же роль на состояние дисгармоничного генетического баланса могли оказывать и экзогенные факторы окружающей среды (например, уровень загрязнения атмосферного воздуха и т.д.). Дисгармоничный баланс (высокий) у наблюдаемых детей с ХА наблюдался в 13,6 ± 1,9 % случаев у 43 больных детей (рисунок, Б).
Таблица 1
Сопоставление генотипов генов цитокинов с уровнем экспрессируемых белков в сыворотке крови у детей-пробандов с хроническим аденоидитом (n = 317)
|
Ген цитокина, полиморфизм |
Генотипы |
Концентрация цитокинов, пг/мл Me [Q25; Q75] |
p ≤ 0,05 |
|
|
IL-1β локус 3954 |
С/С |
1 |
199,40 [190,28; 216,43] |
p1–2, p1–3 p2–3 |
|
С/Т |
2 |
158,35 [66,88; 177,99] |
||
|
Т/Т |
3 |
129,80 [113,50; 155,74] |
||
|
IL-4 локус 589 |
С/С |
1 |
139,40 [134,16; 149,30] |
p1–2, p1–3 p2–3 |
|
С/Т |
2 |
187,70 [141,10; 200,50] |
||
|
Т/Т |
3 |
216,54 [206,40; 247,20] |
||
Примечание. p – статистическая значимость при сравнении концентрации цитокина, детерминируемого одним геном и локусом.
А) Б) В)
Г) Д)
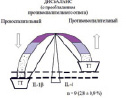
Генетический и фенотипический баланс состояния иммунного цитокинового ответа при хроническом аденоидите у наблюдаемых детей (n = 317). Примечания: группы аддитивного риска:  – низкий риск,
– низкий риск,  – средний риск,
– средний риск,  – высокий риск; пунктирная линия – референсный интервал допустимого цитокинового ответа (в пределах нормы)
– высокий риск; пунктирная линия – референсный интервал допустимого цитокинового ответа (в пределах нормы)
Таблица 2
Клинико-генетическая гетерогенность хронического аденоидита у детей
|
Критерий |
Баланс |
Баланс дисгармоничный |
Дисбаланс |
||
|
Высокий |
Низкий |
Провоспалительный |
Противовоспалительный |
||
|
Частота (M ± m, %) |
6,3 ± 1,4 |
13,6 ± 1,9 |
7,9 ± 1,5 |
35,0 ± 2,7 |
2,8 ± 0,9 |
|
Возраст дебюта (лет) |
4 |
2,8 |
3,2 |
2,4 |
3,2 |
|
Характер течения |
Лёгкой Средней тяжести, Типичное |
Средней тяжести Рецидивирующее С частыми обострениями, осложнениями |
Средней тяжести Рецидивирующее Затяжное |
Тяжёлое Агрессивное С частыми обострениями осложнениями |
Тяжёлое Рецидивирующее Затяжное |
|
Прогноз |
Благоприятный |
Неблагоприятный |
Благоприятный |
Неблагоприятный |
Неблагоприятный |
|
Форма |
Гнойная |
Отёчно- катаральная |
Гнойная |
Гнойная |
Отёчно- катаральная |
|
Гипертрофия глоточной миндалины (степень) |
I–III |
II–III |
II |
II–III |
II |
|
Сатурация крови (Me, %) |
96 |
88 |
91 |
84 |
90 |
|
Нарушение ритма при респираторном событии (риск брадикардии) |
Низкий |
Средний Аритмия |
Средний |
Высокий Аритмия |
Высокий |
|
Сопряжённая патология ЛОР-органов |
Низкий |
Высокий |
Средний |
Высокий |
Высокий |
|
Параинфекционные неврологические симптомы (риск) |
|||||
|
Тип полиморфизма IL-1β/IL-4 |
СТ/СТ |
СС/ТТ |
ТТ/СС |
СС/СС |
ТТ/ТТ |
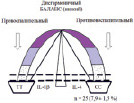
Второй вариант дисгармоничного баланса по изучаемым полиморфным аллельным вариантам заключался в комбинации гомозиготного генотипа (ТТ) по низкопродуцирующему варианту цитокина IL-1β, приводящему к снижению экспрессии гена и снижению продукции этого интерлейкина, и гомозиготного генотипа (СС) по низкопродуцирующему варианту противовоспалительного цитокина IL-4, обуславливающему снижение экспрессии гена и продукции IL-4.
В этом случае баланс также достигался, но по нижней границе референсного коридора реактивности и также являлся дисгармоничным за счёт полигенного влияния других провоспалительных и противовоспалительных цитокинов и влияния экзогенных факторов окружающей среды. Частота встречаемости второго варианта дисгармоничного баланса цитокинового ответа у наблюдаемых нами детей с ХА отмечалась статистически значимо реже по сравнению с первым вариантом дисгармоничного баланса у 25 детей (7,9 ± 1,5 %) (рисунок, В).
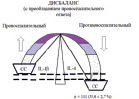
Нарушение баланса с преобладанием провоспалительного и снижением противовоспалительного ответа расценивалось как дисбаланс и встречалось в исследованной группе статистически значимо чаще в 35,0 ± 2,7 % случаев (n = 111). Заключался дисбаланс в комбинированном носительстве гомозиготного генотипа (СС) по высокопродуцирующему варианту гена IL-1β и гомозиготного генотипа (СС) по низкопродуцирующему варианту IL-4 (рисунок, Г).
Контраверсивный вариант дисбаланса подразумевал преобладание противовоспалительного и снижение провоспалительного ответа. Заключался дисбаланс в комбинированном носительстве гомозиготного генотипа (ТТ) по низкопродуцирующему полиморфному аллельному варианту гена IL-1β и гомозиготного генотипа (ТТ) по высокопродуцирующему варианту гена IL-4 (рисунок, Д). Данный вариант констатирован в 2,8 ± 0,9 % случаев (n = 9).В целом иллюстрация наглядно представляет генетическую гетерогенностьиммунного цитокинового ответа при хроническом аденоидите у детей.
Возможны промежуточные комбинации гомозиготных и гетерозиготных вариантов генетического и фенотипического дисбаланса состояния провоспалительного и противовоспалительного цитокинового ответа при ХА у детей. Но пределы колебаний ответа находились в пределах вариантов описанного дисбаланса. При этом акцент ставится на то, что процент детей с ХА, с несоответствующим балансом, составил 93,7 %, что, по сути, представляло доверительный интервал.
Вашему вниманию мы представляем клинико-генетическую характеристику хронического аденоидита с мультисистемными проявлениями, предопределяющую благоприятное или неблагоприятное течение заболевания (табл. 2). В частности, баланс иммунного цитокинового ответа подразумевал поздний дебют, пролонгированный стаж заболевания до развития осложнений, малую частоту осложнений, типичный характер с частотой 4 раза в год.
Крайне неблагоприятным являлся дисбаланс с преобладанием противовоспалительного ответа, т.к. характеризовался активным, тяжёлым, агрессивным, с частыми осложнениями и обострениями течением. Другие варианты имели рецидивирующее течение, склонное к затяжным случаям с вариабельными признаками. Высокий баланс подразумевал ранний дебют, локальные и системные проявления атопии, рецидивирующее течение в отёчно-катаральной форме, с риском формирования параинфекционных неврологических осложнений.
Заключение
Таким образом, современные достижения молекулярной и клинической генетики свидетельствуют о клинико-генетической неоднородности ХА. Тщательный анализ функционирования генов цитокинов позволил установить их роль и место в диагностике мультифакториального заболевания, в частности, ХА у детей, и применения в прикладной оториноларингологии, что ранее оставалось за пределами клинической интерпретации исследователей и интеграции в существующую практику.
Рецензенты:
Дмитренко Д.В., д.м.н., доцент, доцент кафедры медицинской генетики и клинической нейрофизиологии Института последипломного образования, ГБОУ ВПО «Красноярский государственный медицинский университет имени профессора В.Ф. Войно-Ясенецкого» Министерства здравоохранения Российской Федерации, г. Красноярск;
Винник Ю.С., д.м.н., профессор кафедры хирургии им. профессора М.И. Гульмана, ГБОУ ВПО «Красноярский государственный медицинский университет им. профессора В.Ф. Войно-Ясенецкого», г. Красноярск.



