Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
REALDIRONE IMMUNOMODULING ACTIVITY IN TOXIC DAMAGE OF THE LIVER
Токсическое поражение печени – частое побочное действие химиотерапии онкозаболеваний, существенно ограничивающее достижение максимального терапевтического эффекта цитостатической терапии.
Токсическая гепатопатия нередко усугубляет иммуносупрессию, связанную с опухолевым ростом и применением цитостатиков. Предупреждение и лечение такой комбинированной иммунодепрессии представляет сложную клиническую задачу, поэтому нуждается в экспериментальных исследованиях.
Поражение печени тетрахлорметаном (ТХМ) – классическая модель токсического поражения печени [10, 13]. Особого внимания заслуживает проблема коррекции повреждающего воздействия ТХМ на фагоцитарное звено, поскольку оно осуществляет неспецифическую защиту организма, реагирует на малейшие изменения состояния организма, а также активно участвует в процессах как врожденного, так и приобретенного иммунитета, что позволяет использовать фагоцитарные реакции в качестве индикатора для оценки состояния всей иммунной системы в целом [4, 6].
Состояние нейтрофилов и мононуклеарных фагоцитов представляет особый интерес еще и потому, что в последние годы их деятельности отводится немаловажная роль в процессах репаративной регенерации печени [11, 14, 15].
В связи с этим целью исследования явилось изучение эффективности реальдирона (рекомбинантный альфа – 2b интерферон), обладающего способностью стимулировать мононуклеарные фагоциты, а также собственной противоопухолевой активностью, для коррекции иммунотоксических эффектов ТХМ [2].
Материалы и методы исследования
Эксперименты выполнены на 90 белых неинбредных крысах массой 180–200 г, содержавшихся в стандартных условиях вивария. Животные были разделены на 3 группы (по 10 животных в группе): контроль, ТХМ, ТХМ+Р (реальдирон). Животным на протяжении 4 суток (в – 4, – 3, – 2 и – 1 дни) вводили ТХМ внутрижелудочно в дозе 1,25 мл/кг 50 % раствора в оливковом масле [5]. Реальдирон вводили в дозе 100 000 ЕД на крысу [3] внутримышечно 3-кратно (в 0, 3 и 6 дни) после окончания введения токсиканта.
Животные содержались в стандартных условиях вивария с естественным световым режимом, на стандартной диете лабораторных животных (ГОСТР 50258-92), с соблюдением Международных рекомендаций Европейской конвенции по защите позвоночных животных, используемых при экспериментальных исследованиях, а также правил лабораторной практики при проведении доклинических исследований в РФ (ГОСТ З 51000.3-96 и 51000.4-96) и Приказу МЗ РФ № 267 от 19.06.2003 г. «Об утверждении правил лабораторной практики» (GLP).
Определяли количество лейкоцитов, нейтрофилов и лимфоцитов в периферической крови, интенсивность кислородзависимого метаболизма (спонтанный и индуцированный НСТ-тест), поглотительную способность полиморфноядерных лейкоцитов (ПМЯЛ) и перитонеальных макрофагов (ПМФ), антимикробную активность ПМЯЛ и ПМФ в условиях функционирования и блокады (азидом натрия) кислородзависимых факторов микробицидности в отношении грибов Candida albicans, активность миелопероксидазы (МП) и содержание катионных белков (КБ) в фагоцитах [7, 9]. Результаты регистрировали на 7, 14 и 28 сутки.
Статистическую обработку проводили с использованием методов вариационной статистики [1], пакета программ Statistica 8.0. Проверку на нормальность распределения данных выполняли с помощью критерия Шапиро-Вилка. Оценку значимости различий проводили, вычисляя медиану и межквартильный интервал. Дисперсионный анализ проводили с помощью Н-критерия Краскела-Уоллиса, для множественных сравнений использован Q-критерий Дана. Критический уровень значимости р для статистических критериев принимали равным 0,05.
Данные в тексте представлены в процентах к контролю (неинбредные животные).
Результаты исследования и их обсуждение
Воздействие ТХМ приводило на 7 сутки к глубокой лейкопении (до 60,68 %, р = 0,0328), формирование которой было обусловлено снижением числа лимфоцитов (до 52,58 %, р = 0,0008). Наблюдалось глубокое угнетение как оксидантных, так и неоксидантных микробицидных систем ПМЯЛ. Так, интенсивность кислородзависимого киллинга снизилась почти в 2 раза (индекс инактивации (ИИ) составил 59,47 %), что цитохимически подтверждалось снижением активности МП ПМЯЛ (табл. 1). Это сопровождалось усилением кислородзависимого метаболизма в спонтанном НСТ-тесте, что отражает тяжесть токсического воздействия ТХМ. В то же время в условиях индукции отмечено снижение интенсивности оксидантного метаболизма ПМЯЛ (индуцированный НСТ-тест): ПА лат – 72,58 % (р = 0,6282), ИА лат – 71,53 % (р = 0,2228), что отражает снижение резервного потенциала нейтрофилов.
Полученные данные могут свидетельствовать об угнетении как пероксидазозависимых, так и пероксидазонезависимых факторов оксидантного киллинга ПМЯЛ при воздействии ТХМ.
В условиях блокады оксидантных механизмов микробицидности азидом натрия ИИ снизился более чем в 2,5 раза (ИИ – 48,70 %), а цитохимически наблюдалось почти трехкратное снижение уровня КБ в ПМЯЛ (табл. 2). Отмечено и снижение поглотительной способности ПМЯЛ.
Мононуклеарные фагоциты оказались более устойчивыми к действию ТХМ: на 7 сутки наблюдалось угнетение только неоксидантного киллинга ПМФ (ИИ – 75,59 %), что цитохимически сопровождалось снижением уровня КБ в ПМФ.
Применение реальдирона ослабило выраженность лейкопении за счет увеличения числа нейтрофилов (до 134,76 %, p = 0,0023) при сохранявшейся лимфопении (количество лимфоцитов составило 52,82 %, p = 0,0004), а также в 1,5 раза (по отношению к ТХМ) повысило активность неоксидантных микробицидных систем ПМЯЛ (ИИ – 62,34 %). Цитохимически это проявилось двукратным (по отношению к ТХМ) повышением уровня КБ в нейтрофилах (табл. 2).
На 14 сутки сохранялась индуцированная ТХМ лейкопения (65,37 %, р = 0,0002), формирование которой было уже связано со снижением числа как нейтрофилов, так и лимфоцитов (до 62,82 % (р = 0,0021) и 67,64 % (р = 0,0002) соответственно).
Как и на 7 сутки, наблюдалась депрессия кислородзависимых механизмов киллинга ПМЯЛ (ИИ – 63,23 %), что сопровождалось подавлением кислородзависимого метаболизма ПМЯЛ (индуцированный НСТ-тест) и активности МП (табл. 1). В условиях блокады оксидантных механизмов фунгицидность ПМЯЛ несколько повышалась (по сравнению с 7-ми сутками), хотя оставалась сниженной (ИИ – 63,23 %), как и уровень КБ в нейтрофилах (табл. 2).
Воздействие ТХМ привело на 14 сутки к подавлению оксидантных факторов микробицидности ПМФ (ИИ – 86,93 %), что сочеталось со снижением интенсивности кислородзависимого метаболизма ПМФ как в спонтанном, так и в индуцированном НСТ-тесте. Это свидетельствует о существенном истощении резервного потенциала ПМФ и способности к образованию активных форм кислорода, которым, как известно, принадлежит ведущая роль в механизмах оксидантного киллинга ПМФ. Также наблюдалось снижение активности МП в мононуклеарных фагоцитах: процент МП – позитивных макрофагов составил 67,92 % (р = 0,0009), а СЦК – 72,19 % (р = 0,0022).
Таблица 1
Влияние тетрахлорметана и его комбинации с реальдироном на активность миелопероксидазы в ПМЯЛ (СЦК, в % к контролю)
|
Сутки наблюдения |
ТХМ |
ТХМ + Р |
|
7 |
70,24 [53,57–73,81] Р1 = 0,0003 |
75,60 [70,83–80,95] |
|
14 |
77,14 [72,86 – 82,86] Р1 = 0,0010 |
88,57 [82,86–100,0] |
|
28 |
72,12 [67,31–94,23] |
117,31 [101,92–125,0] Р2 = 0,0040 |
Примечание. Достоверность отличий Р1 – от контроля, Р2 – от ТХМ.
Таблица 2
Влияние тетрахлорметана и его комбинации с реальдироном на содержание катионных белков в ПМЯЛ (СЦК, в % к контролю)
|
Сутки наблюдения |
ТХМ |
ТХМ+Р |
|
7 |
38,95 [35,79–43,16] Р1 << 0,00001 |
78,95 [69,47–88,42] Р2 = 0,0104 |
|
14 |
69,05 [64,29–72,62] Р1 = 0,0228 |
116,67 [114,29–125,0] Р2 = 0,0001 |
|
28 |
74,04 [69,23–76,92] Р1 = 0,0001 |
92,31 [86,54–98,08] Р2 = 0,0164 |
Примечание. Достоверность отличий Р1 – от контроля, Р2 – от ТХМ.
Сохранялась депрессия ТХМ неоксидантного киллинга мононуклеаров (ИИ составил 77,06 %), что сопровождалось снижением содержания КБ в ПМФ: процент КБ – положительных клеток составил 59,69 (р = 0,0082) %, а СЦК – 64,08 % (р = 0,0368). На 14 сутки наблюдалось увеличение как количества ПМФ, участвующих в фагоцитозе, так и их поглотительной способности: ФЧ составило 127,94 % (р = 0,2698), а ФИ – 131,67 % (р = 0,0012).
Использование реальдирона (14 сутки) полностью восстанавливало активность оксидантных и неоксидантных микробицидных систем ПМЯЛ (ИИ составил 103,23 % и 114,73 % соответственно). При этом реальдирон устранял депрессию ТХМ кислородзависимого метаболизма ПМЯЛ. Это согласуется с данными других авторов об активирующем влиянии реальдирона на оксидантный метаболизм нейтрофильных гранулоцитов, и может свидетельствовать о повышении резервного потенциала ПМЯЛ [8, 12].
Реальдирон устранял депрессию активности МП в ПМЯЛ (табл. 1). Следовательно, применение реальдирона обеспечивало повышение активности пероксидазозависимых и пероксидазонезависимых оксидантных механизмов киллинга ПМЯЛ.
Восстановление активности неоксидантных факторов микробицидности ПМЯЛ (ИИ – 114,73 %) под влиянием реальдирона (14-е сутки) сопровождалось двукратным (по сравнению с 7 сутками) повышением уровня КБ в ПМЯЛ (табл. 2).
Реальдирон снижал до нормы число фагоцитирующих ПМЯЛ (ФЧ – 90,0 %, р = 1,00) при восстановлении их поглотительной активности (ФИ – 89,39 %, р = 1,00).
На 14-е сутки реальдирон устранял индуцированную ТХМ депрессию как кислородзависимых, так и кислороднезависимых механизмов микробицидности ПМФ (ИИ составил 100,15 % и 132,97 % соответственно). Восстанавливались интенсивность оксидантного метаболизма, уровень МП и КБ в мононуклеарных фагоцитах.
Реальдирон снижал до нормы число ПМФ, участвующих в фагоцитозе (ФЧ – 85,29 %, р = 0,1324) при сохранении их поглотительной способности на уровне интактных животных (ФИ – 93,33 %, р = 1,0).
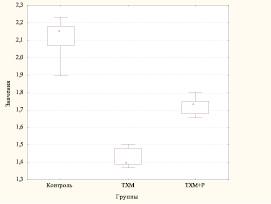 А)
А)
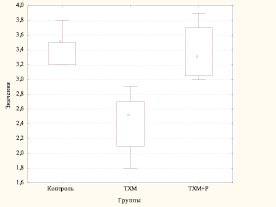 Б)
Б)
Влияние ТХМ и его комбинации с реальдироном на содержание КБ (СЦК) (А) и поглотительную способность (ФИ) (Б) в ПМФ (28 сутки наблюдения)
К 28 суткам после интоксикации ТХМ выраженность лейкопении уменьшалась (76,44 %, р = 0,2165) за счет повышения до нормы числа лимфоцитов (83,75 %, p = 0,7144) при сохранявшейся нейтропении (61,25 %, p = 0,0005). Микробицидность ПМЯЛ как в условиях функционирования, так и блокады кислородзависимых механизмов повышалась, но не восстанавливалась (ИИ составил 79,19 % и 75,53 % соответственно). Это согласовалось с глубоким снижением активности оксидантного метаболизма и МП в нейтрофильных гранулоцитах (табл. 1).
Усугублялась депрессия токсикантом кислороднезависимых факторов микробицидности ПМФ (ИИ составил 60,52 %), что подтверждалось снижением уровня КБ в них: процент КБ – положительных клеток составил 68,0 % (p<<0,00001), а СЦК – 64,65 % (p<<0,00001). На 28-е сутки сохранялось увеличение числа ПМФ, участвующих в фагоцитозе (ФЧ – 123,53 %, р = 1,00) при значимом снижении их поглотительной способности (ФИ – 71,43 %, р = 0,0430).
На 28 сутки сохранялись индуцированные токсикантом лейкопения (68,44 %, р = 0,1093), обусловленная снижением числа лимфоцитов (до 69,17 %, р = 0,0652).
На 28-е сутки, так же, как и на 14-е сутки, реальдирон устранял депрессию токсикантом кислородзависимых и кислороднезависимых факторов микробицидности ПМЯЛ (ИИ составил 101,16 % и 110,97 % соответственно). Восстанавливался оксидантный метаболизм ПМЯЛ и повышалась активности МП ПМЯЛ (табл. 1), что свидетельствует об активации реальдироном пероксидазозависимых и пероксидазонезависимых механизмов киллинга ПМЯЛ.
Восстановление активности неоксидантных механизмов киллинга ПМЯЛ подтверждалось повышением до нормы уровня КБ в них (табл. 2). Реальдирон нормализовал поглотительную способность в нейтрофилах.
На 28-е сутки реальдирон восстанавливал активность оксидантных механизмов киллинга ПМФ (ИИ – 103,76 %) за счет повышения активности кислородзависимого метаболизма ПМФ, что свидетельствует об активации реальдироном пероксидазонезависимых оксидантных микробицидных систем ПМФ.
В то же время применение реальдирона не устраняло вызванное ТХМ угнетение неоксидантных механизмов киллинга ПМФ (ИИ – 76,01 %). Однако цитохимически наблюдалось повышение (по отношению к ТХМ) уровня КБ в ПМФ (рис. А).
Использование реальдирона снижало число ПМФ, участвующих в фагоцитозе, при повышении до нормы их поглотительной активности (рис. Б).
Заключение
Таким образом, воздействие ТХМ на организм, которое рассматривается как экспериментально-химический стресс [Халимов], приводит к формированию глубокой лейкопении, угнетению микробицидности фагоцитов, особенно в условиях блокады оксидантного киллинга (что коррелирует со снижением в них активности миелопероксидазы и уровня катионных белков). Применение реальдирона существенно корректирует/нивелирует повреждающее действие ТХМ на клетки фагоцитарного звена: восстанавливает микробицидность фагоцитов, что сопровождается повышением в них оксидантного метаболизма, активности миелопероксидазы и уровня неферментных катионных белков, а также предупреждает падение их поглотительной способности.
Рецензенты:
Медведев Ю.А., д.м.н., профессор, старший научный сотрудник лаборатории № 9 Научно-исследовательского технологического института гербицидов и регуляторов роста растений Академии наук республики Башкортостан, г. Уфа;
Сакаева Д.Д., д.м.н., заместитель главного врача по химиотерапии ГБУЗ «Республиканского клинического онкологического диспансера» Министерства здравоохранения республики Башкортостан, г. Уфа.
Библиографическая ссылка
Муфазалова Н.А., Муфазалова Л.Ф., Мухаметзянова А.Я., Батракова К.В. ИММУНОМОДУЛИРУЮЩАЯ АКТИВНОСТЬ РЕАЛЬДИРОНА ПРИ ТОКСИЧЕСКОМ ПОРАЖЕНИИ ПЕЧЕНИ // Фундаментальные исследования. 2015. № 1-5. С. 1013-1018;URL: https://fundamental-research.ru/en/article/view?id=37507 (дата обращения: 04.06.2026).



