Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
PROBABILISTIC AND STATISTICAL APPROACHES WHEN PREDICTING PH VALUE OF PRODUCED WATER WESTERN SIBERIA VERTICAL STEEL TANKS
Магистральная нефть содержит в себе растворенную воду с различными химическими примесями. Технически и экономически целесообразно подвергать нефть специальной подготовке перед подачей в магистральный нефтепровод, в том числе производить ее обезвоживание. И хотя массовая доля воды в нефти регламентируется согласно [1], процесс обезвоживания затрудняется тем, что нефть и вода образуют стойкие эмульсии типа «вода в нефти», поэтому вода диспергирует в нефтяной среде на мельчайшие капли, образуя стойкую эмульсию. На практике несмотря на применение на промыслах таких технологических процессов, как гравитационный отстой нефти, горячий отстой нефти, термохимические методы, электрообессоливание и электрообезвоживание нефти, магистральная нефть все же содержит в себе растворенную подтоварную воду. По пути следования магистральной нефти в различных случаях возникает необходимость в ее хранении, для чего используются различные емкости, в частности самые распространенные – вертикальные стальные резервуары. При так называемом ответственном хранении нефть отстаивается, в результате чего в силу физических законов подтоварная вода как вещество с большей плотностью, чем другие составляющие нефти, оседает на дно резервуара, образуя некоторый слой.
По российским нормативным документам, в частности [1], массовая доля воды составляет не более 0,5 % для первой и второй групп нефти и не более 1,0 % для третьей группы. Так, при содержании одного процента воды в объеме хранимой нефти РВС-20000, глубина слоя подтоварной воды составит 32 мм.
По наблюдениям специалистов и в проведенных ранее исследованиях [2] было установлено, что в основном коррозия встречается на уровне первого пояса резервуара для товарной нефти, причем особенно глубокие повреждения оказываются лишь на расстоянии до 20 см от уровня уторного шва по первому поясу стенки. Кроме того, окрайка и днище резервуара также подвержены сильному коррозионному износу, что подтверждается частой заменой металлоконструкций этих элементов при капитальных ремонтах. Основной причиной такого расположения коррозионных повреждений является наличие на этих уровнях подтоварной воды. Подтоварная вода представляет собой набор химических веществ и соединений, растворенных в чистой воде. Ее химический анализ проводят, руководствуясь нормативными документами для сточных вод, в том числе [10]. В них нормируется содержание таких анионов, как иодиды (J–), иодаты (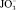 ), хлориды (Cl–), карбонаты (
), хлориды (Cl–), карбонаты (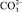 ), гидрокарбонаты (
), гидрокарбонаты (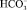 ), и некоторых катионов, – сумму ионов кальция и магния (Ca2+ + Mg2+). Кроме того, определяются основные физико-химические свойства: прозрачность, осадок, запах и уровень pH. Появившиеся в последнее время измерительные системы позволили существенно расширить перечень измеряемых параметров определяемых компонентов раствора. Имеющиеся в подтоварной воде химические вещества и соединения значительно ускоряют коррозионные процессы системы вследствие повышения электропроводности электролита (воды). Известно, что способность изотермической среды к коррозионному воздействию однозначно определяется значениями водородного показателя pH и окислительно-восстановительного потенциала (редокс-потенциала) Eh. Таким образом, если известны значения температуры, рН и Еh, то можно выяснить, в какой форме будет находиться тот или иной металл при контакте с водой. Для определения вероятности попадания pH подтоварной воды в интервал допустимых значений была выполнена статистическая обработка данных. В выборку входили 102 пробы подтоварной воды магистральной нефти из резервуаров Западной Сибири (Среднее Приобье). Известно, что водородный показатель водной среды в основном принимает значения от 0 до 14. В результате измерений минимальная установленная величина pH составляет 4,5, максимальная величина pH = 10,5. Поэтому цена деления шкалы pH составила 0,5 единицы. Проанализировав данные химического анализа подтоварной воды, произвели расчет частоты попадания (w) в тот или иной интервал значений водородного показателя. Как уже отмечалось, всего было взято 102 пробы (n = 102). Рассчитана частота попадания в интервал (w/n), соответствующая вероятности наступления события (Px) (таблица):
), и некоторых катионов, – сумму ионов кальция и магния (Ca2+ + Mg2+). Кроме того, определяются основные физико-химические свойства: прозрачность, осадок, запах и уровень pH. Появившиеся в последнее время измерительные системы позволили существенно расширить перечень измеряемых параметров определяемых компонентов раствора. Имеющиеся в подтоварной воде химические вещества и соединения значительно ускоряют коррозионные процессы системы вследствие повышения электропроводности электролита (воды). Известно, что способность изотермической среды к коррозионному воздействию однозначно определяется значениями водородного показателя pH и окислительно-восстановительного потенциала (редокс-потенциала) Eh. Таким образом, если известны значения температуры, рН и Еh, то можно выяснить, в какой форме будет находиться тот или иной металл при контакте с водой. Для определения вероятности попадания pH подтоварной воды в интервал допустимых значений была выполнена статистическая обработка данных. В выборку входили 102 пробы подтоварной воды магистральной нефти из резервуаров Западной Сибири (Среднее Приобье). Известно, что водородный показатель водной среды в основном принимает значения от 0 до 14. В результате измерений минимальная установленная величина pH составляет 4,5, максимальная величина pH = 10,5. Поэтому цена деления шкалы pH составила 0,5 единицы. Проанализировав данные химического анализа подтоварной воды, произвели расчет частоты попадания (w) в тот или иной интервал значений водородного показателя. Как уже отмечалось, всего было взято 102 пробы (n = 102). Рассчитана частота попадания в интервал (w/n), соответствующая вероятности наступления события (Px) (таблица):
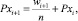 (1)
(1)
где Pxi + 1 – вероятность попадания значения в интервал (i + 1); Pxi – вероятность попадания значения в интервал (i); wi + 1 – частота попадания в интервал (i + 1); n – общее число экспериментальных значений.
Распределение значений pH подтоварной воды
|
Кислая среда (pH < 7) |
Значение pH |
Частота попадания (w) |
Накопленная частость (w/n)∙100 % |
Вероятность, Px |
|
3,5 |
1 |
0,98 % |
0,0098 |
|
|
4 |
1 |
0,98 % |
0,0098 |
|
|
4,5 |
3 |
2,94 % |
0,0294 |
|
|
5 |
7 |
6,86 % |
0,0686 |
|
|
5,5 |
9 |
8,82 % |
0,0882 |
|
|
6 |
17 |
16,67 % |
0,1667 |
|
|
6,5 |
21 |
20,59 % |
0,2059 |
|
|
7 |
16 |
15,69 % |
0,1569 |
|
|
Щелочная среда (pH > 7) |
7,5 |
12 |
11,76 % |
0,1176 |
|
8 |
7 |
6,86 % |
0,0686 |
|
|
8,5 |
3 |
2,94 % |
0,0294 |
|
|
9 |
1 |
0,98 % |
0,0098 |
|
|
9,5 |
2 |
1,96 % |
0,0196 |
|
|
10 |
1 |
0,98 % |
0,0098 |
|
|
10,5 |
1 |
0,98 % |
0,0098 |
|
|
∑ |
102 |
100 % |
1,0000 |
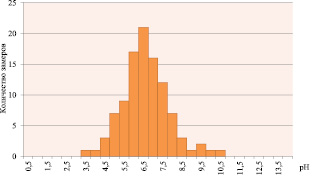
Рис. 1. Гистограмма распределения замеров подтоварной воды по уровню pH
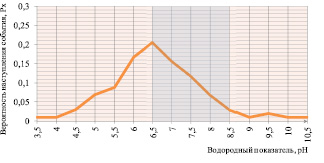
Рис. 2. Вероятностное распределение значений уровня кислотности подтоварной воды
Гистограмма распределения замеров подтоварной воды по уровню pH приведена на рис. 1.
Прогнозирование значения водородного показателя подтоварной воды резервуаров Западной Сибири выполнено в статистической постановке.
Используя значения таблицы, построена диаграмма (рис. 2).
Среднее значение вероятности (математическое ожидание MpH) определяется формулой
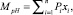 (2)
(2)
где n – общее количество введенных экспериментальных значений; Pi – вероятность наступления события i; xi – значение водородного показателя для каждого события i.
Для поставленной задачи математическое ожидание является средним значением уровня кислотности с учетом вероятностного распределения и составляет 6,63 pH.
Таким образом, суммируя вероятности, мы можем утверждать, что лишь в 57 % случаев подтоварная вода удовлетворяет требованиям нормативных значений, в 20 % случаев водородный показатель равен 6,63 pH, в 42 % случаев подтоварная вода является кислой средой с уровнем pH < 7. В каждом конкретном случае можно проследить коррозионное поведение металла по диаграмме Пурбе, построенной в координатах равновесный потенциал Eh – pH среды при обычной температуре. Диаграмма Пурбе обобщает химию водных растворов элементов и в сжатой и наглядной форме позволяет однозначно определить область коррозионной устойчивости металла, в которой его окисление невозможно термодинамически, а также прогнозировать область пассивного и коррозионно-активного состояния металла. Диаграмма Пурбе характеризует равновесное состояние металла в указанных условиях. На рис. 3 представлена диаграмма Еh – рН, характеризующая химию водных растворов кислородсодержащих соединений железа.
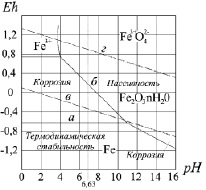
Рис. 3. Диаграмма Пурбе для устойчивости соединений железа в воде
Здесь сплошными линиями обозначены границы полей устойчивости. Так, горизонтальная линия «a» показывает потенциал равновесия:
Fe ↔ Fe2+ + 2e.
Наклонная линия «б» характеризует равновесие между ионами двухвалентного железа в растворе и твердой окисью железа, т.е. отражает условия возникновения твердых нерастворимых продуктов коррозии:
2Fe2+ + 3H2O ↔ Fe2O3 + 6H+ + 2e.
Выше этой линии находится область пассивности, где металл термодинамически неустойчив, но коррозионный процесс не развивается благодаря образованию на его поверхности нерастворимых продуктов. Вторая область коррозии, располагающаяся справа, соответствует образованию ферритов железа в сильнощелочных растворах. Верхняя пунктирная наклонная прямая «г» характеризует равновесие воды в зоне окисления:
1/2O2 + H2O ↔ 2OH–,
а нижняя «в» – равновесие воды в зоне восстановления:
H+ + e ↔ 1/2H2.
Можно заключить, что если при определенном ранее наиболее вероятном потенциале подтоварной воды, равном 6,63 pH, окислительно-восстановительный потенциал Eh примет одно из значений от –0,6 до 0,2 В, то будут активно протекать процессы электрохимической коррозии. При значениях Eh ниже –0,6 достигается термодинамическая стабильность системы, коррозионные процессы останавливаются. При Eh более 0,2 В металл становится термодинамически неустойчивым, но на поверхности образуются нерастворимые соединения, препятствующие проникновению агрессивной среды, а значит, и замедляющих коррозионные процессы.
Стоит отметить, что коррозионную активность металла можно определить при любом значении Eh и Ph, а полученные значения приблизительны, поскольку в состав стали кроме железа входит около 3 % легирующих элементов.
Выводы
1. Получена гистограмма распределения замеров подтоварной воды по уровню pH, характеризующая опасность развития коррозионных процессов в вероятностной постановке для нефтей Среднего Приобья.
2. Установлено, что в 57 % случаев подтоварная вода удовлетворяет требованиям нормативных значений, в 20 % случаев водородный показатель равен 6,63 pH, в 42 % случаев подтоварная вода является кислой средой с уровнем pH < 7.
3. При определенном ранее наиболее вероятном потенциале подтоварной воды, равном 6,63 pH, окислительно-восстановительный потенциал Eh примет одно из значений от –0,6 до 0,2 В, что ведет к активному протеканию процессов электрохимической коррозии. При значениях Eh ниже –0,6 достигается термодинамическая стабильность системы, коррозионные процессы останавливаются. При Eh более 0,2 В металл становится термодинамически неустойчивым, но на поверхности образуются нерастворимые соединения, препятствующие проникновению агрессивной среды, а значит, и замедляющих коррозионные процессы.
4. Все расчеты выполнены для отключенной системы электрохимической защиты, заземления, молниезащиты и пр. При наличии дополнительных потенциалов при эксплуатации резервуаров необходимо вносить корректировки в выполняемые расчеты. Авторы рекомендуют получать величину потенциалов экспериментальным путем, поскольку в реальном резервуаре происходит смешение потенциалов разных происхождений.
Рецензенты:Обухов А.Г., д.ф.-м.н., профессор кафедры «Высшая математика», ФГБОУ ВПО «Тюменский государственный нефтегазовый университет», г. Тюмень;
Мерданов Ш.М., д.т.н., профессор, зав. кафедрой «Транспортные и технологические системы», ФГБОУ ВПО «Тюменский государственный нефтегазовый университет», г. Тюмень.
Работа поступила в редакцию 18.03.2015.
Библиографическая ссылка
Тарасенко М.А., Чепур П.В., Тарасенко А.А. ВЕРОЯТНОСТНО-СТАТИСТИЧЕСКИЙ ПОДХОД ПРИ ПРОГНОЗИРОВАНИИ ЗНАЧЕНИЙ ВОДОРОДНОГО ПОКАЗАТЕЛЯ ПОДТОВАРНОЙ ВОДЫ ВЕРТИКАЛЬНЫХ СТАЛЬНЫХ РЕЗЕРВУАРОВ ЗАПАДНОЙ СИБИРИ // Фундаментальные исследования. 2015. № 2-10. С. 2129-2133;URL: https://fundamental-research.ru/en/article/view?id=37369 (дата обращения: 16.05.2026).



