Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
A STUDY OF PSYCHOTROPIC ACTIVITY OF DERIVATIVES OF ARYL(HYDRAZINOCARBONYLMETHYL)PHOSPHINIC ACIDS
Производные фосфорилированных карбоновых кислот, содержащие четырехкоординированный атом фосфора в составе фосфорильного фрагмента, привлекают внимание исследователей в качестве потенциальных психотропных препаратов [1, 5, 6, 7]. С целью оптимизации скрининга фармакологически активных веществ все шире используются методы компьютерного прогнозирования [2, 3, 11].
Проведенными ранее исследованиями было установлено, что компьютерная программа PASS (Prediction of Activity Spectra for Substances) [10] перспективна для прогноза психотропной активности гидразиниевых солей фосфорилированных карбоновых кислот и выявлена ведущая роль фосфорильного фрагмента в реализации мнемотропной и антидепрессивной активности [9]. В данном исследовании в результате компьютерного дизайна химической структуры и прогноза психотропной активности 47 новых производных арил(гидразинокарбонилметил)фосфиновых кислот (АГКМФК) были синтезированы 16 наиболее перспективных соединений, различающихся структурой катионного и анионного фрагментов молекулы, и экспериментально изучена их психотропная активность.
Цель настоящей работы – осуществить компьютерный прогноз психотропной активности производных АГКМФК и экспериментально изучить мнемотропные, антидепрессивные и анксиолитические свойства наиболее перспективных соединений.
Материалы и методы исследования
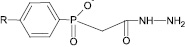
Объектами для компьютерного прогноза явились 47 производных АГКМФК с общей формулой 4-XPhP(O)(O▬)CH2NHNH2●[Z+].
Результаты прогноза вероятной биологической активности представлены в виде списка видов активностей с расчетными оценками вероятности наличия (Ра) или отсутствия (Pi) от 0 до 1.
Объектами фармакологических исследований явились 16 наиболее перспективных соединений с показателями Ра от 0,330 до 0,840, химические формулы соединений и ДЛ50 представлены в табл. 1.
Таблица 1
Химические формулы производных АГКМФК и их ДЛ50 при внутрибрюшинном введении мышам
|
Общая формула производных арил(гидразинокарбонилметил)фосфиновых кислот
|
||||
|
№ п/п |
Шифр соединения |
R |
Z + |
ДЛ50 |
|
1 |
A6 |
Cl |
H |
5000 ± 15 |
|
2 |
S7 |
Cl |
Na+ |
7430 ± 25,2 |
|
3 |
S8 |
Cl |
NH3+CH(Me)Ph (dl) |
980 ± 33,8 |
|
4 |
S9 |
Cl |
NH3+CH(Me)Ph (l) |
631,0 + 39,2 |
|
5 |
S10 |
Cl |
NH3+CH(Me)Ph (d) |
715 ± 28,2 |
|
6 |
S11 |
Cl |
NH4+ |
3480 ± 35,7 |
|
7 |
S12 |
Cl |
NH3+CH2CH2COOEt |
5045 ± 21,8 |
|
8 |
S16 |
H |
NH3+CH(Me)Ph (l) |
950 ± 34,2 |
|
9 |
S17 |
F |
NH3+CH(Me)Ph |
1010 ± 37,0 |
|
10 |
S18 |
Me |
NH3+CH(Me)PhMe |
990 ± 72,3 |
|
11 |
S19 |
Me2N |
NH3+CH(Me)PhNH2 |
975 ± 29,9 |
|
12 |
S21 |
Cl |
NH3+(CH2)3NC4H8O |
710 ± 45,2 |
|
13 |
S24 |
H |
NH3+CH(Me)Ph (dl) |
1015 ± 30,8 |
|
14 |
S28 |
Cl |
NH3+CH(CH3)CH(OH)Ph |
980 ± 35 |
|
15 |
S29 |
F |
NH3+CH(CH3)CH(OH)Ph |
2490 ± 45 |
|
16 |
S30 |
Cl |
NH3+(CH2)3C(O)Oet |
520 ± 38,8 |
Эксперименты проведены на 1152 белых беспородных мышах – самцах массой 18–22 г. До начала экспериментов все животные содержались в стандартных условиях вивария с естественным световым режимом на полнорационной сбалансированной диете (ГОСТ Р 50258-92) с соблюдением Международных рекомендаций Европейской конвенции по защите позвоночных животных, используемых при экспериментальных исследованиях (1997), а также правил лабораторной практики при проведении доклинических исследований в РФ (ГОСТ З 51000.3-96 и 51000.4-96). Все исследования были одобрены комитетом по этической экспертизе.
Экспериментальные работы по исследованию спектра психотропной активности соединений были проведены согласно «Руководству по экспериментальному (доклиническому) изучению новых фармакологических веществ» [4].
Для изучения двигательной и исследовательской реакции животных использовали метод «открытое поле» (Buccafusco J.J., 2009) на установке «Открытое поле» (НПК Открытая Наука, Москва, Россия). Мнемотропное действие исследовали на модели условной реакции пассивного избегания (УРПИ) (при силе тока 0,4 мА – 1 с). (Bures J., 1983), анксиолитическую активность – на модели «конфликтная ситуация с водной депривацией» (Vogel J.R., et al., 1971), антидепрессивное действие – на модели «поведенческое отчаяние» (Porsolt R.D. et. al., 1977).
Исследуемые соединения вводили в дозах, составляющих 1/100 и 1/1000 от ДЛ50, внутрибрюшинно за 40 мин до эксперимента. Контрольным группам животных вводили соответствующие объемы физиологического раствора. В качестве препаратов сравнения использовали пирацетам (200 мг/кг, «Марбиофарм», Россия), мелипрамин (7 мг/кг, «Эгис», Венгрия), диазепам (2 мг/кг, «Гедеон Рихтер», Венгрия), а также соединение 2-хлорэтокси-пара-N-диметиламинофенилфосфорилацетогидразид (КАПАХ) (1 и 10 мг/кг), проходящее заключительную стадию доклинических исследований [7, 8].
Результаты экспериментов обрабатывали статистически с вычислением t-критерия Стъюдента.
Результаты исследования и их обсуждение
Прогнозируемая мнемотропная, антидепрессивная и анксиолитическая активность производных АГКМФК по структуре анионного фрагмента представлена на табл. 2.
Значения прогноза мнемотропной активности по структуре анионного фрагмента были наибольшими для соединений S16, S24 (Ра = 0,840) и наименьшими для соединения S19 (Ра = 0,747). Антидепрессивная активность была прогнозирована для всех изучаемых соединений (Ра = 0,543–0,663). Значения вероятности наличия анксиолитической активности находятся в диапазоне 0,330–0,642, наибольшая вероятность была прогнозирована для соединения S19 (Ра = 0,642), а наименьшая – для соединений S17, S29 (Ра = 0,330).
Прогноз по структуре катионных фрагментов также выявил наличие мнемотропной, антидепрессивной и анксиолитической активностей, однако значения Pa были несколько ниже, чем для анионных фрагментов.
Мнемотропная активность была подтверждена экспериментально на модели УРПИ. Большинство соединений улучшали процессы обучения и памяти, удлиняя латентный период захода мышей в темный отсек экспериментальной камеры на 2-й день тестирования (рис. 1).
Таблица 2
Прогнозируемая в программе PASS мнемотропная, антидепрессивная и анксиолитическая активность производных АГКМФК по структуре анионного фрагмента
|
Шифр соединений |
R |
Мнемотропная активность (Pa) |
Антидепрессивная активность (Pa) |
Анксиолитическая активность (Pa) |
|
S16, S24 |
Н |
0,840 |
0,663 |
0,564 |
|
S17, S29 |
F |
0,805 |
0,659 |
0,330 |
|
A6, S7, S8, S9, S10, S11, S12, S21, S28, S30 |
Cl |
0,767 |
0,652 |
0,343 |
|
S19 |
N(CH3)2 |
0,742 |
0,543 |
0,642 |
|
S18 |
OCH3 |
0,755 |
0,577 |
0,542 |
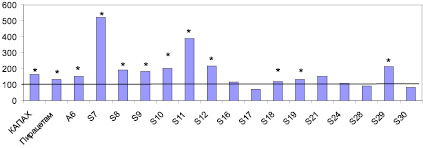
Рис. 1. Влияние производных арил(гидразинокарбонилметил)фосфиновых кислот на латентный период захода мышей в темный отсек камеры на модели УРПИ в дозах, составляющих 1/100 от ДЛ50. По оси ординат – латентный период захода мышей в %, по оси абсцисс – соединения. * – р < 0,05 по сравнению с показателями контрольной группы, принятыми за 100 %
В дозе, составляющей 1/100 от ДЛ50, наибольшую мнемотропную активность проявили соединения S7 и S11, содержащие атом хлора в пара-положении фенильного радикала в анионном фрагменте. Длительность латентного периода захода животного в темный отсек камеры была выше, чем у препаратов сравнения. Мнемотропная активность большинства соединений сохранялась и в дозах, составляющих 1/1000 от ДЛ50, исключением явились соединения S7 и S11.
В дозах, составляющих 1/100 от ДЛ50, большинство соединений проявляли антидепрессивную активность, наиболее выраженную у соединений S7 и S16. При их введении периоды неподвижности у мышей укорачивались в 1,3 и 1,4 раза соответственно (рис. 2).
Наибольшая антидепрессивная активность в дозах, составляющих 1/1000 от ДЛ50, отмечена у соединений S7 и S19.
Данные компьютерного прогноза подтвердились и в отношении анксиолитической активности соединений. В дозах, составляющих 1/100 от ДЛ50, на модели «конфликтная ситуация» наибольшую активность проявили соединение S19, содержащее диметиламиногруппу в пара-положении фенильного радикала в фосфорильном фрагменте, и соединения с незамещенным (S24) и хлорфенильным (S11, A6) радикалами, что выражалось в увеличении количества взятий воды из поилки (рис. 3).
В дозах, равных 1/1000 от ДЛ50, анксиолитические свойства проявили соединения S7, S11, S19 и S30, которые увеличивали количество взятий воды из поилки по сравнению с контрольной группой животных в 1,3–1,6 раза. КАПАХ в исследуемых дозах не проявил активности в данном тесте.
Соединения, эффективные на модели «конфликтной ситуации», как правило, угнетали ориентировочно-исследовательскую реакцию мышей в «открытом поле». Однако соединение S7, напротив, увеличивало количество заглядываний в отверстия в 1,4 раза по сравнению с контролем.
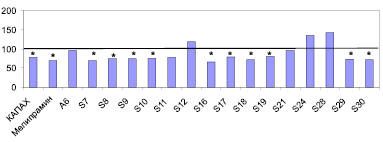
Рис. 2. Влияние производных арил(гидразинокарбонилметил)фосфиновых кислот на длительность периодов неподвижности у мышей на модели «поведенческое отчаяние» в дозах, составляющих 1/100 от ДЛ50. По оси ординат – длительность периодов неподвижности в %, по оси абсцисс – шифр соединения. * – р < 0,05 по сравнению с показателями контрольной группы, принятыми за 100 %
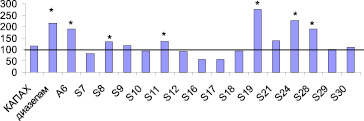
Рис. 3. Анксиолитическая активность производных арил(гидразинокарбонилметил)фосфиновых кислот на модели «конфликтная ситуация» у мышей в дозах, составляющих 1/100 от ДЛ50. По оси ординат – количество взятий воды из поилки в %, по оси абсцисс – шифр соединения. * – р < 0,05 по сравнению с показателями контрольной группы, принятыми за 100 %
Таким образом, результаты скрининга нового ряда соединений АГКМФК позволяют предположить наличие у них антидепрессивной, анксиолитической активности и способности улучшать память и обучение в дозах, составляющих 1/100 и 1/1000 от ДЛ50. Результаты экспериментальных исследований совпадают с данными компьютерного прогноза.
Выводы
1. Производные арил(гидразинокарбонилметил)фосфиновых кислот в дозах, составляющих 1/100 и 1/1000 ДЛ50, проявляют мнемотропные, антидепрессивные и анксиолитические свойства на лабораторных животных.
2. Результаты экспериментального изучения мнемотропной, антидепрессивной и анксиолитической активности в целом совпадают с данными компьютерного прогноза по программе PASS с вероятностью (Ра) в диапазонах 0,742-0,840, 0,543-0,663 и 0,330-0,642 соответственно.
Исследования поддержаны грантом РФФИ № 12-04-97095 (2012-2014).
Рецензенты:Залялютдинова Л.Н., д.м.н., профессор кафедры фармакологии, ГБОУ ВПО «Казанский ГМУ» Минздрава России, г. Казань;
Валеева И.Х., д.б.н., старший научный сотрудник, ГБОУ ВПО «Казанский ГМУ» Минздрава России, г. Казань.
Работа поступила в редакцию 06.03.2015.
Библиографическая ссылка
Макарова Е.А., Семина И.И., Байчурина А.З., Шиловская Е.В., Тарасова Р.И., Мустафин Р.И. ИЗУЧЕНИЕ ПСИХОТРОПНОЙ АКТИВНОСТИ ПРОИЗВОДНЫХ АРИЛ(ГИДРАЗИНОКАРБОНИЛМЕТИЛ)ФОСФИНОВЫХ КИСЛОТ // Фундаментальные исследования. 2015. № 2-7. С. 1407-1411;URL: https://fundamental-research.ru/en/article/view?id=37163 (дата обращения: 01.05.2026).




