Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
STUDY OF THE PROCESS OF STRIPPING NITROGEN COMPOUNDS FROM SPENT SULPHURIC ACID NONCONDENSABLE GAS PHASE
Концентрирование денитрированной серной кислоты является одной из стадий процесса регенерации отработанной серной кислоты (ОСК). Выпаривание воды из растворов серной кислоты сопровождается образованием сернокислотного тумана и частичного восстановления кислоты органическими соединениями с выделением диоксида серы. Поэтому отходящие газы подвергают очистке перед выбросом в атмосферу.
Для концентрирования разбавленных растворов серной кислоты наиболее эффективными являются аппараты с непосредственным соприкосновением газа и жидкости. По экономичности и простоте аппаратурного оформления другие способы не могут конкурировать с этим методом. Однако метод обладает существенным недостатком – высоким туманообразованием. Обезвреживание отходящих газов от тумана серной кислоты, несмотря на применение громоздких и дорогостоящих электрофильтров, представляет значительные трудности.
Исследование [4, 5] показало, что максимальные значения массовой доли тумана серной кислоты после электрофильтра относятся к частицам со среднегеометрическим диаметром 2,2 и менее 0,6 мкм при работе на природном газе и на мазуте. Соответственно концентрация тумана находится в пределах 0,4–0,6 и 0,8–1,5 г/м3.
Сложности улавливания мелких частиц тумана серной кислоты предопределяют пути не столько на совершенствование способов и аппаратов очистки отходящих газов, сколько на разработку конструкций концентраторов или условий и методов, предотвращающих образование тумана.
Для ликвидаций условий туманообразования необходимо исключить перенасыщение газовой фазы парами серной кислоты, превышающее критические значения при переходе газовой фазы с предыдущей ступени контакта на последующую. В действующих типах концентраторов при значительной разнице равновесного давления паров серной кислоты в первой и второй ступенях контакта фаз основным методом туманообразования является вторая ступень, где пресыщение паров серной кислоты достигает 40–120 при критическом значении 2,5–4,0. Поэтому во второй ступени контакта фаз происходит интенсивное туманообразование.
В диапазоне концентраций 63–80 % серной кислоты равновесное парциальное давление паров серной кислоты практически равно нулю. Поэтому процесс концентрирования надо разбить на две стадии – предварительное укрепление до 76–80 % и затем доукрепление до 91–93 % H2SO4 на второй стадии. Поскольку на вторую стадию поступает кислота с повышенной концентрацией, то существенно меняются условия – увеличивается температура и концентрация кислоты. С уменьшением перепада концентраций и увеличением температуры по камерам резко уменьшается пресыщение газов парами серной кислоты. Так, при вводе на вторую стадию 80 %-й кислоты пресыщение парами кислоты снижается во второй камере в среднем до 4,8 при критической величине 2,1; в третьей камере до 9,7 при критическом пресыщении 2,7. Это снижает количество тумана и увеличивает размеры его частиц.
Цель исследования – выполнить исследования по отдувке соединений азота из серной кислоты неконденсируемой фазой в зависимости от свободного сечения тарелки, температуры и продолжительности процесса. Определить константу и степень десорбции соединений азота из серной кислоты и концентрацию упаренной кислоты.
Материалы и методы исследования
Исследования проводили следующим образом. Термостатированный реактор с ситчатой тарелкой предварительно продували азотом, очищенным от кислорода пирогаллолом А. В реактор заливали 100 мл предварительно подогретой до требуемой температуры кислоты и продували горячим воздухом. После окончания опыта определяли константу и степень десорбции оксидов азота из серной кислоты и концентрацию кислоты.
Результаты исследования и их обсуждение
Практический интерес представляет отдувка соединений азота из ОСК неконденсируемой фазой [2].
Изучена десорбция оксидов азота и азотной кислоты из 70 % серной кислоты воздухом при 80–170 °С. Определение оптимального расхода воздуха при десорбции соединений азота на колонках с разным свободным сечением проводили с использованием серной кислоты, содержащей 0,03 % N2O3 и 0,05 % HNO3. Влияние расхода воздуха на степень отдувки соединений азота при 110°С представлено в табл. 1. Свободное сечение тарелки – 5 %.
Наличие в нитрозе азотной кислоты резко повышает равновесное парциальное давление оксида азота над раствором [1]. Следовательно, присутствие азотной кислоты должно интенсифицировать процесс отдувки оксида азота. Для выяснения влияния азотной кислоты на показатели десорбции была исследована десорбция оксида азота (III) из кислоты с 70 % H2SO4 и 0,05–0,5 % N2O3 при температуре 160 °С. Массовую долю азотной кислоты меняли от 0,05 до 1,5 %. Расход воздуха составлял 0,32 м3/ч. Результаты опытов подтвердили интенсификацию процесса при наличии в нитрозе даже небольших количеств свободной азотной кислоты.
Таблица 1
Влияние расхода воздуха на степень удаления оксида азота (III) и азотной кислоты
|
Расход воздуха, м3/ч |
Степень денитрации (a при продолжительности, мин |
|||||||||||
|
20 |
40 |
60 |
80 |
100 |
120 |
|||||||
|
α N2O3 |
α HNO3 |
α N2O3 |
α HNO3 |
α N2O3 |
α HNO3 |
α N2O3 |
α HNO3 |
α N2O3 |
α HNO3 |
α N2O3 |
α HNO3 |
|
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
0 |
1,9 |
0,9 |
4,5 |
2,7 |
8,1 |
4,6 |
13,5 |
7,0 |
18,7 |
9,2 |
21,4 |
11,4 |
|
0,20 |
27,5 |
6,5 |
31,3 |
11,0 |
35,1 |
15,1 |
40,0 |
18,6 |
41,2 |
21,9 |
43,9 |
24,5 |
|
0,32 |
34,5 |
12,5 |
41,5 |
16,2 |
45,2 |
22,9 |
47,4 |
25,4 |
50,0 |
29,6 |
54,8 |
35,8 |
|
0,40 |
38,8 |
18,7 |
44,0 |
21,4 |
48,9 |
26,7 |
51,1 |
30,0 |
54,9 |
33,3 |
57,3 |
38,7 |
|
0,58 |
40,8 |
21,1 |
45,9 |
24,6 |
50,5 |
28,9 |
52,3 |
31,5 |
56,2 |
35,5 |
59,0 |
39,8 |
|
0,76 |
41,5 |
22,6 |
46,2 |
26,1 |
50,8 |
31,0 |
52,8 |
33,0 |
56,9 |
36,7 |
60,5 |
41,0 |
|
0,98 |
42,0 |
23,5 |
46,8 |
26,5 |
51,2 |
32,2 |
53,0 |
34,4 |
57,3 |
38,1 |
62,0 |
41,4 |
Степень десорбции и константа скорости десорбции в начале опыта существенно возрастают с повышением доли азотной кислоты. По мере протекания процесса ее влияние снижается. Так, при повышении доли азотной кислоты с 0,05 до 1,5 % за 5 минут степень десорбции возрастает в 2,9 раза, а константа скорости десорбции – в 4,5 раза, а за 35 минут эти показатели возрастают соответственно в 1,1 и 2,1 раза.
Опыты показали, что продувка кислоты горячим воздухом в количестве 0,30–0,40 м3/ч приводит к удалению 38,8–57,3 % N2O3 и 18,7–38,7 % HNO3 за время 20–120 мин. При увеличении количества воздуха до 0,98 м3/ч степень отгонки соединений азота дополнительно возрастает лишь на 4–12 %. С целью предотвращения возврата оксидов азота с конденсатом в опытах конденсацию паров исключали путем обогрева верхней зоны колонки до 120–130 °С. Вследствие испарения воды серная кислота концентрировалась (рисунок). При 110 °С, продолжительности продувки 1 ч и свободном сечении тарелки 5 % происходит концентрирование кислоты с 72,3 до 78,3 % при увеличении расхода воздуха от 0 до 0,98 м3/ч, а при 130 °С – с 73,8 до 80,2 %. Увеличение концентрации серной кислоты приводит к снижению равновесного парциального давления оксида азота (III) над нитрозами. Так, при температуре 80°С равновесное парциальное давление оксидов азота над раствором, содержащим 0,03 % N2O3 и 71,6 % H2SO4, равно примерно 30 Па, тогда как при таком же содержании оксида азота (III) в 76,7 % серной кислоте оно равно примерно 12 Па, а для 82,0 % серной кислоты давление составляет лишь 3 Па. Особенно заметно влияние концентрирования серной кислоты при десорбции соединений азота из серной кислоты при совместном присутствии оксида азота и азотной кислоты. В последующих опытах были установлены следующие расходы воздуха: для колонки со свободным сечением тарелки 10 % – 0,70 м3/ч, для колонки со свободным сечением 5 % – 0,32 м3/ч. Для таких расходов воздуха рассчитаны коэффициенты десорбции соединений азота из серной кислоты (табл. 2). При определении коэффициента десорбции количество десорбированного оксида (III) или азотной кислоты отнесены к объему продуваемого воздуха. Данные справедливы для соотношения объема денитрируемой кислоты и продуваемого воздуха 0,156 л/м3 при свободном сечении тарелки 10 % и 0,107 л/м3 при сечении 5 %.
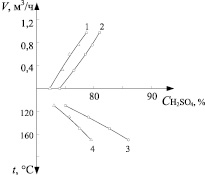
Влияние расхода воздуха (V) и температуры (t) на упаривание серной кислоты (CH2SO4)
С уменьшением свободного сечения тарелки интенсивность концентрирования серной кислоты возрастает. Это происходит вследствие того, что большая скорость воздуха в свободном сечении тарелки, равном 5 %, способствует интенсивному обновлению поверхности контакта фаз, снижая сопротивление десорбции паров воды в газовой пленке. Этот же эффект наблюдается при увеличении расхода воздуха при постоянной температуре и продолжительности опыта (рисунок).
Полученные коэффициенты десорбции могут быть объяснены следующим образом: при продувке кислоты, содержащей 0,029 % N2O3, более высокие коэффициенты десорбции получены на колонке со свободным сечением 10 %, т.к. здесь эффект концентрирования серной кислоты был ниже. Очевидно, меньшие значения коэффициентов десорбции оксидов азота (III) из нитрозной серной кислоты при свободном сечении тарелки в колонке 5 % объясняются меньшей степенью гидролиза НСК при более высокой концентрации серной кислоты [3].
В случае денитрации смеси серной и азотной кислот влияние концентрирования серной кислоты противоположно. При прочих равных условиях увеличение концентрации серной кислоты приводит к возрастанию парциального давления азотной кислоты.
При совместном присутствии оксида азота (III) и свободной азотной кислоты коэффициенты десорбции соединений азота несколько выше при температурах 80–130 °С для колонки со свободным сечением тарелки 5 % по сравнению с колонкой, свободное сечение которой равно 10 %. При высоких температурах (170 °С) десорбция азотной кислоты лучше происходит на колонке с большим свободным сечением тарелки.
Таблица 2
Коэффициенты десорбции соединений азота при продувке воздухом
|
Температура, °С |
Время, мин |
Состав исходной кислоты, % |
Коэффициент десорбции, 107 моль/с×м3 |
||||
|
N2O3 |
HNO3 |
||||||
|
N2O3 |
HNO3 |
Свободное сечение тарелки, % |
|||||
|
10 |
5 |
10 |
5 |
||||
|
80 |
20 |
0,029 |
– |
7,9 |
0,8 |
– |
– |
|
40 |
3,0 |
0,4 |
– |
– |
|||
|
60 |
1,6 |
0,4 |
– |
– |
|||
|
80 |
1,0 |
0,3 |
– |
– |
|||
|
100 |
0,6 |
0,3 |
– |
– |
|||
|
170 |
20 |
0,029 |
– |
13,0 |
11,6 |
– |
– |
|
40 |
4,6 |
3,3 |
– |
– |
|||
|
60 |
2,4 |
1,7 |
– |
– |
|||
|
80 |
1,5 |
1,1 |
– |
– |
|||
|
100 |
1,0 |
0,8 |
– |
– |
|||
|
80 |
20 |
– |
0,054 |
– |
– |
43,7 |
93,7 |
|
40 |
– |
– |
14,5 |
23,6 |
|||
|
60 |
– |
– |
7,5 |
12,0 |
|||
|
80 |
– |
– |
4,3 |
6,8 |
|||
|
100 |
– |
– |
2,9 |
4,3 |
|||
|
170 |
20 |
– |
0,054 |
– |
– |
58,2 |
103,2 |
|
40 |
– |
– |
17,5 |
26,5 |
|||
|
60 |
– |
– |
8,2 |
11,9 |
|||
|
80 |
– |
– |
4,4 |
6,6 |
|||
|
100 |
– |
– |
2,9 |
4,2 |
|||
|
80 |
20 |
0,032 |
0,051 |
1,0 |
15,1 |
4,4 |
9,0 |
|
40 |
1,0 |
4,8 |
1,5 |
3,5 |
|||
|
60 |
0,5 |
2,2 |
0,8 |
1,8 |
|||
|
80 |
0,5 |
1,4 |
0,7 |
1,4 |
|||
|
100 |
0,4 |
0,9 |
0,5 |
0,9 |
|||
|
170 |
20 |
0,032 |
0,051 |
6,6 |
16,4 |
45,0 |
33,0 |
|
40 |
2,2 |
4,2 |
24,0 |
9,3 |
|||
|
60 |
2,0 |
2,0 |
5,0 |
4,5 |
|||
|
80 |
1,3 |
1,2 |
2,9 |
2,9 |
|||
|
100 |
0,6 |
0,4 |
1,3 |
1,4 |
|||
Все последующие опыты с продувкой воздухом проводили на колонке со свободным сечением тарелки 5 % при расходе воздуха 0,32 м3/ч.
С ростом температуры в пределах 80–170 °С степень денитрации оксида азота (III) из нитрозной серной кислоты, содержащей 0,029 % N2O3, продувкой воздухом увеличивается примерно в 35 раз при продолжительности опыта 20 мин (с 0,6 до 20,8 %) и в 4 раза при продолжительности продувки 120 мин (с 14,9 до 56,4 %). При 170 °С и продолжительности отдувки 120 мин в газовую фазу переходит не более 56,4 % оксида азота (III), остаточное содержание N2O3 в кислоте при этом составляет 0,013 %. Таким образом, отгонка N2O3 из нитрозной серной кислоты горячим воздухом без введения восстановителей не обеспечивает снижение концентрации оксида азота (III) в серной кислоте менее 0,013 %. Исследованием отдувки азотной кислоты из совместного раствора серной и азотной кислот установлено, что продувка серной кислоты горячим воздухом позволяет удалить основное количество азотной кислоты (табл. 3) при начальном содержании ее 0,054 %.
Таблица 3
Кинетика десорбции азотной кислоты из 70 % серной кислоты
|
Время, мин |
Остаточное содержание HNO3 (×103, %) при температуре, °С |
||||
|
80 |
110 |
130 |
150 |
170 |
|
|
20 |
7,5 |
4,3 |
3,7 |
2,6 |
1,8 |
|
40 |
7,2 |
2,4 |
2,5 |
0,8 |
0,7 |
|
60 |
2,5 |
1,4 |
0,7 |
0,6 |
0,5 |
|
80 |
1,1 |
0,6 |
0,4 |
0,3 |
0,3 |
|
100 |
0,6 |
0,3 |
0,3 |
0,3 |
0,2 |
|
120 |
0,3 |
0,3 |
0,2 |
0,2 |
0,14 |
Как видно из табл. 3, при температуре опыта 110 °С и продолжительности продувки 20 мин остаточное содержание азотной кислоты составляет 0,0043 %, а степень денитрации серной кислоты 92,0 %. При 170 °С за 120 мин отдувается 99,7 % азотной кислоты, что соответствует остаточному содержанию азотной кислоты 0,00014 %.
Таким образом, отдувкой горячей неконденсируемой фазой следует довести концентрацию серной кислоты до 80 % и такую кислоту непосредственно направить во вторую ступень концентратора.
Выводы
1. Приведен краткий анализ работы аппаратов концентрирования серной кислоты, туманообразования и снижения пресыщения газовой фазы парами серной кислоты, превышающее критическое значение.
2. Выполнено исследование по отдувке соединений азота из серной кислоты неконденсируемой средой в зависимости от свободного сечения тарелки, температуры и продолжительности процесса.
3. Определены константа, степень десорбции соединений азота и упаривания серной кислоты.
Рецензенты:
Ксандров Н.В., д.т.н., профессор, зав. кафедрой ТНВ, Дзержинский политехнический институт, НГТУ им. Р.Е. Алексеева, г. Дзержинск;
Сидягин А.А., д.т.н., профессор кафедры МАХПП, Дзержинский политехнический институт, НГТУ им. Р.Е. Алексеева, г. Дзержинск.
Работа поступила в редакцию 04.02.2015.
Библиографическая ссылка
Ким П.П., Пастухова Г.В., Чубенко М.Н., Комаров В.А. ИССЛЕДОВАНИЕ ПРОЦЕССА ОТДУВКИ СОЕДИНЕНИЙ АЗОТА ИЗ ОТРАБОТАННОЙ СЕРНОЙ КИСЛОТЫ НЕКОНДЕНСИРУЕМОЙ ГАЗОВОЙ ФАЗОЙ // Фундаментальные исследования. 2015. № 3. С. 85-89;URL: https://fundamental-research.ru/en/article/view?id=37088 (дата обращения: 15.05.2026).



