В настоящее время в медицине, особенно хирургии, большое внимание уделяется синдрому эндогенной интоксикации (ЭИ). Причины его развития многообразны. Чаще всего эндогенная интоксикация возникает при патологиях, сопровождающихся воспалительно-деструктивными явлениями. В хирургии одними из основных причин развития эндогенной интоксикации являются перитонит и панкреатит [1, 3, 4].
Лечение больных с тяжелым перитонитом остается сложной проблемой в абдоминальной хирургии. В этой категории пациентов летальность остается на высоком уровне и достигает 50 %. Основной причиной смерти больных перитонитом является прогрессирующая ЭИ, приводящая к системным полиорганным нарушениям [6–10, 12].
Тяжелой патологией до настоящего времени остается панкреатит. Неуклонный рост заболеваемости острым панкреатитом, частое прогрессирование заболевания до деструктивных форм, высокая (до 80 % при панкреонекрозах) летальность определяют необходимость дальнейшей разработки теоретических и клинических вопросов этой тяжелой патологии. Тяжелое состояние больных и летальные исходы при остром панкреатите обусловлены панкреатогенным эндотоксикозом, приводящим к плюривисцеральным поражениям, которые оказываются причиной смерти [2, 5, 11, 13, 14].
Поэтому исследования последних лет сконцентрированы на проблеме выбора способа лечения не только основного заболевания, но и борьбы с прогрессированием ЭИ.
Важно отметить, что наиболее спорным и обсуждаемым является вопрос о том, какое значение имеют полиорганные поражения в прогрессировании эндотоксикоза.
Цель работы – установить значение органных (кишечник, печень, легкие, почки) липидных дестабилизаций в прогрессировании эндогенной интоксикации при острой хирургической патологии на примере острого перитонита и острого панкреатита.
Материалы и методы исследования
Поставлены следующие серии опытов:
1 серия – модель острого серозного перитонита (10 животных);
2 серия – модель острого гнойно-фибринозного перитонита (10 животных);
3 серия – модель острого отечного панкреатита (10 животных);
4 серия – модель острого деструктивного панкреатита (панкреонекроза) (10 животных). Для получения данных, принятых за норму, произведены исследования у 8 здоровых животных.
Перитонит моделировали путем введения в брюшную полость каловой взвеси: при серозном перитоните экспозиция 24 ч, при гнойно-фибринозном – экспозиция 48 ч.
Панкреатит моделировали путем введения в паренхиму поджелудочной железы желчи: при отечном панкреатите – 4 точки введения, при панкреонекрозе – 8 точек введения.
В контрольные сроки исследования (1-е, 3-и и 5-е сутки) животным производили релапаротомию, оценивали состояние поджелудочной железы, кишечника, определяли характер их повреждений, а также производили биопсию тканей, забор венозной крови.
Опыты проводились под внутривенным наркозом с использованием тиопентал-натрия из расчета 0,04 мг/кг массы тела животного. После проведения исследований животных выводили из эксперимента введением летальной дозы тиопентал-натрия.
Остановимся на особенностях забора крови. Как указано выше, нами впервые поставлена задача изучить детоксикационную роль основных органов детоксикационной системы. С этой целью оценен уровень токсических продуктов гидрофильной и гидрофобной природы в притекающей и оттекающей от органа крови. Для кишечника, почек, и легких исполнить это не так уж и сложно. Большие затруднения возникли по отношению к печени. Нами разработана оригинальная методика, позволяющая производить забор крови, оттекающей от печени.
Нами выполнялась биопсия исследованных органов, в тканях которых оценен липидный состав, а также интенсивность перекисного окисления липидов (ПОЛ) и фосфолипазная активность.
Отметим, что по этому фрагменту работы нам представилось возможным не только оценить активность основных мембранодеструктивных факторов, но и непосредственный результат их действия по изменениям состава фосфолипидного бислоя мембран.
Липиды из тканей экстрагировали хлороформметаноловой смесью (Хиггинс Дж.А., 1990). Липиды фракционировали методом тонкослойной хроматографии (Хиггинс Дж.А., 1990; Vaskovsky V.E. et al., 1975). Молекулярный анализ проводили на денситометре Model GS-670 (BIO-RAD, США) с соответствующим программным обеспечением (Phosphor Analyst/PS Sowtware).
Показатели интенсивности ПОЛ: диеновые конъюгаты (ДК) определяли спектрофотометрическим методом при длине волны 232–233 нм (Ганстон Ф.Д., 1986); уровень малонового диальдегида (МДА) – спектрофотометрическим методом в реакции с тиобарбитуровой кислотой (Sigma), активность супероксиддисмутазы (СОД) – в реакции с нитросиним тетразолием (Гуревич В.С. и др., 1990). Активность фосфолипазы А2 (ФЛА2) исследовали в среде, содержащей 10 ммоль трис-HCL-буфер (рH 8,0), 150 ммоль тритон Х-100, 10 ммоль CaCl2 и 1,2 ммоль субстрата, в качестве которого использовали фосфатидилхолины яичного желтка (Трофимов В.А., 1999).
Определение молекул средней массы (МСМ). Сыворотку крови смешивают с 10 % раствором трихлоруксусной кислоты в соотношении 1:2, центрифугируют 30 мин при скорости 3000 g. Затем 0,5 мл супернатанта смешивают с 4,5 мл дистиллированной воды и измеряют оптическую плотность на спектрофотометре СФ-46 при длине волны 254 и 280 нм. Результат выражают в условных единицах (Пикуза О.И., Шакирова Л.З., 1994).
Определение общей (ОКА) и эффективной концентрации альбумина (ЭКА) проводили по методике Грызунова Ю.А. и Добрецова Г.Е. (1994) на специализированном анализаторе АКЛ-01 «Зонд». Использовали набор реактивов «Зонд-Альбумин» (г. Москва) в соответствии с прилагаемыми инструкциями. Рассчитывали: резерв связывания альбумина РСА по формуле РСА = ЭКА/ОКА; индекс токсичности плазмы (ИТ), отражающий степень заполнения тканевых центров различными токсическими веществами, по формуле: ИТ = ОКА/ЭКА – 1.
Исследования проведены в соответствии с этическими требованиями к работе с экспериментальными животными («Правила проведения работ с использованием экспериментальных животных» (приказ МЗ СССР № 755 от 12.08.1987 г.) Федеральный закон «О защите животных от жестокого обращения» от 01.01.1997 г., «Об утверждении правил лабораторной практики» (приказ МЗ РФ от 19.06.2003 г. № 267) и одобрены локальным этическим комитетом.
Полученные цифровые экспериментальные данные обработаны методом вариационной статистики с использованием t-критерия Стьюдента. Оценена корреляционная зависимость показателей по r-критерию. Вычисления и построение диаграмм, отражающих динамику изученных показателей, совершали с поддержкой программы Microsoft Excel XP. Применен текстовый процессор Microsoft Word XP.
Результаты исследования и их обсуждение
Результаты опытов показали, что при нетяжелых формах как перитонита, так и панкреатита барьерная функция органов детоксикационной системы существенно не страдает. Несмотря на повышение содержания продуктов эндотоксикоза в плазме крови, а также печени, легких, почках и кишечнике, проявляющееся ростом показателей среднемолекулярных пептидов и индекса токсичности в 2–6 раз (p < 0,05) по сравнению с нормой, уровень токсических продуктов в притекающей крови к печени, легким и почкам был ниже, чем в оттекающей (рис. 1).
Исключением был кишечник. В оттекающей от него крови уровень токсических продуктов был выше, особенно при остром перитоните.
Отметим, что при указанных формах заболеваний в тканевых структурах исследованных органов отмечены небольшие приросты интенсивности ПОЛ, оцененные показателями ДК и МДА и фосфолипазной активности в 1,5–2 раза в сравнении с нормой (p < 0,05), что не приводило к заметным изменениям состава фосфолипидного бислоя мембран клеток (рис. 2). Как видно из рисунка, уровень суммарных фосфолипидов (СФЛ), холестерола (ХЛ) и эфиров холестерола (ЭХЛ) существенно от нормы не отличался.
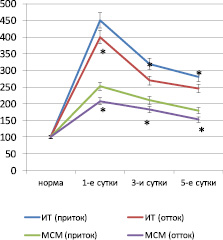
Рис. 1. Показатели детоксикационной активности печени при остром серозном перитоните (* – достоверность отличия показателей при р < 0,05)
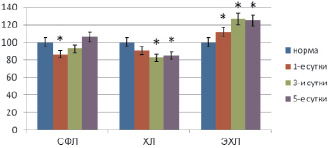
Рис. 2. Содержание некоторых липидов в ткани легких при остром отечном панкреатите (* – достоверность отличия показателей при р < 0,05)
При тяжелых формах патологий функциональное состояние органов детоксикационной системы угнеталось, и на определенных этапах патологического процесса в оттекающей крови от печени, легких и почек уровень токсических продуктов или соответствовал таковому в притекающей крови или даже был выше его (рис. 3). При этом уровень токсических продуктов (ИТ и МСМ) в исследуемых органах возрастал в сравнении с нормой в 3,5–7,5 раз (p < 0,05).
Подчеркнем, что при указанной тяжести заболеваний в тканевых структурах исследованных органов отмечены резкий прирост интенсивности ПОЛ (ДК, МДА), фосфолипазной активности и снижение активности СОД, что, безусловно, явилось триггером для существенной модификации состава фосфолипидного бислоя мембран клеток. При этом наиболее значимо возрастал уровень лизофосфолипидов – в 15–20 раз в сравнении с нормой (рис. 4–5).
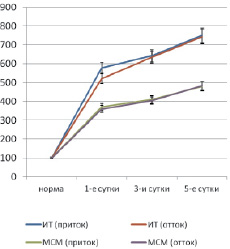
Рис. 3. Показатели детоксикационной активности печени при остром гнойно-фибринозном перитоните (* – достоверность отличия показателей при р < 0,05)
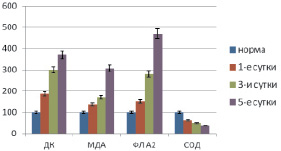
Рис. 4. Показатели ПОЛ и активности фосфолипазы А2 в тканях легких при остром деструктивном панкреатите
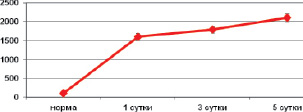
Рис. 5. Содержание лизофосфолипидов в ткани печени при остром гнойно-фибринозном перитоните
Корреляционный анализ показал, что между показателями детоксикационной способности органов и нарушениями липидного состава имеется корреляционная связь (r = 0,678 – 0,972). Таким образом, впервые доказана сопряженность состояния органных барьеров противотоксиновой защиты с мембранодестабилизирующими явлениями.
Как отмечено выше, при определенных условиях, которые в наших модельных экспериментах выражались в чрезмерной интенсивности ПОЛ и фосфолипазной активности, в клетках исследованных органов детоксикационной системы возникали такой выраженности мембранодеструктивные процессы, при которых органы не только не обеспечивали нейтрализацию токсических продуктов, а сами становились дополнительным источником ЭИ.
Заключение
В рамках молекулярной динамики мембранных клеточных фосфолипидных перестроек и модуляции дисфункционального состояния исследованных органов сформулирована концепция значимости мембранодестабилизирующего процесса в прогрессировании эндотоксикоза.
Концепция не только определяет сам факт возможности прогрессирования ЭИ вследствие утраты детоксикационной способности органов, на которые возложена эта функция, но и «активное» их участие в прогрессировании эндотоксикоза. Фактически на определенных этапах патологического процесса органы детоксикационной системы могут становиться дополнительным источником эндотоксикоза.
Полученные данные, на наш взгляд, имеют не только академическое, но и прикладное значение, определяя наиболее важный спектр направлений по решению проблемы эндотоксикоза, в частности по сохранению структурно-функциональной организации биомембран клеток органов естественной системы детоксикации.
Рецензенты:
Смолькина А.В., д.м.н., профессор кафедры госпитальной хирургии медицинского факультета им. Т.З. Биктимирова, ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск;
Саушев И.В., д.м.н., профессор кафедры анестезиологии и реаниматологии, ФГБОУ ВПО «Мордовский государственный университет им. Н.П. Огарёва», г. Саранск.
Работа поступила в редакцию 29.12.2014.



