Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
WATER SECRETORY FUNCTION OF KIDNEYS AND SENSITIVITY OF KIDNEYS TO THE ANTIDIURETIC HORMONE AT RATS WITH AUTOIMMUNE NEPHRITE
Актуальность настоящей работы обусловлена высокой частотой нефрологических заболеваний, которые в большинстве случаях протекают латентно и клинические проявления часто наблюдаются при уже запущенных случаях, что не позволяет практическому здравоохранению оказывать эффективную помощь. Заболевания почек, как правило, характеризуются тяжелым течением, развитием рецидивов и в 1,5 % случаев, переходят в почечную недостаточность, при которой летальность достигает 50 % [3, 5]. К тому же нефропатии вызывают дисбаланс в других системах, в частности сердечно-сосудистой и эндокринной, а поражения почек возникают при других заболеваниях (печени, сахарном диабете, тяжелых гестозах, коллагенозах и др.) и патологических состояниях (интоксикация, шок, синдром длительного сдавления) [2, 4]. По европейским эпидемиологическим данным, заболеваниями почек страдают около 10 % населения, а в России до 16,5 % [7], и в последние десятилетия отмечается значительное омоложение нефрологической патологии, что уже, помимо широкой распространенности, приобретает и социальную значимость. Поэтому научно-исследовательские работы, способные вскрыть механизмы изменений работы почек и оказать помощь практическому здравоохранению при лечении почечных больных, остаются актуальными.
Целью настоящей работы являлось изучение водовыделительной функции почек и выяснение чувствительности канальцевого аппарата почек к антидиуретическому гормону у крыс с экспериментальным аутоиммунным нефритом.
Материалы и методы исследований
Для решения поставленной цели на 24 половозрелых крысах линии Wistar возрастом 8-10 месяцев и весом в 180–220 г создавалась экспериментальная модель аутоиммунного нефрита [9], которую вызывали путём однократного введения крысам в пяти местах (п/к в подмышечные и паховые области, внутрибрюшинно) по 0,2 мл равнодолевой смеси гомогената коркового вещества почки (на 100,0 мг ткани 1,0 мл физраствора) с полным адъювантом Фрейнда (водно-жировая эмульсия, содержащая вазелиновое масло, ланолин, БЦЖ или мурамилдипептид и эмульгатор, способный к депонированию антигена, усиливая его захват фагоцитами и оказывая активирующее влияние на макрофаги и Т-клетки).
Для выяснения чувствительности канальцевого аппарата почек к антидиуретическому гормону в условиях водного диуреза крысам в/м вводился десмопрессин – синтетический аналог вазопрессина (получен в результате дезаминирования цистеина и замещения L-аргинина на D-аргинин), обладающий выраженным и длительным антидиуретическим эффектом на дистальные извитые канальцы и собирательные трубочки. Доза десмопрессина для крыс (0,15 мкг/100 г) рассчитывалась в нашей лаборатории эмпирически с условием того, чтоб его антидиуретический эффект длился около одного часа [1].
На 12 интактных крысах изучали водовыделительную функцию почек, влияние десмопрессина и объемную скорость кровотока, для чего животным внутрибрюшинно вводили анестетик общего действия «Золетил» в дозе 0,1 мл/100 г, а затем из сердца отбирали кровь для исследований и почки для морфологии.
Опыты на крысах с аутоиммунным нефритом ставили через две недели после иммунизации, через месяц и в конце второго месяца и каждый раз после их завершения у шести крыс определяли скорость объемного кровотока, а затем брали кровь и почки. Поэтому через один месяц после иммунизации количество опытных крыс было 18, а в конце второго месяца – 12.
Водный диурез у крыс создавали внутрижелудочным введением водопроводной воды в объеме 5 % веса. Мочу собирали в специальных клетках-воронках в течение трех часов отдельно за каждый. В собранной моче и плазме крови спектрофотометрически определяли содержание эндогенного креатинина (метод Поппера), общего белка (метод Лоури в моче и биуретовый в плазме крови) [6]. Расчетные показатели, по которым можно судить о функции почек, – диурез, скорость клубочковой фильтрации, объем канальцевой реабсорбции воды и степень протеинурии. Объемную скорость почечного кровотока определяли инвазивным способом с помощью ультразвукового флуометра Transonic НТ 313 (США). О морфологической картине почек судили по результатам световой микроскопии (толщина срезов 7-8 мкм, окраска гематоксилин-эозином, увеличение в 600 раз). Полученные результаты статистически обрабатывались с применением параметрического метода сравнения средних величин, а степень достоверности оценивалась по t-критерию Стьюдента.
Все исследования проводили в соответствии с приказом Минздравсоцразвития России № 708н от 23 августа 2010 г. «Об утверждении Правил лабораторной практики».
Результаты исследования и их обсуждение
Начнем описательную часть исследований с морфологической характеристики почек. Через две недели после введения гомогената с адъювантом Фрейнда отмечались расширение полости капсул и капиллярной сети, появление лимфо-и лейкоцитарных инфильтратов вокруг клубочков, частичный отёк стромы, дистрофические изменения и белковые отложения в отдельных канальцах. Мозговое вещество почек особо не менялось.
Через месяц после иммунизации можно было уже констатировать разнокалиберность клубочков – от резко увеличенных и полнокровных до мелких и сморщенных, а лимфо- и лейкоцитарные инфильтраты вокруг них уже были с явлениями облитерации капсул и редукции части капилляров, участки полнокровия и кровоизлияний. Канальцы дистрофически изменены с разрушением щёточной каёмки и десквамацией эпителия. В полости трубочек скопления рыхлых и уплотнённых белковых масс. В канальцах мозгового вещества имелась мелкая вакуольная дистрофия. Сосудистая сеть неравномерна – от сужения, до полнокровия (рисунок). В конце второго месяца отмеченные изменения у семи крыс приобрели более выраженное ухудшенное состояние с явлениями дистрофических изменений.
До выяснения чувствительности канальцевого аппарата почек к антидиуретическому гормону при аутоиммунном нефрите, предварительно исследовали влияние десмопрессина у интактных крыс, введение которого после водной нагрузки вызвало за первый час полное отсутствие диуреза у восьми крыс из двенадцати, а у оставшихся четырех он был равен 0,49 ± 0,06 мл/час/100 г, то есть десмопрессин вызвал у 2/3 крыс полный антидиурез, а у других снизил его по сравнению с контролем в 3,28 раз. Это было обусловлено усилением обратного всасывания воды в дистальных канальцах и собирательных трубочках нефронов. Скорость клубочковой фильтрации не менялась (табл. 1). Диурез оказался сниженным и на втором часе, а за третий час, наоборот, повысился, но суммарный трехчасовой диурез оставался на 23,4 % меньше (р < 0,02). То есть у интактных крыс чувствительность части канальцевого аппарата почек, регулируемая вазопрессином, сохранена.
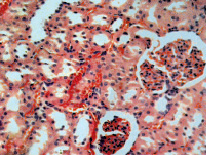
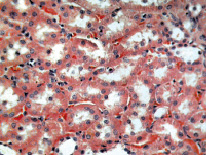
Морфология коркового и мозгового вещества почек крыс с аутоиммунным нефритом. Окраска азур-эозином. Увеличение в 600 раз
Таблица 1
Водный диурез, скорость клубочковой фильтрации и объем канальцевой реабсорбции у интактных крыс и после введения десмопрессина
|
Время |
Стат. показатель |
Диурез (мл/ч/100 г) |
Клубочковая фильтрация (мл/ч/100 г) |
Канальцевая реабсорбция (%) |
|
Интактные крысы |
||||
|
1 час |
М ± m |
1,49 ± 0,12 |
16,35 ± 1,25 |
90,88 ± 0,46 |
|
2 час |
М ± m |
1,59 ± 0,11 |
18,06 ± 1,36 |
91,19 ± 0,53 |
|
3 час |
М ± m |
0,78 ± 0,06 |
12,75 ± 1,03 |
93,87 ± 0,39 |
|
За 3 часа |
М ± m |
3,86 ± 0,29 |
47,16 ± 3,64 |
91,98 ± 0,46 |
|
Интактные крысы + Десмопрессин |
||||
|
1 час |
М ± m // р |
0,49 ± 0,06 // < 0,001 |
15,82 ± 1,21 // * |
96,90 ± 0,57 // < 0,001 |
|
2 час |
М ± m // р |
1,08 ± 0,07 // < 0,001 |
17,64 ± 1,94 // * |
93,87 ± 0,49 // < 0,001 |
|
3 час |
М ± m // р |
1,39 ± 0,1 // < 0,001 |
14,52 ± 1,13 // * |
90,43 ± 0,57 // < 0,001 |
|
За 3 часа |
М ± m // р |
2,96 ± 0,23 // < 0,02 |
47,98 ± 4,28 // * |
93,77 ± 0,54 // < 0,02 |
Определение влияния десмопрессина на объемную скорость почечного кровотока выявило незначительное ее снижение (11,86 ± 0,65 мл/мин – интактные крысы, 10,16 ± 0,82 мл/мин – десмопрессин), что, скорее всего, было связано со способностью десмопрессина незначительно суживать сосуды и слабо увеличивать артериальное давление [8]. Не менялись в плазме крови содержания общего белка и креатинина (61,27 ± 2,46 г/л и 73,25 ± 2,63 мкмоль/л – интактные крысы, 60,05 ± 3,12 г/л и 71,87 ± 3,46 мкмоль/л – десмопрессин).
У крыс с аутоиммунным нефритом через две недели после иммунизации водный диурез статистически значимо повысился за каждый час (на 38,6 % за три часа), что было обусловлено снижением канальцевой реабсорбции воды (р < 0,001), несмотря на то, что одновременно уменьшалась и скорость клубочковой фильтрации (табл. 2). Угнетение первоначального этапа процесса мочеобразования, очевидно, связано с характерным для нефритов поражением клубочков [5], на что указывают и наши морфологические изменения (от полнокровных до мелких и сморщенных), а не выявленное незначительное (на 7,7 %) снижение объемной скорости кровотока. Одновременно усилилась протеинурия (на 61,1 %), а в плазме крови повысилось содержание креатинина (82,46 ± 3,21 мкмоль/л, р < 0,05) и незначительно снизился уровень общего белка (57,28 ± 2,68 г/л). Все отмеченные изменения у крыс через месяц после иммунизации усилились. Это и повышение содержания креатинина в плазме крови (87,55 ± 4,34 мкмоль/л, р < 0,01), и протеинемия (52,74 ± 2,26 г/л, р < 0,05), и степень протеинурии, и полиурия, вызванная снижением обратного всасывания воды в канальцах почек, и продолжающее снижение скорости клубочковой фильтрации (табл. 2). Начала уменьшаться и объемная скорость почечного кровотока (9,52 ± 0,84 мл/мин).
Таблица 2
Водный диурез (мл/ч/100 г), скорость клубочковой фильтрации (мл/ч/100 г), объем канальцевой реабсорбции воды (%) и степень протеинурии (мкг/мл) у крыс с аутоиммунным нефритом
|
Условия опыта |
Исследуемый показатель |
Стат. показатель |
1 час |
2 час |
3 час |
За 3 часа |
|
|
Интактные крысы |
Диурез |
М ± m |
1,49 ± 0,12 |
1,59 ± 0,11 |
0,78 ± 0,06 |
3,86 ± 0,29 |
|
|
Фильтрация |
М ± m |
16,35 ± 1,25 |
18,06 ± 1,36 |
12,75 ± 1,03 |
47,16 ± 3,64 |
||
|
Реабсорбция |
М ± m |
90,88 ± 0,46 |
91,19 ± 0,53 |
93,87 ± 0,39 |
91,98 ± 0,46 |
||
|
Протеинурия |
М ± m |
4,87 ± 0,39 |
4,31 ± 0,57 |
6,25 ± 0,56 |
5,14 ± 0,51 |
||
|
Аутоиммунный нефрит |
Через 2 недели |
Диурез |
М ± m р |
1,92 ± 0,16 < 0,02 |
2,35 ± 0,19 < 0,02 |
1,08 ± 0,07 < 0,05 |
5,35 ± 0,42 < 0,02 |
|
Фильтрация |
М ± m р |
12,39 ± 1,17 < 0,05 |
13,86 ± 1,38 < 0,05 |
9,37 ± 0,92 < 0,02 |
35,62 ± 3,39 < 0,05 |
||
|
Реабсорбция |
М ± m р |
84,52 ± 0,76 < 0,001 |
83,06 ± 0,84 < 0,001 |
91,37 ± 0,60 < 0,001 |
86,32 ± 0,73 < 0,001 |
||
|
Протеинурия |
М ± m р |
7,64 ± 0,52 < 0,001 |
8,15 ± 0,62 < 0,001 |
9,05 ± 0,70 < 0,002 |
8,28 ± 0,61 < 0,001 |
||
|
Через 1 месяц |
Диурез |
М ± m р |
2,05 ± 0,15 < 0,01 |
2,13 ± 0,18 < 0,01 |
0,89 ± 0,06* |
5,07 ± 0,39 < 0,02 |
|
|
Фильтрация |
М ± m р |
11,43 ± 0,86 < 0,005 |
12,92 ± 1,02 < 0,01 |
10,21 ± 0,82* |
34,56 ± 2,70 < 0,02 |
||
|
Реабсорбция |
М ± m р |
82,06 ± 1,12 < 0,001 |
83,51 ± 1,34 < 0,001 |
91,28 ± 0,77 < 0,001 |
85,62 ± 1,07 < 0,001 |
||
|
Протеинурия |
М ± m р |
16,41 ± 1,27 < 0,001 |
15,64 ± 1,09 < 0,001 |
18,15 ± 1,31 < 0,001 |
16,73 ± 1,22 < 0,001 |
||
|
Через 2 месяца |
Диурез |
М ± m р |
0,73 ± 0,12 < 0,001 |
0,95 ± 0,10 < 0,001 |
0,46 ± 0,04 < 0,001 |
2,14 ± 0,27 < 0,001 |
|
|
Фильтрация |
М ± m р |
10,09 ± 0,95 < 0,001 |
10,57 ± 1,31 < 0,001 |
8,73 ± 0,92 < 0,05 |
29,39 ± 3,18 < 0,02 |
||
|
Реабсорбция |
М ± m |
92,76 ± 0,96* |
91,01 ± 0,76* |
94,73 ± 0,88* |
92,83 ± 0,86* |
||
|
Протеинурия |
М ± m р |
20,25 ± 1,76 < 0,001 |
18,64 ± 1,23 < 0,001 |
18,02 ± 1,46 < 0,001 |
18,97 ± 1,48 < 0,001 |
||
Примечание. * – отсутствие достоверных отличий.
К завершению экспериментов в конце второго месяца (табл. 2) уменьшились количество мочи, особенно за первый час (в 2 раза), скорость клубочковой фильтрации, объемная скорость кровотока (8,96 ± 0,72 мл/мин, р < 0,02), содержание общего белка в плазме крови (50,62 ± 1,88 г/л, р < 0,02) и одновременно повысились канальцевая реабсорбция воды, содержание креатинина в плазме крови (92,36 ± 5,12 мкмоль/л, р < 0,02) и протеинурия (в 3,7 раз).
Таким образом, введение крысам 1,0 мл смеси гомогената коркового вещества почек и полного адъюванта Фрейнда первоначально вызывает повышение водного диуреза за счет торможения канальцевой реабсорбции воды, а через два месяца – угнетение диуреза и объемной скорости почечного кровотока, протеинурию, снижение в плазме крови содержания общего белка и увеличение креатинина.
Выяснение чувствительности канальцевого аппарата почек к антидиуретическому гормону при аутоиммунном нефрите у крыс показало, что введение десмопрессина не оказало влияния на содержание в плазме крови креатинина и общего белка, а также на степень протеинурии. Что касается диуреза и основных процессов мочеобразования, то в первый месяц, когда отмечалось повышение диуреза, введение десмопрессина хоть и заблокировало выделение мочи, однако не столь выраженно, как у интактных крыс. И диурез в двухнедельных опытах отсутствовал у 10 крыс из 21, в конце первого месяца – у 10 из 18. При этом у крыс, у которых за первый час выделялась моча, ее количество по сравнению с интактными было статистически значимо (р < 0,001) больше и в двухнедельных (0,83 ± 0,05 мл/ч/100 г), и в месячных (1,06 ± 0,08 мл/ч/100 г) опытах. Расчет основных процессов мочеобразования показал, что скорость клубочковой фильтрации особо не менялась, а изменения диуреза были обусловлены канальцевой реабсорбцией воды (93,08 ± 0,87 % через две недели и 90,24 ± 1,23 % через месяц), которая была большей, чем у крыс с аутоиммунным нефритом (84,52 ± 0,76 % через две недели и 82,06 ± 1,12 % через месяц).
Спустя два месяца после иммунизации крыс эффект десмопрессина стал значительно слабее и если у 2/3 интактных крыс он вызвал полное отсутствие водного диуреза за первый час, а через один месяц – примерно у половины, то сейчас только у 1/4 крыс (у 9 крыс из 12). То есть к концу второго месяца после введения крысам смеси гомогената коркового вещества почек и полного адъюванта Фрейнда происходит ослабление чувствительности канальцевого аппарата к антидиуретическому гормону, что говорит о поражении не только клубочков, но и канальцев.
Рецензенты:
Брин В.Б., д.м.н., профессор, заведующий кафедрой нормальной физиологии, Северо-Осетинская государственная медицинская академия, г. Владикавказ;
Болиева Л.З., д.м.н., профессор, заведующая кафедрой фармакологии с клинической фармакологией, Северо-Осетинская государственная медицинская академия, г. Владикавказ.
Работа поступила в редакцию 02.12.2014.
Библиографическая ссылка
Джиоев И.Г., Клочков Д.А., Кабоева Б.Н., Батагова Ф.Э., Батагова Ф.Э. ВОДОВЫДЕЛИТЕЛЬНАЯ ФУНКЦИЯ И ЧУВСТВИТЕЛЬНОСТЬ ПОЧЕК К АНТИДИУРЕТИЧЕСКОМУ ГОРМОНУ У КРЫС С АУТОИММУННЫМ НЕФРИТОМ // Фундаментальные исследования. 2014. № 10-6. С. 1098-1102;URL: https://fundamental-research.ru/en/article/view?id=35995 (дата обращения: 16.05.2026).



