Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
COMPARISON OF DISSOLUTION KINETIC PARAMETERS IN DIFFERENT HYDROCARBONS OF PETROLEUM WAXES AND PARAFFIN TYPE ASPHALTENE- RESIN-PARAFFIN DEPOSITS
В настоящее время использование растворителей для удаления уже сформировавшихся АСПО является одним из самых распространенных способов борьбы с этим явлением. Считается [8], что процесс растворения АСПО заключается в физико-химическом взаимодействии ингредиентов растворителя с отдельными компонентами, составляющими отложения. Растворитель действует следующим образом: он растворяет связующий агент (смолу), в результате происходит оголение агломератов асфальтенов и парафинов, дальнейшее растворение которых зависит от состава растворителя. В зависимости от того, какие компоненты содержатся в АСПО в высоких концентрациях, АСПО могут быть парафинового, асфальтенового и смешанного типов. Так, эффективными растворителями парафинового АСПО являются низкокипящие алифатические углеводороды (УВ): пентан, гексан и гептан [11], а для удаления АСПО асфальтенового типа используют растворители на основе ароматических УВ [13]. Однако выбор растворителя до сих осуществляется полуэмпирически из-за:
1) недостатка информации о структуре и свойствах компонентов отложений;
2) трудностей изучения механизма взаимодействия нефтяных дисперсных систем с растворителями [2].
Таким образом, целью работы является попытка определения кинетических параметров растворения нефтяных парафинов в различных УВ для установления возможного механизма их взаимодействия с растворителями.
Материал и методы исследования
Добыча нефти на Иреляхском газонефтяном месторождении осложнена образованием АСПО. Для очистки нефтепромыслового оборудования от отложений используется газовый конденсат, добываемый на этом же месторождении, но, несмотря на то, что его годовой расход составляет свыше 300 м3, полностью очистить оборудование не удается. Нами установлено [5], что АСПО, образующиеся на поверхностях насосно-компрессорных труб (НКТ), относятся к парафинистому типу, а в составе газового конденсата преобладает н-гексан. Поэтому в качестве объекта исследования был выбран нефтяной парафин (ГОСТ 23683-89 марки В2), а в качестве его растворителей были исследованы н-гексан и бинарная смесь, состоящая из н-гексана и бензола (ГБС) в соотношении 1:1. Выбор нефтяного парафина основан на том, что он является высокоочищенным, не содержит воды и механических примесей, которые могут исказить экспериментальные результаты. Эксперименты были проведены при 10 и 25 °С, что соответствует сезонным условиям эксплуатации этого месторождения, а также при более высоких температурах (40 и 60 °С) для определения общей зависимости скорости растворения парафина от температуры.
Исследование кинетики растворения парафинов в вышеназванных УВ проводилось гравиметрически в статических условиях на торсионных весах по методике, описанной в [7]. Статистический расчет параметров кинетических моделей, выраженных в линейном виде, осуществлялся методом наименьших квадратов [10].
Результаты исследования и их обсуждение
С использованием методики [7] определены лимитирующие стадии процессов растворения (n), константы скоростей растворения (К), время, за которое половина количества парафинов перейдет в раствор (τ1/2), и рассчитаны эффективные энергии активации (Еа) разрушения нефтяных парафинов в исследуемых УВ системах (рис. 1; табл. 1).
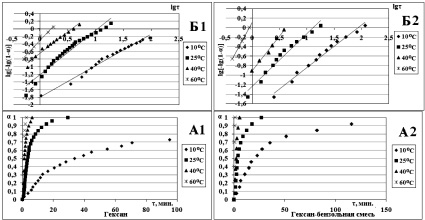
Рис. 1. Кинетические кривые растворения парафинов в гексане и ГБС (А1, А2) и их логарифмические анаморфозы (Б1, Б2) при 10, 25, 40 и 60 °С
Таблица 1
Кинетические параметры растворения нефтяных парафинов в различных УВ
|
Образец |
t, °С |
n |
r2 |
К, мин–1 |
τ1/2, мин |
Еа, кДж/моль |
|
Парафины + Гексан |
10 |
0,83 ± 0,04 |
0,984 |
1,53∙10–2 |
– |
125,2 |
|
25 |
1,17 ± 0,07 |
0,958 |
2,23∙10–1 |
3,11 |
||
|
40 |
1,12 ± 0,09 |
0,975 |
6,27∙10–1 |
1,11 |
||
|
60 |
1,58 ± 0,06 |
0,972 |
1,72 |
0,40 |
||
|
Парафины + Гексан + Бензол (1:1) |
10 |
0,90 ± 0,12 |
0,984 |
2,62∙10–2 |
26,46 |
90,3 |
|
25 |
1,11 ± 0,09 |
0,966 |
1,81∙10–1 |
3,83 |
||
|
40 |
1,45 ± 0,07 |
0,991 |
6,32∙10–1 |
1,10 |
||
|
60 |
2,11 ± 0,03 |
1,000 |
3,52 |
– |
Видно (табл. 1), что процесс разрушения нефтяных парафинов в алифатическом растворителе при 10 °С является диффузионно контролируемым (n < 1), но при его нагреве до 25 °С и выше процесс переходит из диффузионного режима в кинетический (n > 1). В бинарном алифатико-ароматическом растворителе процесс при разных температурах протекает как реакция первого порядка (n = 1), т.е. скорость растворения парафинов в ГБС не ограничивается ни скоростью физико-химического взаимодействия на поверхности раздела фаз, ни диффузией. Следует отметить, что добавление бензола к гексану приводит к снижению эффективной энергии активации. Известно, что [9] наиболее активными растворителями по отношению к парафинам являются низкокипящие алкановые УВ. Растворение парафинов в этих УВ объясняется [12] благоприятной сольватацией длинноцепочечных алканов алканами с более короткой углеродной цепью. Авторами работы [1] проведены систематические исследования температурной зависимости растворимости парафина в ароматических УВ, и было установлено, что в толуоле растворимость парафина имеет максимальное значение, а минимальное – в алкилбензоле. Уменьшение энергии активации разрушения парафинов в гексан-бензольной смеси, возможно, объясняется синергетическим эффектом алифатических и ароматических УВ в этой смеси по отношению к парафинам. Синергизм нафтеновых и ароматических добавок в алифатическом растворителе отмечен в работах [3, 6]. В табл. 2 приведены кинетические параметры растворения промысловых АСПО в гексане и ГБС, опубликованных в работах [4, 6].
Таблица 2
Кинетические параметры растворения АСПО парафинового типа в различных УВ
|
Образец |
t, °C |
n |
r2 |
K, мин–1 |
τ1/2, мин |
Еа, кДж/моль |
|
АСПО + Гексан |
10 |
0,84 ± 0,04 |
0,990 |
1,43∙10–2 |
– |
57,5 |
|
25 |
0,97 ± 0,03 |
0,952 |
4,89∙10–2 |
14,17 |
||
|
40 |
1,40 ± 0,03 |
0,976 |
1,81∙10–1 |
3,83 |
||
|
60 |
1,74 ± 0,11 |
0,988 |
2,97∙10–1 |
2,33 |
||
|
АСПО + Гексан + Бензол (1:1) |
10 |
0,99 ± 0,07 |
0,981 |
3,10∙10–2 |
22,36 |
39,4 |
|
25 |
1,05 ± 0,13 |
0,975 |
6,10∙10–2 |
11,36 |
||
|
40 |
1,04 ± 0,11 |
0,982 |
1,53∙10–1 |
4,53 |
||
|
60 |
1,13 ± 0,16 |
0,993 |
3,47∙10–1 |
2,00 |
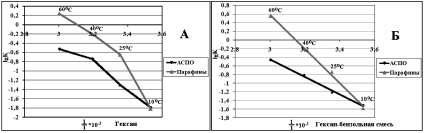
Рис. 2. Зависимость констант скорости растворения К от 1/T парафинов и АСПО в гексане (А) и в ГБС (Б)
Сравнение данных, приведенных в табл. 1 и 2, позволило установить, что процессы растворения нефтяных парафинов и АСПО парафинового типа в гексане и ГБС при исследованных температурах имеют практически идентичный характер. Так, при низких температурах процессы растворения как парафинов, так и АСПО в гексане лимитируются диффузией, а в ГБС этот процесс протекает как реакция первого порядка, а также процессы их растворения в ГБС характеризуются более низким значением эффективной энергии активации. Причем значение энергии активации разрушения АСПО в исследуемых растворителях почти в два раза меньше по сравнению с парафинами.
Исследования кинетики разрушения парафинов и АСПО [3, 6] при более высоких температурах позволили установить зависимость логарифма константы скорости растворения от величины обратной температуры (рис. 2).
Видно, что для моделей Парафины + Гексан и АСПО + Гексан опытные данные на графике в координатах lgK – 1/T располагаются на линиях с изломом, что указывает на отклонение от температурной зависимости констант скорости растворения в этих системах от уравнения Аррениуса. Возможно, это связано с тем, что измеряемая константа скорости относится более чем к одной стадии реакции. В бинарном композите исследуемая зависимость имеет линейный характер без излома.
Заключение
Таким образом, исследована и описана макрокинетика растворения нефтяных парафинов в различных УВ системах при разных температурах: определены кинетические параметры их растворения и установлены лимитирующие стадии этих процессов. Обнаружено, что процессы растворения парафинов и промысловых АСПО парафинистого типа в гексане и гексан-бензольной смеси подчиняются одинаковым закономерностям и протекают по одному механизму. Возможно, что проведенное исследование позволит прогнозировать поведение промысловых АСПО парафинового типа в различных УВ системах, основываясь на экспериментальных данных изучения модельных процессов растворения нефтяных парафинов в случае, когда забор проб АСПО непосредственно на месторождении или их доставка представляет трудную задачу.
Работа поддержана Интеграционным проектом СО РАН № 19 «Газовые гидраты в нефтяной промышленности» (2012–2014 гг.).
Рецензенты:
Охлопкова А.А., д.т.н., профессор, зав. кафедрой высокомолекулярных соединений и органической химии Института естественных наук, ФГАОУ «Северо-Восточный федеральный университет им. М.К. Аммосова», г. Якутск;
Степанов А.В., д.т.н., главный научный сотрудник отдела тепломассообменных процессов, ФГБУН «Институт физико-технических проблем Севера» СО РАН, г. Якутск.
Работа поступила в редакцию 23.10.2014.
Библиографическая ссылка
Иванова И.К. СРАВНЕНИЕ КИНЕТИЧЕСКИХ ПАРАМЕТРОВ РАСТВОРЕНИЯ В РАЗЛИЧНЫХ УГЛЕВОДОРОДАХ НЕФТЯНЫХ ПАРАФИНОВ И ПРОМЫСЛОВЫХ АСФАЛЬТОСМОЛОПАРАФИНОВЫХ ОТЛОЖЕНИЙ ПАРАФИНОВОГО ТИПА // Фундаментальные исследования. 2014. № 11-5. С. 1028-1031;URL: https://fundamental-research.ru/en/article/view?id=35672 (дата обращения: 13.05.2026).



