Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
PARTIAL DELETIONS OF FOXK1 IN CHILDREN WITH AUTISM: IDENTIFICATION OF A NEW CANDIDATE GENE OF AUTISTIC SPECTRUM DISORDERS BY POSTGENOMIC TECHNOLOGIES
Многие работы в области биологической психиатрии и психиатрической генетики последних лет демонстрируют связь между аутизмом и геномными вариациями. У детей с аутистическими расстройствами выявляются регулярные структурные хромосомные аберрации, включая интерстициальные микроделеции/микродупликации, и вариации числа копий последовательностей ДНК (CNV), затрагивающие гены, многие из которых рассматриваются в качестве кандидатов для этого заболевания [3–6, 11]. С внедрением методов, позволяющих сканировать геном с высоким разрешением (в частности, молекулярное кариотипирование), количество позитивных ассоциаций между геномной патологией и аутизмом в значительной степени увеличилось [2, 6, 10]. Помимо этого, применение технологий изучения межклеточных вариаций генома также демонстрирует большое число случаев (до 16 %) аутистических расстройств, связанных с соматическим мозаицизмом (наличие нескольких популяций клеток в организме, отличающихся друг от друга по геномному составу) [7, 8, 16]. Более того, вариабельность участков генома, содержащих последовательности ДНК, которые до сих пор остаются фактически неизвестными (гетерохроматиновые участки хромосом), также считается одним из факторов риска развития аутизма [1, 15]. Создание унифицированного каскада патогенетических процессов, включающего весь широкий спектр вариабельности генома при данных формах нарушения психики, является одним из приоритетов в современной психиатрической генетики, в рамках основной парадигмы которой поиск генов-кандидатов аутизма считается основополагающим. Наличие соответствующих данных также позволяет определять молекулярные механизмы заболевания с целью последующей разработки научно обоснованной терапии [5].
Целью настоящей работы явился поиск генов-кандидатов в группе 64 детей с аутизмом с помощью постгеномных технологий: молекулярное кариотипирование или высокоразрешающее сканирование генома с разрешением не менее 1 тыс. пн и биоинформатический анализ, включающий в себя оценку патогенности вариаций генома с помощью геномных, эпигеномных и протеомных баз данных, а также моделирования белковых взаимодействий (интерактомный анализ).
Материалы и методы исследования
Полногеномное сканирование было использовано для анализа 64-х образцов ДНК периферической крови детей с клиническим диагнозом «аутистические расстройства», входящих в российскую когорту детей с аутизмом, описанную ранее [1, 2, 5, 10, 15, 16]. Молекулярное кариотипирование проводилось с использованием высокоразрешающих чипов Affymetrix (CytoScan HD) для SNP (single nucleotide polymorphism)/олигонуклеотидной сравнительной геномной гибридизации (разрешение 1000 пн и более) в соответствии с протоколами, представленными ранее [2, 10]. Биоинформатический анализ выявленных перестроек включал в себя оценку патогенности с помощью геномных, эпигеномных/транскриптомных, протеомных и метаболических баз данных. Оригинальная биоинформатическая технология подробно описана в предыдущих работах [9, 10]. Интерактомная цепочка для анализа взаимодействий белка, кодируемым геном FOXK1, была получена с использованием программы Cytoscape 2.8.3 [12].
Результаты исследования и их обсуждение
В ходе анализа генома 64 пациентов у двух (3,1 %) были обнаружены CNV в виде делеций последовательности ДНК гена FOXK1. В первом случае делеция затронула семь экзонов гена FOXK1 (с третьего по девятый) и гены KIAA0415 и RADIL. Биоинформатический анализ этих двух генов показал, что вероятность их ассоциации с аутистическими расстройствами крайне мала. Во втором случае делеция затронула первый экзон гена FOXK1 (рис. 1).
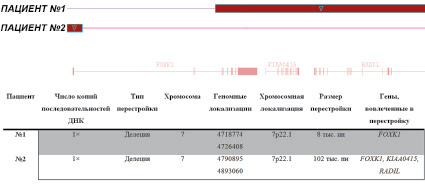
Рис. 1. Схематическое изображение делеций, затронувших ген FOXK1, которые были выявлены у двух пациентов с помощью полногеномного сканирования, с обозначением геномной и хромосомной локализации, размера перестройки и других генов, вовлеченных в перестройку
Примечательно, что вариации последовательностей ДНК гена FOXK1 ранее не были ассоциированы с какими-либо фенотипическими проявлениями. Ранее было лишь показано, что ген FOXK1 обладает повышенной экспрессией в нервных клетках у млекопитающих [13] и вовлечен в геномную цепочку регуляции пролиферации клеток [14]. С другой стороны, биоинформатический анализ показывает, что данный ген, скорее всего, кодирует белок-регуляции транскрипции. Интерактомный анализ (изучение межбелковых взаимодействий продукта транскрипции гена-мишени) (рис. 2) свидетельствует о том, что нарушение функционирования FOXK1 связано с изменениями в следующих внутриклеточных процессах: регуляция митотического деления клеток, апоптоза и экспрессии генов (за счет нарушения взаимодействия с YWHAB); ремоделирование хроматина (за счет нарушения взаимодействия с BAP1); внутриутробное развитие (за счет нарушения взаимодействия с AMOT); метаболизм ионов металлов (за счет нарушения взаимодействия с FYCO1).
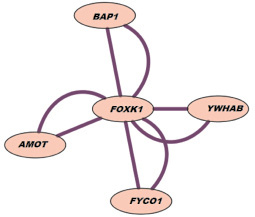
Рис. 2. Результаты интерактомного анализа, демонстрирующего взаимодействие белка, кодируемого геном FOXK1 с помощью программы Cytoscape 2.8.3 [12]
Примечательно, что нарушения регуляции митоза и/или апоптоза рассматриваются как факторы риска при аутизме, являясь причиной хромосомного мозаицизма и нестабильности, наблюдаемых при этом заболевании [4–7, 15, 16], а изменения таких эпигенетических феноменов, как регуляция экспрессии генов и ремоделирование хроматина неоднократно ассоциировались с различными формами аутистических расстройств [1, 5, 6, 11]. Совокупность полученных биоинформатических данных позволяет сделать вывод о том, что мутации в гене FOXK1 могут приводить к нарушениям психики, а вывод о том, что он является геном-кандидатом аутизма, является обоснованным.
Заключение
Анализ генома с целью выявления генов-кандидатов аутистических расстройств и патогенетических процессов, характерных для этого заболевания, является неотъемлемой частью современных исследований в области психиатрической генетики и биологической психиатрии [3–8, 11]. Однако, несмотря на повышенный интерес к генетике аутизма, существует ряд проблем при выявлении молекулярных основ подобных форм нарушения психики, связанных преимущественно с интерпретацией обнаруженных геномных вариаций. Преодоление подобных сложностей, как было показано ранее [9, 10], возможно только при использовании биоинформатических технологий в дополнение к методам высокоразрешающего сканирования генома. Применяя комплекс постгеномных технологий, сочетающий молекулярное кариотипирование и биоинформатический анализ, был обнаружен новый ген-кандидат аутизма. В связи с этим, принимая во внимание потенциал сканирования генома и оригинальных технологий in silico, использованных в настоящей работе, можно с уверенностью утверждать, что описываемый подход к поиску генетических изменений, приводящих к аутизму, является эффективным.
Исследование выполнено за счёт гранта Российского Научного Фонда (проект № 14-35-00060).
Работа поступила в редакцию 10.10.2014.
Библиографическая ссылка
Юров И.Ю., Юров И.Ю., Юров И.Ю., Ворсанова С.Г., Ворсанова С.Г., Ворсанова С.Г., Васин К.С., Васин К.С., Коростелев С.А., Юров Ю.Б., Юров Ю.Б., Юров Ю.Б. ЧАСТИЧНЫЕ ДЕЛЕЦИИ ГЕНА FOXK1 У ДЕТЕЙ С АУТИЗМОМ: ОПРЕДЕЛЕНИЕ НОВОГО ГЕНА-КАНДИДАТА АУТИСТИЧЕСКИХ РАССТРОЙСТВ С ПОМОЩЬЮ ПОСТГЕНОМНЫХ ТЕХНОЛОГИЙ // Фундаментальные исследования. 2014. № 10-4. С. 767-770;URL: https://fundamental-research.ru/en/article/view?id=35620 (дата обращения: 06.05.2026).



