Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THE ACTUAL ASPECTS OF THE CREATION OF DOMESTIC PHYTOPHARMACEUTICALS
В настоящее время одной из актуальных задач фармацевтической науки является создание и внедрение импортозамещающих лекарственных средств, в том числе лекарственных препаратов растительного происхождения. Актуальность данной проблемы обусловлена тем обстоятельством, что на фармацевтическом рынке Российской Федерации значительный удельный вес занимают зарубежные средства, причем, как правило, дорогостоящие. Создание и внедрение конкурентоспособных импортозамещающих лекарственных средств, с одной, стороны, будет способствовать успешной реализации Стратегии лекарственного обеспечения населения Российской Федерации на период до 2025 года, а с другой, позволит обеспечить лекарственную безопасность страны. Актуальность исследований в области создания лекарственных растительных препаратов обусловлена также тем обстоятельством, что, в соответствии с прогнозом ВОЗ, через 15–20 лет доля фитопрепаратов в общем ассортименте лекарственных средств может составить около 60 % [3]. Данный прогноз можно объяснить тем фактом, что лекарственные средства растительного происхождения, обладающие мягкостью терапевтического действия наряду с отсутствием выраженных побочных эффектов, широко применяются для профилактики и лечения различных заболеваний [2–5]. В этом отношении особый интерес представляют лекарственные растения, содержащие фенилпропаноиды, флавоноиды, антраценпроизводные, сапонины, причем часто в одном виде лекарственного растительного сырья (ЛРС) имеет место сочетание нескольких групп действующих веществ, что и обусловливает широкую амплитуду биологической активности [1–8]. Лекарственные растения, содержащие вышеперечисленные биологически активные соединения (БАС), являются ценным источником тонизирующих, адаптогенных, антидепрессантных, ноотропных, анксиолитических, седативных, гепатопротекторных, антиоксидантных, иммуномодулирующих, антимикробных, противовоспалительных, слабительных фитопрепаратов [1–8].
Цель исследования – обоснование целесообразности создания конкурентоспособных импортозамещающих лекарственных растительных препаратов.
Материал и методы исследования
В качестве объектов использованы корневища и биомасса родиолы розовой (Rhodiola rosea L.), кора сирени обыкновенной (Syringa vulgaris L.), корневища и корни элеутерококка колючего [Eleutherococcus senticosus (Rupr. et Maxim.) Maxim.], кора сирени обыкновенной (Syringa vulgaris L.), семена и плоды лимонника китайского (Schizandra chinensis Baill.), трава мелиссы лекарственной (Melissa officinalis L.), цветки лаванды колосовой (Lavandula spica L.), листья гинкго двулопастного (Ginkgo biloba L.), трава зверобоя продырявленного (Hypericum perforatum L.) и зверобоя пятнистого (Hypericum maculatum Grantz.), трава эхинацеи пурпурной [Echinacea purpurea (L.) Moench.], плоды расторопши пятнистой [Silybum marianum (L.) Gaertn.], цветки пижмы обыкновенной (Tanacetum vulgare L.), цветки бессмертника песчаного [Helichrysum arenarium (L.) Moench.], почки тополя черного (Populus nigra L.), цветки календулы лекарственной (Calendula officinalis L.), кора ивы остролистной (Salix acutifolia Willd.), листья березы бородавчатой (Betula verrucosa Ehrh.), корни солодки голой (Glycyrrhiza glabra L.), трава гречихи посевной (Fagopyrum sagittatum Gilib.), плоды черники обыкновенной (Vaccinium myrtillus L.), плоды жостера слабительного (Rhamnus cathartica L.), кора крушины ломкой (Frangula alnus Mill.), листья кассии остролистной (Сassia acutifolia Del.), корни щавеля конского (Rumex confertus Willd.), корни женьшеня настоящего (Panax ginseng C.A. Meyer), а также фенилпропаноиды, флавоноиды, антраценпроизводные и сапонины, выделенные из исследуемого ЛРС.
В работе использованы тонкослойная хроматография (ТСХ), высокоэффективная жидкостная хроматография (ВЭЖХ), спектрофотометрия, 1Н-ЯМР-спектроскопия, масс-спектрометрия, различные химические превращения. 1Н-ЯМР-спектры получали на приборах «Bruker AM 300» (300 МГц), масс-спектры снимали на масс-спектрометре «Kratos MS-30», регистрацию УФ-спектров проводили с помощью спектрофотометра «Specord 40» (Analytik Jena). Воздушно-сухое растительное сырье подвергали исчерпывающему экстрагированию 70 % спиртом этиловым, полученные водно-спиртовые экстракты упаривали под вакуумом до густого остатка и далее подвергали хроматографическому разделению на силикагеле L 40/100 и полиамиде «Woelm». Контроль за разделением веществ осуществляли с помощью ТСХ-анализа на пластинках «Сорбфил ПТСХ-АФ-А-УФ» в системах хлороформ – этанол (9:1), хлорофор – этанол – вода (26:16:3), а также н-бутанол – ледяная уксусная кислота – вода (4:1:2).
Результаты исследования и их обсуждение
В результате изучения химического состава целого ряда лекарственных растений выделены и охарактеризованы с использованием УФ-, ЯМР-спектроскопии, масс-спектрометрии, ТСХ и ВЭЖХ, различных химических превращений фенилпропаноиды (1-8), флавоноиды (9-20), антраценпроизводные (21-24) и сапонины (25 и 26), представляющие интерес с точки зрения химической стандартизации сырья и препаратов соответствующих лекарственных растений (рис. 1–4).
На основе изучения химического состава целого ряда видов ЛРС обоснованы подходы к стандартизации сырья и фитопрепаратов, заключающиеся в использовании в методиках анализа стандартных образцов розавина (родиола розовая), триандрина (биомасса родиолы розовой), сирингина (элеутерококк колючий, сирень обыкновенная), силибина (расторопша пятнистая), лавандозида (лаванда колосовая), розмариновой кислоты (мелисса лекарственная), цикориевой кислоты (эхинацея пурпурная), гамма-схизандрина (лимонник китайский), гинкгетина (гинкго двулопастный), 3,811-биаспигенина (зверобой продырявленный), тилианина (пижма обыкновенная), цинарозида (пижма обыкновенная), гиперозида (береза бородавчатая, зверобой пятнистый), никотифлорина (гинкго двулопастный), нарциссина (календула лекарственная), изосалипурпозида (бессмертник песчаный), ликуразида, глицирризиновой кислоты, глицирама (солодка голая), пиностробина (тополь черный), цианидин-3-О-глюкозида (черника обыкновенная), франгулина А (крушина ломкая, жостер слабительный), сеннозида В (кассия остролистная), 1,7-дигидрокси-3-карбоксиантрахинона (кассия остролистная), 8-О-β-D-глюкопиранозида эмодина (щавель конский) и гинзенозида Rg1 (женьшень настоящий).
|
|
|
|
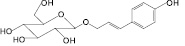
Розавин (1): родиола розовая |
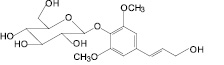
Триандрин (2): родиола розовая (биомасса) |
|
|
|
|
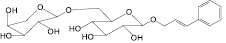
Сирингин, или элеутерозид В (3): элеутерококк колючий, сирень обыкновенная |
Лавандозид (4): лаванда колосовая |
|
|
|
|
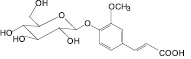
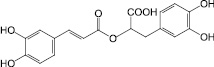
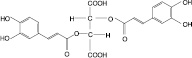
Розмариновая кислота (5): мелисса лекарственная |
Цикориевая кислота (6): эхинацея пурпурная |
|
|
|
|
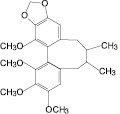
Гамма-схизандрин (7): лимонник китайский |
Силибин (8): расторопша пятнистая |
Рис. 1. Фенилпропаноиды лекарственных растений
Разработаны методики качественного и количественного анализа биологически активных соединений сырья вышеперечисленных лекарственных растений с использованием тонкослойной хроматографии, высокоэффективной жидкостной хроматографии и спектрофотометрии. Обоснованы технологии получения лекарственных субстанций и фитопрепаратов, обладающих выраженными тонизирующими, адаптогенными, антидепрессантными, ноотропными, анксиолитическими, седативными, гепатопротекторными, антиоксидантными, иммуномодулирующими, антимикробными, противовоспалительными, слабительными свойствами, превосходящими соответствующие эффекты отечественных и зарубежных аналогов.
|
|
|
|
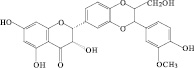
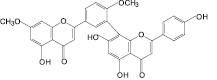
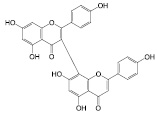
Гинкгетин (9): гинкго двулопастный |
3,81-Бисапигенин (10): зверобой продырявленный |
|
|
|
|
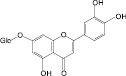
Тилианин (11): пижма обыкновенная |
Цинарозид (12): пижма обыкновенная |
|
|
|
|
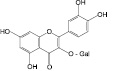
Гиперозид (13): береза бородавчатая, зверобой пятнистый |
Никотифлорин (14): гинкго двулопастный |
|
|
|
|
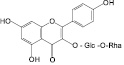
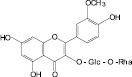
Рутин (15): зверобой продырявленный, гречиха посевная и др. |
Нарциссин (16): календула лекарственная |
|
|
|
|
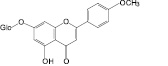
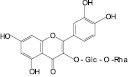
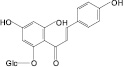
Изосалипурпозид (17): бессмертник песчаный, ива остролистная |
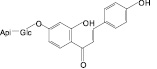
Ликуразид (18): солодка голая |
|
|
|
|
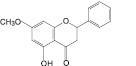
Пиностробин (19): тополь черный |
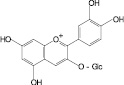
Цианидин-3-О-глюкозид (20): черника обыкновенная |
Рис. 2. Флавоноиды лекарственных растений
|
|
|
|
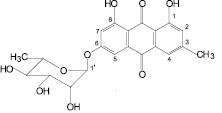
Франгулин А (21): крушина ломкая, жостер слабительный |
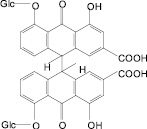
Сеннозид В (22): кассия остролистная |
|
|
|
|
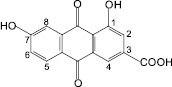
1,7-Дигидрокси-3-карбоксиантрахинон (23) (10): кассия остролистная |
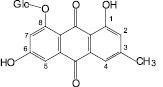
8-О-?-D-глюкопиранозид эмодина (24): щавель конский |
Рис. 3. Антраценпроизводные лекарственных растений
|
|
|
|
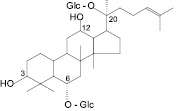
Гинзенозид Rg1 (25): женьшень настоящий |
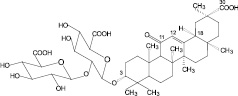
Глицирризиновая кислота (26): солодка голая |
Рис. 4. Сапонины лекарственных растений
Выводы
Таким образом, в результате проведенных исследований обоснованы новые подходы к стандартизации лекарственного растительного сырья и фитопрепаратов, содержащих фенилпропаноиды, флавоноиды и антраценпроизводные с использованием ТСХ, ВЭЖХ, спектрофотометрии и соответствующих стандартных образцов. На основе изучения физико-химических, химических, спектральных и фармакологических свойств фенилпропаноидов, флавоноидов, антраценпроизводных и сапонинов обоснована целесообразность создания целого ряда импортозамещающих лекарственных средств, обладающих выраженными тонизирующими, адаптогенными, антидепрессантными, ноотропными, анксиолитическими, седативными, гепатопротекторными, антиоксидантных, иммуномодулирующими, антимикробными, противовоспалительными, слабительными свойствами.
Рецензенты:
Первушкин С.В., д.фарм.н., профессор, зав. кафедрой фармацевтической технологии, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Самара;
Дубищев А.В., д.м.н., профессор, зав. кафедрой фармакологии им. заслуженного деятеля науки РФ, профессора А.А. Лебедева, ГБОУ ВПО «Самарский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Самара.
Работа поступила в редакцию 06.10.2014.
Библиографическая ссылка
Куркин В.А., Петрухина И.К. АКТУАЛЬНЫЕ АСПЕКТЫ СОЗДАНИЯ ИМПОРТОЗАМЕЩАЮЩИХ ЛЕКАРСТВЕННЫХ РАСТИТЕЛЬНЫХ ПРЕПАРАТОВ // Фундаментальные исследования. 2014. № 11-2. С. 366-371;URL: https://fundamental-research.ru/en/article/view?id=35529 (дата обращения: 05.05.2026).