Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
FEATURE IMMUNOCYTES CD4/CD8 OF MUCOUS MEMBRANE IN PATHOGENESIS ODONTOGENIC MAXILLARY SINUSITIS
На современном этапе болезни околоносовых пазух являются самой распространенной ЛОР-патологией [7, 10, 13, 19]. Oколо 40 % всех госпитализированных лорбольных составляют пациенты с синуситами. Частой причиной развития верхнечелюстных синуситов являются тесные топографо-анатомические взаимоотношения верхнечелюстной пазухи (ВЧП) с зубами верхней челюсти [1, 2, 4, 16]. По мнению многих авторов, особенности строения стенки верхнечелюстной пазухи повышают степень риска возникновения внутриглазничных и внутричерепных осложнений при воспалительных заболеваниях этой пазухи, что требует участия различных специалистов: офтальмологов, челюстно-лицевых хирургов, стоматологов, отоларингологов и нейрохирургов [18]. Основным методом диагностики заболеваний околоносовых пазух (ОНП) в настоящее время является рентгенологический, который, как и жесткая эндоскопия носовой полости, и возможность компьютерного сканирования (КТ) синусов, тем не менее, не позволяет комплексно оценить состояние всех ОНП, не даёт полного представления о динамике патологического процесса и патогенетических механизмах [8, 14, 15]. Следует учесть, что ни один из этих диагностических методов не доступен для врача общей практики, которому нередко приходится ставить диагноз и лечить синусит на основании клинических симптомов. Диагностика и лечение болезней придаточных пазух носа (ППН) связаны с неспецифичностью и неинформативностью неинвазивных методов обследования. При этом КТ подвергает пациента значительному облучению. Запущенный синусит приводит к распространению инфекции за пределы пазух, приводя к серьезным осложнениям, чаще у детей [3, 5, 12] . При этом, как следствие, эмпирическая неадекватная антибиотикотерапия не является полностью патогенетически обоснованной: при остром синусите отсутствует единое мнение о выборе антибиотика и продолжительности курса лечения, что также подтверждают данные об особенностях анаэробной инфекции у пациентов с различными формами хронических максиллярных синуситов [11]. Микроорганизмы, присутствующие в околоносовых пазухах, не реагируют на антибактериальные средства. Опасность длительного курса антибиотиков заключается в развитии антибиотикорезистентности, риске остаточной инфекции с высокой вероятностью развития осложнений. Поэтому разработка методов гистологической и иммуногистохимической оценки патологического процесса в слизистой оболочке гайморовой пазухи с использованием маркеров CD4/CD8 является наиболее актуальной на современном этапе.
Цель исследования. Установить особенности взаимодействия CD4:CD8 в структурах слизистой гайморовой пазухи и их роль в патогенезе одонтогенного гайморита.
В задачи исследования мы включили получение характеристики морфологических особенностей альтерации структур слизистой оболочки верхнечелюстной пазухи в зависимости от сроков заболевания, а также выявление количественной динамики изменений CD4:CD8 в гайморовой пазухе в зависимости от возраста и давности заболевания.
Материалы и методы исследования
Исследование было проведено с учётом положений Хельсинской декларации (2000) и с разрешением этического комитета ФГАОУ ВПО Дальневосточный Федеральный Университет. По клиническим показаниям и с письменного информированного согласия пациентов с учётом зависимости показателей от циркадных ритмов произвели забор биоптатов слизистой гайморовой пазухи у 42 пациентов в возрасте от 45 до 78 лет, которых распределили с учётом возрастных групп, принятых Международным симпозиумом по возрастной периодизации в Москве (1965 г.) и сроков заболевания одонтогенным гайморитом (табл. 1).
Таблица 1
Распределение больных с учётом возрастной периодизации и сроков давности одонтогенного гайморита
|
Количество больных в возрастных группах |
Всего больных |
Продолжительность заболевания |
||||
|
1 мес. |
1,5 мес |
3 мес. |
0,5 года |
1 год и более |
||
|
VI |
5 |
1 |
1 |
1 |
1 |
1 |
|
VII |
7 |
1 |
1 |
2 |
2 |
1 |
|
VIII |
5 |
1 |
2 |
1 |
1 |
1 |
|
IX |
3 |
1 |
0 |
0 |
0 |
1 |
|
X |
6 |
1 |
1 |
2 |
2 |
0 |
|
XI |
7 |
3 |
1 |
1 |
1 |
1 |
|
XII |
9 |
3 |
3 |
1 |
1 |
1 |
|
Итого |
42 |
11 |
9 |
8 |
8 |
6 |
Клинический анализ материала показал, что причинами одонтогенного гайморита в большинстве случаев были мероприятия по имплантации зубов (35), ретенционные зубы (2) и инфицирование в результате кариозного поражения зубов (5).
По клиническим показаниям и с согласия пациентов производили забор биоптатов с помощью интраназальной этмоидэктомии, образцы нормальный слизистой оболочки были получены из области задней решетчатой пазухи от трех пациентов, у которых заболевание было ограничено передним решётчатым регионом. Кроме того, ни один из этой группы пациентов не получал интраназальных препаратов, оральных стероидов, а также антибиотиков для лечения в течение предыдущих 6 месяцев. Все они имели отрицательные результаты на аллергические пробы. Полученные биоптаты фиксировали в 10 %-м формалине на фосфатном буфере с рН 6,8–7,2 в течение 24-х часов, затем промывали в воде в течение 2-х часов и обезвоживали в спиртах возрастающей концентрации в течение 1 часа в каждой порции. В спирте 96 °С выдерживали в течение 1, 2, 4-х часов, а затем помещали в абсолютный спирт 5 раз по 30 минут, потом оставляли в последней порции на всю ночь. После этого материал помещали в смесь абсолютного спирта и ксилола в соотношении 1:1 на 30 минут, а затем в сменах ксилола в термостате при 37 °С по 30 минут в каждой. После этого использовали смесь ксилола с парафином (1:1) при 56 °С по 20 минут в 2-х порциях, а затем в двух порциях парафина при 56 °С (по 1 часу в каждой порции), после чего проводили заливку. Парафиновые блоки выдерживали в течение суток в термостате при 37 °С, после чего производили срезы толщиной 3–5 мкм. Срезы и вся дальнейшая обработка материала (депарафинирование и обезвоживание) выполнялась на автоматизированной аппаратуре лаборатории патоморфологии Международного медицинского научно-образовательного центра (IMERC, Ниигата, Япония). Идентификация иммунокомпетентных клеток проводилась по одинаковой схеме, в связи с одинаковой локализацией антигена в клеточных структурах. Иммуногистохимическими методами на определение CD4/CD8 в биоптатах слизистой гайморовой пазухи, произвели фенотипирование иммуноцитов и проанализировали их количественные соотношения в слизистой оболочке гайморовой пазухи в норме, а также выявили особенности топографии иммуноцитов при одонтогенном гайморите. Демаскировка антигенных детерминант проводилась в стеклянном контейнере, заполненном восстанавливающим раствором, с созданием водяной бани в течение одного часа. Часть препаратов была обработана в течение 30 минут с помощью микроволнового излучения, которое даёт лучший демаскировочный эффект. Для демаскировки антигенов использовали 10 ммоль/л цитратный буфер с рН 6,0 или DAKO TRS (Target retrieval solution, code № S1700). Остывшие препараты промывали в дистиллированной воде. Антитела применяли в разведении 1:50 и 1:100. Анализ материала проведён с помощью микроскопа Olympus – Bx82 и цифровой камеры РDх25.
Результаты исследования и их обсуждение
Нами установлено, что в группе обследованных пациентов развитие одонотогенного верхнечелюстного синусита чаще было связано с тем, что нижняя стенка, или дно, верхнечелюстной пазухи находилось вблизи задней части альвеолярного отростка верхней челюсти и обычно соответствовало лункам четырех задних верхних зубов, корни которых в 12 случаях отделялись от пазухи лишь мягкими тканями. Также развитию патологического процесса способствовало низкое расположение дна, а также нахождение корней зубов и их луночек вблизи или даже внутри верхнечелюстной полости. При этом было отмечено, что вдающиеся в пазуху луночки зубов имели отверстия, через которые надкостница корня приходила в соприкосновение со слизистой оболочкой пазух. Это способствовало лёгкому распространению одонтогенной инфекции в соответствующих зубах на слизистую оболочку верхнечелюстной пазухи.
Слизистая оболочка, выстилающая верхнечелюстную пазуху, плотно спаяна с костными стенками. Отличие от слизистой оболочки проксимального отдела дыхательного тракта заключается в том, что она не содержит кавернозной ткани, очень тонкая, включает небольшое количество слизистых желез и обильно кровоснабжена. В норме верхнечелюстная пазуха выстлана слизистой оболочкой, покрытой многорядным призматическим мерцательным эпителием. Нами установлено, что толщина слизистой оболочки в околоносовых пазухах составляет 120–1000 мкм и не видна на рентгенограмме, но при воспалении она может увеличиваться в десятки и сотни раз, давая пристеночное затемнение.
Основными морфофункциональными единицами эпителия в пазухах являются реснитчатые, вставочные и бокаловидные клетки. Известно, что реснитчатые клетки имеют на своей поверхности 50–200 ресничек длиной 5–8, диаметром 0,15–0,3 мкм.
Нами отмечено, что препараты, изготовленные из биоптатов больных с продолжительностью процесса 1–1,5 месяца, в сравнении с нормой характеризовались гипертрофией слизистой оболочки и гиперплазией бокаловидных клеток (рис. 1 а, б, в).
 а
а 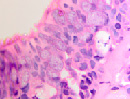 б
б 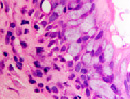 в
в
Рис. 1 а, б. А – в норме количество бокаловидных клеток 2–3 в поле зрения, идентифицируется слой ресничек. Б – гиперплазия и гипертрофия бокаловидных эпителиоцитов. В – слой ресничек разрушен (указано стрелкой). Микрофото. Окраска гематоксилин-эозином. Ув.х400
Известно, что ранние дегенеративные изменения реснитчатых эпителиоцитов проявляются уменьшением удельного объема митохондрий, гранулярной эндоллазматической сети, увеличением ядерно-цитоплазматических отношений, что связано с нарушением эвакуации секрета из бокаловидных клеток.
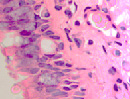
При появлении воспалительного инфильтрата в слое эпителиальной пластинки слизистой оболочки в сочетании с разрушением базальной мембраны и гибели базальных и бокаловидных клеток в отсутствие дифференцировки и специализации происходит замещение однослойных многорядных эпителиоцитов многослойным эпителием в результате реституции пролиферирующих стволовых клеток (рис. 2 а, б, в).
 а
а 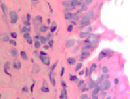 б
б 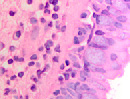 в
в
Рис. 2 а, б. А – расширение кровеносных сосудов с гипертрофированными эндотелиоцитами и лейкоцитарная инфильтрация в собственной пластинке слизистой оболочки. Кровеносный сосуд указан белой стрелкой. Б – разрушение эпителиальной пластинки, реснитчатого эпителия, апоптоз бокаловидных клеток. Микрофото. Окраска гематоксилин-эозином. Ув.х400
Кроме этого, лейкоцитарная инфильтрация, которая при инфицировании наблюдается не только в пределах собственной соединительнотканной пластинки, но и на поверхности слизистой, сопровождается разрушением базальной мембраны (рис. 2 б).
При продолжительности заболевания более 3-х месяцев развивается метаплазия эпителия в однорядный кубический и многослойный плоский ороговевающий или неороговевающий (рис. 2 в).
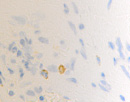
Нами установлено, что содержание СD4/ СD8 иммуноцитов в слизистой оболочке синусов постепенно увеличивается, но при продолжительности заболевания более 6 месяцев уменьшается содержание CD4 клеток, одновременно возрастает содержание CD8 как в эпителиальной пластинке, так и на поверхности слизистой оболочки (рис. 3; табл. 2).
 а
а 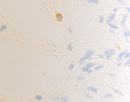 б
б 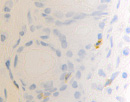 в
в
 г
г д
д
Рис. 3. а, б. А, б – CD4 инфильтрация в собственной пластинке слизистой оболочки верхнечелюстного синуса. В, г, д – идентификация CD 8 лимфоцитов как в собственной пластинке слизистой оболочки синуса, так и на поверхности эпителия. Наблюдается разрушение эпителиальной пластинки, реснитчатого эпителия, апоптоз бокаловидных клеток. Микрофото. Иммунная гистохимия. Ув.х400
Таблица 2
Показатели иммунного гомеостаза в слизистой оболочке верхнечелюстного синуса в норме и при хронической инфекции
|
Параметры фенотипирования |
CD 4 |
CD8 |
||||||
|
Продолжительность заболевания |
контроль |
1 мес. |
3–6 мес. |
1 год |
контроль |
1 мес. |
3–6 мес. |
1 год |
|
От 20 до 40 лет |
1,69 ± 0,11 |
3,78 ± 0,11 |
3,21 ± 0,05 |
2,60 ± 0,07 |
1,41 ± 0,18 |
2,79 ± 0,23 |
3,45 ± 0,27 |
3,57 ± 0,12 |
|
От 40 до 60 лет |
1,55 ± 0,09 |
2,77 ± 0,09 |
3,64 ± 0,07 |
3,24 ± 0,05 |
1,09 ± 0,24 |
2,53 ± 0,19 |
3,37 ± 0,10 |
3,44 ± 0,13 |
|
Старше 60 лет |
1,43 ± 0,25 |
2,44 ± 0,17 |
3,15 ± 0,11 |
2,99 ± 0,14 |
1,06 ± 0,19 |
2,01 ± 0,18 |
3,24 ± 0,22 |
3,35 ± 0,16 |
Примечание: критерий достоверности при уровне значимости p < 0,05.
Выявленное количество CD4/CD8 в слизистой оболочке верхнечелюстного синуса в группе контроля согласуется с данными литературы о показателях CD4/CD8 в периферической крови, количество CD4 превышает содержание CD8 во всех возрастных группах (р < 0,05). Динамика изменения количества эффекторных иммуноцитов в слизистой оболочке верхнечелюстного синуса в группе контроля согласуется с данными литературы об уменьшении с возрастом количества CD4/CD8 ежегодно на 0,09 %. Повышение соотношения CD4/CD8 отмечается в острой фазе воспалительного процесса, за счёт повышения количества Т-хелперов и снижения Т-супрессоров. При переходе воспалительного заболевания в хронический процесс отмечается медленное снижение содержания Т-хелперов и повышение количества Т-супрессоров. При стихании воспалительного процесса эти показатели и их соотношения нормализуются.
Гиперсекреция слизи является общей чертой при хронических синуситах, сопровождаясь выраженной гиперплазией бокаловидных клеток, что, по мнению, связано с генами, отвечающими за выработку муцина матричными РНК (мРНК), которые выражены в бокаловидных клетках поверхностных эпителиальных пластов респираторного тракта человека. На сегодняшний день идентифицированы 12 генов человека, отвечающие за выработку муцина (MUC1-4, MUC5AC, MUC5B, MUC6-8, MUC9, MUC11, при этом MUC12, MUC5AC, MUC5B, MUC6, MUC7 и MUC8 известны как гены, отвечающие за секреторную активность бокаловидных клеток в дистальных дыхательных путях. Увеличение количества лимфоцитов CD4/CD8 и динамика изменения их соотношения в патогенезе синусита свидетельствуют о том, что эффекторные иммуноциты обеспечивают защитные барьерные свойства покровной ткани в условиях гипер-, гипофункции и гибели эпителиальных пластов.
Таким образом, соотношение CD4/CD8 является интегральным показателем состояния иммунных процессов в слизистой оболочке верхнечелюстного синуса. Несмотря на то, что существует мнение о том, что исследование поверхностных маркеров лимфоцитов периферической крови при заболеваниях, не связанных с классифицированными иммунодефицитами или онкогематологией, не является диагностически значимым, однако эти показатели в слизистой оболочке синусов позволяют оценивать распространенность, тяжесть заболевания и патогенетические особенности воспалительного процесса, прогнозировать развитие патологии.
Фенотипирование лимфоцитов у пациентов с воспалительными заболеваниями дает дополнительную информацию о текущем состоянии больного и может использоваться для мониторинга состояния иммунной системы пациента в процессе лечения.
Работа выполнена при поддержке Научного Фонда ДВФУ и Международного гранта ДВФУ (соглашение № 13-09-0602-м_а от 6 ноября 2013 г.
Рецензенты:
Храмова И.А., д.м.н., профессор, врач акушер-гинеколог, Приморский Краевой Диагностический Центр, г. Владивосток;
Транковская Л.В., д.м.н., профессор, заведующая кафедрой гигиены ТГМУ, г. Владивосток.
Работа поступила в редакцию 25.08.2014.
Библиографическая ссылка
Рева И.В., Рева И.В., Рева Г.В., Ямамото Т., Ямамото Т., Толмачёв В.Е., Первов Ю.Ю., Догадина Н.А., Миргазизов А.М., Гилифанов Е.А., Бочаров В.С., Мухлаев С.Ю., Ким А.Р., Грахова Н.В. ХАРАКТЕРИСТИКА ИММУНОЦИТОВ CD4/CD8 CЛИЗИСТОЙ ОБОЛОЧКИ В ПАТОГЕНЕЗЕ ОДОНТОГЕННОГО ВЕРХНЕЧЕЛЮСТНОГО СИНУСИТА // Фундаментальные исследования. 2014. № 10-1. С. 160-165;URL: https://fundamental-research.ru/en/article/view?id=35233 (дата обращения: 27.04.2026).



