Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
IMPORTANCE A SYSTEM OF COMPLEMENT AND C5A SUBUNIT IN THE FORMATION SYSTEMIC INFLAMMATORY RESPONSE IN THE POSTOPERATIVE PERIOD PROSTHETIC VALVES OF HEART IN PATIENTS WITH INFECTIVE ENDOCARDITIS
Система комплемента является одним из основных механизмов реализации как врождённого, так и приобретённого иммунитета. И несмотря на то, что все активационные и регуляторные механизмы до сих пор не определены, исследования в этой области демонстрируют важность системы комплемента при тяжёлых состояниях [7]. Имеется возможность активации каскада комплемента через три пути: классическому, лектиновому и альтернативному, которые сходятся в конечной точке реализации общих эффекторных функций [4]. Каскад комплемента протекает через управляемый, ограниченный протеолиз и конформационные изменения белков. Активация комплемента сопровождается усилением фагоцитоза и цитотоксических эффектов, оказывает инициирующее влияние на все виды иммунокомпетентных клеток и усиливает их хемотаксис к очагу поражения. Появление в результате активации и протеолитического превращения белков системы комплемента цитокиноподобной субъединицы С5а сопровождается усилением воспалительной реакции и цитотоксическими эффектами [1]. В настоящее время основной объём публикаций направлен на исследование эффектов системы комплемента, связанных с противоинфекционной [11, 15] и противовирусной [13] иммунной защитой. Однако, некоторые авторы описывают связь между нарушениями в системе комплемента с тяжёлым течением сепсиса [3, 9] и формированием органных дисфункций [12]. Однако, некоторые авторы указывают на то, что до сих пор остаются недостаточно изученными некоторые механизмы активации и функционирования системы комплемента [2]. Все вышеизложенное свидетельствует о несомненном вкладе компонентов системы комплемента в патогенез системного воспаления. Однако изучение значения активации каскада этой системы по одному из известных путей применительно к патогенезу системного воспалительного ответа в послеоперационном периоде пациентов с инфекционным эндокардитом находится на начальных этапах.
Цель: изучить значение изменения активности классического, лектинового и альтернативного путей активации комплемента, а также динамику С5а субъединицы комплемента в формировании системного воспалительного ответа в послеоперационном периоде протезирования клапанов сердца пациентов с инфекционным эндокардитом.
Материалы и методы исследования
В качестве методологической основы принято ретроспективное когортное исследование в модели случай ˗ контроль. В исследование включено 110 пациентов с верифицированным диагнозом инфекционный эндокардит, подвергшихся хирургическому лечению в объёме полостной операции по протезированию клапанов сердца в условиях искусственного кровообращения на базе ФГБУ «НИИ КПССЗ» СО РАМН, г. Кемерово. Сбор материала осуществлялся с 2010 по 2013 гг.
Критерии включения: установленный клинически и инструментально диагноз инфекционного эндокардита, возраст не менее 20 и не более 70 лет, подписанное информированное согласие на участие в исследовании. Критерии исключения: смена диагноза по результатам морфологического исследования удалённых тканей, сочетанные операции, наличие в анамнезе злокачественных новообразований, отказ от участия в исследовании, развитие в госпитальном периоде после операции (до момента выписки) осложнений инфекционного генеза (сепсис и другие похожие состояния).
Диагноз инфекционного эндокардита установлен на основании анамнестических данных, клинической картины, клинико-лабораторных методов исследования (трёхкратные бактериологические исследования посевов крови, данные ЭХО-кардиографии, результаты гистологического исследования удалённых клапанов сердца).
Все пациенты прошли предоперационную подготовку (в том числе курс антибиотикотерапии), находились в «холодном периоде» основного заболевания (степень активности инфекционного эндокардита на момент операции минимальна), были компенсированы по степени хронической сердечной недостаточности (не более IIБ стадии по Василенко-Стражеско).
Наличие и выраженность системного воспалительного ответа (СВО) в послеоперационном периоде оценивали по критериям R. Bone (Bone R.C. 1992), степень тяжести состояния пациента – по шкале APACHE II (Acute Physiology And Chronic Helth Evalution) (Knaus W.A., 1985), степень полиорганной недостаточности (ПОН) по шкале SOFA (Sepsis-Related Organ Failure Assessment) (J-L. Vincent et al., 1996). По клиническому течению послеоперационного периода все пациенты были разделены на три группы: 1-я группа (без осложнений) – 36 пациентов, имеющих в послеоперационном периоде не более 2-х признаков СВО по R.Bone, APACHE II 0–1 балл, SOFA- 0–1 балл; 2-я группа (осложненный СВО) – 49 пациентов имеющих 3 и более критерия по R. Bone, APACHE II 2–3 балла SOFA – 1–2 балла в 1-е сутки. И 25 человек составили 3-ю группу (СВО с ПОН) – 3 и более признака СВО по R. Bone, APACHE II 3–4 балла и более 3 баллов по шкале SOFA.
Средний возраст пациентов в исследовании составил 50 (36; 58) лет, при этом 71 человек (64,55 %) – мужчин и 39 человек (35,45 %) – женщин.
Кровь забирали из центральной локтевой вены в вакуумные коммерческие пробирки с активатором свёртывания. Cыворотку аликвотировали, хранили при -700 C. Скрининг активации комплемента по одному из путей проводили с использованием коммерческих наборов «Wieslab®Complement system Scrinkit» (Euro Diagnostica Headquarters, Швеция). Количественное определение С5а компонента комплемента с использованием коммерческого набора «HUMAN C5a EISA TEST KIT» (Hycult Biotech, Нидерланды). Исследования проводились по протоколам производителя в следующие сроки: до операции, в 1-е и на 7-е сутки после операции. Статистический анализ проводили непараметрическими методами с использованием Statistica 6.0. Результаты выражали в виде медианы (МЕ) и 25 % и 75 % межквартильных отклонений. Различия считали значимыми при уровне р < 0,01.
Результаты исследования и их обсуждение
Определили, что до операции у всех обследованных пациентов активность комплемента, независимо от пути инициализации (рис. 1), находилась на одном уровне (р ˃ 0,01).
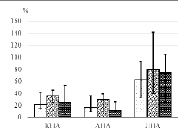
До операции
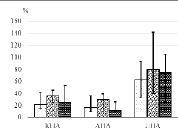
1-е сутки после операции
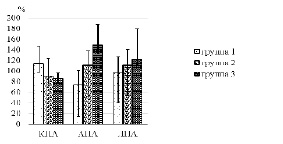
7 – сутки после операции
Рис. 1. Динамика инициализации комплемента в периоперационном периоде пациентов с инфекционным эндокардитом, КПА – классический путь активации, АПА – альтернативный путь активации, ЛПА – лектиновый путь активации
Однако активность лектинового пути в это время была выше (р < 0,01), чем у двух других путей инициализации комплемента (таблица), несмотря на значительные межиндивидуальные различия у пациентов одной группы. Учитывая известные данные о непосредственной связи этого пути комплемента с противоинфекционной защитой [10], можно заключить, что его активность до операции напрямую связана с профилем активности врождённого иммунного ответа, сформированным в результате течения инфекционного эндокардита.
Активность комплемента до операции у пациентов с инфекционным эндокардитом, в %
|
Группа |
Путь активации комплемента |
Р = |
||
|
Классический |
Альтернативный |
Лектиновый |
||
|
Без осложнений (n = 26) |
20, 00 (14,00; 42,00) |
16,97 (9,53; 35,37) |
62,34 (32,39; 93,17) |
р 1 ,3 < 0,01 р 2,3 < 0,01 |
|
Осложнённого СВО (n = 22) |
35,30 (25,00; 45,00) |
30,28 (10,51; 38,76) |
79,67 (39,43; 141,33) |
р 1 ,3 < 0,01 р 2,3 < 0,01 |
|
СВО с ПОН (n = 20) |
25,00 (5,00; 53,00) |
11,10 (10,01; 25,61) |
74,21 (25,61; 104,98) |
р 1 ,3 < 0,01 р 2,3 < 0,01 |
В раннем послеоперационном периоде межгрупповых различий по активности лектинового пути активации комплемента также не было (Н = 5,53, р = 0,06), а его активность в целом не претерпевала значительных (р ˃ 0,01) изменений (рис. 1). Так, у пациентов 1-й группы его активность была на уровне 77,38 (34,05; 143,03) %, у пациентов 2-й группы -77,02 (56,76; 111,57) % и 3-ей – 105,08 (96,93; 143,85) %. Это косвенно подтверждает неинфекционный генез системного воспалительного ответа у пациентов в этот момент послеоперационного периода.
В это время основным инициирующим путём активации комплемента являлся классический. Так, в 1-е сутки после операции его активность усилилась у пациентов всех анализируемых групп. По сравнению с дооперационным его активность значительно усилилась как у пациентов 1-й группы (60,53 (38,05; 95,96) %, р = 0,0001), так и у пациентов 2-й (104,42 (85,09; 130,05) %, р < 0,0001) и 3-ей (156,73 (100,38; 251,62) %, р < 0,0001). При этом наибольшая активность определена в группе СВО с ПОН (р < 0,0001). Высокая активность классического пути комплемента в это время может быть связана с необходимостью противостоять постишемической транслокации микрофлоры из кишечника, а также инициирована механическим повреждением тканей и проведением искусственного кровообращения [6]. В то же время, в одном из исследований [8], была показана прямая корреляционная связь чрезмерной активации каскада комплемента и фатальным исходом реперфузионных повреждений миокарда после нелетальной остановки сердца, что отражалось в динамике активации комплемента по данному пути. И если в 1-е сутки лидировала активность классического пути у пациентов группы СВО с ПОН, то в позднем послеоперационном периоде уровень активности в разных группах не имел значимых отличий (Н = 0,77, р = 0,68). Это произошло как за счёт очередного значимого подъёма активности у пациентов группы без осложнений (113,85 (66,86; 156,19) %, р = 0,01), так и за счёт снижения у пациентов с СВО с ПОН (86,03 (78,75; 97,119), р = 0,032). Обращает внимание, что у пациентов с осложнённым СВО активность осталась в диапазоне значений, регистрируемых в раннем послеоперационном периоде (90,56 (75,14; 123,62) %, р = 0,68). Высокая активность классического пути связывается с нарастанием в сыворотке крови титра антител, как эндогенной, так и микробной природы. Благодаря адекватному реагированию врождённой иммунной системы транзиторная постишемическая транслокация микрофлоры не имела фатального значения, а презентация антигена клеткам адаптивного иммунного ответа позволила к 7-м суткам переключить иммунную защиту на следующий уровень, с синтезом специфических антител.
Одновременно в 1-е сутки после операции регистрировалось усиление активности альтернативного пути комплемента (р < 0,01) у пациентов всех групп. Для пациентов группы без осложнений уровень активности соответствовал 40,58 (28,74; 83,95) %, группы осложнённого СВО – 73,21 (22,81; 100,70) %, а при СВО с ПОН поднимался до 96,93 (86,47; 111,03) %. Однако межгрупповых различий в это время определено не было (Н = 5,73, р = 0,057). Затем, в позднем послеоперационном периоде, инициализация комплемента по альтернативному пути у всех пациентов продолжалась (р < 0,01). Наибольшая его активность на 7-е сутки наблюдалась у пациентов с СВО с ПОН (149,40 (136,39; 187;71) %), а наименьшая у пациентов без осложнений (73,65 (57,33; 84,05) %). Активность альтернативного пути комплемента у пациентов с осложнённым течением СВО в это время была на промежуточном уровне между двумя вышеописанными группами (110,94 (51,97; 138,34) %). Таким образом, в случае развития системного ответа по варианту СВО с ПОН отмечается потеря контроля регуляции активности этого пути. Схожая динамика, но меньшей степени выраженности, отмечается у пациентов группы осложнённого СВО. Однако регистрируемые уровни активности ниже, что обеспечивает более низкую степень тканевых повреждений и абортивность органной дисфункции.
Следует отметить, что на протяжении всего периоперационного периода динамика активации лектинового пути комплемента также имела свои особенности в зависимости от варианта течения СВО. Для варианта СВО с ПОН было характерно значительное усиление его активности к концу наблюдения (122,00 (111,19; 179,12) %, р = 0,01), такая же тенденция прослеживалась и при неосложнённом СВО (97,07 (60,28; 137,98), р = 0,006). В то же время, у пациентов группы осложнённого СВО значимых отличий активности от уровня до операции (111,15 (54,52; 140,64), р = 0,22) не определено.
Высокая активность комплемента сопровождается возрастанием числа мембраноатакующих комплексов и опосредует клиническую манифестацию в виде органных дисфункций (в первую очередь сердечной и почечной недостаточности). Реализация эффекторных цитолитических механизмов зависит от образования субъединиц C5a и последующего каскада C5B -9 компонентов комплемента [5], что приводит к образованию терминального комплекса нарушениям клеточной стенки.
Нами было определено, что у пациентов группы СВО с ПОН, имеющих на всем протяжении периоперационного периода высокую активность комплемента, уровни С5а субъединицы были самыми высокими (рис. 2).
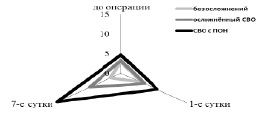
Рис. 2. Диаграмма динамики С5а субъединицы компонента комплемента в периоперационном периоде пациентов с инфекционным эндокардитом
Несмотря на отсутствие разницы в уровнях активности путей комплемента, ещё до операции сывороточные концентрации С5а субъединицы компонента комплемента у пациентов группы СВО с ПОН (4,46 (3,78; 6,02) пг/мл) были выше (0,004), чем таковые пациентов группы без осложнений (2,93 (2,43;4,35) пг/мл), но не отличались от уровней пациентов группы осложнённого СВО (3,23 (1,77; 5,84) пг/мл), что свидетельствует о большей степени активности комплемента у пациентов группы СВО с ПОН в период начала основного заболевания, до момента проведения консервативной терапии по стабилизации инфекционного процесса. В последующем, параллельно с инициализацией комплемента, происходит увеличение количества и С5а субъединицы в сыворотке крови. Наиболее выраженное увеличение его концентраций определено у пациентов группы СВО с ПОН. В 1-е сутки количество С5а у этих пациентов увеличилось до 8,23 (6,04; 9,56) пг/мл, р = 0,001). На на 7-е сутки у пациентов этой группы отмечается потеря контроля над регуляцией активности комплемента, что отражается в значимом (р = 0,001) дополнительном увеличении сывороточного уровня С5а субъединицы (14,56 (12,03; 17,97) пг/мл). Так как высокие концентрации С5а субъединицы комплемента связаны с повреждением клеточных стенок различных тканей, то и подтверждается его участие в формировании органной недостаточности в результате ишемического и реперфузионного повреждения после операций в условиях искусственного кровообращения. Похожая динамика описана для критических состояний [14], но связана с сепсисом.
Аналогичная предыдущей динамика С5а субъединицы комплемента у пациентов группы с осложнённым СВО связана с увеличением концентраций в послеоперационном периоде (рис. 2). Однако его уровни на всем протяжении наблюдения ниже (5,26 (3,1; 7,08) пг/мл, р = 0,007 в 1-е сутки и 7,24 (4,79; 8,77) пг/мл, р < 0,001), чем у пациентов группы СВО с ПОН. Менее выраженная интенсивность клеточных повреждений, связанных с анафилатоксическим действием С5а субъединицы комплемента, может отражаться в обратимости тканевых деструктивных процессов и абортивности органной недостаточности.
В противовес имеющимся у пациентов с осложнениями СВО увеличениям количества сывороточных С5а субъединиц комплемента, у пациентов без осложнений СВО в послеоперационном периоде наблюдается иная динамика (рис. 2). В соответствии с усилением активности комплемента в 1-е сутки у пациентов этой группы увеличивается и количество сывороточного С5а (4,56 (3,73; 5,87) пг/мл, р = 0,003), но его концентрации ниже чем у пациентов группы СВО с ПОН (р = 0,001). На 7-е сутки концентрации С5а субъединицы возвращаются к исходным (2,35 (1,56; 3,39) пг/мл, р = 0,07), и его количество в это время ниже чем у пациентов как группы с осложнённым СВО (р < 0,001), так и группы СВО с ПОН (р < 0,001). Как и умеренная активация комплемента, динамика С5а субъединицы комплемента у пациентов группы без осложнений СВО свидетельствует о регулируемом системном воспалении, направленном в послеоперационном периоде на восстановление гомеостаза и элиминации экзо- и аутотоксинов.
Выводы
Наибольшее значение в формировании системного воспалительного ответа после протезирования клапанов сердца у пациентов с инфекционным эндокардитом в раннем послеоперационном периоде имеет активность классического пути комплемента. Альтернативный путь имеет значение при развитии осложнений в позднем послеоперационном периоде. Параллельно, в развитии осложнений системного воспалительного ответа вносит С5а субъединица комплемента. Его высокие дооперационные концентрации связаны с увеличением риска развития полиорганной недостаточности.
Рецензенты:
Лисаченко Г.В., д.м.н., профессор, заведующий кафедрой патологической физиологии, ГОУ ВПО «Кемеровская государственная медицинская академия» Минздрава Российской Федерации, г. Кемерово;
Будаев А.В., д.м.н., профессор кафедрой патологической физиологии, ГОУ ВПО «Кемеровская государственная медицинская академия» Минздрава Российской Федерации, г. Кемерово.
Работа поступила в редакцию 05.08.2014.
Библиографическая ссылка
Понасенко А.В., Головкин А.С., Григорьев Е.В. ЗНАЧЕНИЕ СИСТЕМЫ КОМПЛЕМЕНТА И С5А СУБЪЕДИНИЦЫ ПРИ ФОРМИРОВАНИИ СИСТЕМНОГО ВОСПАЛИТЕЛЬНОГО ОТВЕТА В ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ ПРОТЕЗИРОВАНИЯ КЛАПАНОВ СЕРДЦА ПАЦИЕНТОВ С ИНФЕКЦИОННЫМ ЭНДОКАРДИТОМ // Фундаментальные исследования. 2014. № 10-1. С. 141-146;URL: https://fundamental-research.ru/en/article/view?id=35230 (дата обращения: 27.04.2026).



