Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
COMPARATIVE RESEARCH OF ENTEROPROTECTIVE ACTION OF DEANOL ACEGLUMATE AND ETOXYDOL AGAINST THE BACKGROUND OF INTRODUCTION OF INDOMETACIN AND DICLOFENAC
Энтеропатия, индуцированная введением нестероидных противовоспалительных средств (НПВС-энтеропатия), встречается чаще, чем НПВС-гастропатия, хотя диагностика ее затруднительна [4,7]. Серьезные осложнения НПВС-индуциро-ванной энтеропатии могут включать массивное кровотечение, перфорацию и стриктуры, иногда приводящие к смерти [4,5,8]. Кроме того, в настоящее время нет разработанных методов лечения НПВС – индуцированной энтеропатии с обоснованной эффективностью [9,10]. Доказано, что ингибиторы протонной помпы уменьшают тяжесть повреждения и кровотечения в желудке и двенадцатиперстной кишке, где важна роль соляной кислоты в процессе язвообразования [11,12]. Однако отсутствуют доказательства о снижении тяжести НПВС-индуцированной энтеропатии под влиянием каких-либо антисекреторных препаратов [6]. В связи с вышеуказанными данными особенно актуальным является изучение энтеропротеторного эффекта у отечественных препаратов антиоксидантного действия [1,2].
Целью работы явилось сравнение энтеропротекторного эффекта отечественных лекарственных препаратов антиокисдантного действия – деанола ацеглумата и этоксидола – в условиях моделирования язвенного поражения желудочно-кишечного тракта введением индометацина и диклофенака.
Материалы и методы исследования
В работе исследовалось энтеропротекторное действие этоксидола (2-этил-6-метил-3-гидроксипири-дина гидроксибутандиоат), созданного на базе Всероссийского научного центра по безопасности биологически активных веществ (ВНЦ БАВ) (Старая Купавна, Россия) (директор Н.М.Митрохин) под руководством заведующей отделом химии и технологии лекарственных средств, лауреата Государственной премии РФ, доктора химических наук, профессора С.Я. Скачиловой. В качестве препарата сравнения выбран деанола ацеглумата (N-ацетил-L-глютамат 2 (диметиламино) этанола) с доказанным ранее энтеропротекторным действием в условиях индукции эрозивно-язвенного поражения желудочно-кишечного тракта нестероидными противовоспалительными препаратами [2], также созданный на базе ВНЦ БАВ.
Экспериментальные исследования выполнены на 60 белых нелинейных крысах-самцах весом 220-280гр., содержащихся в стандартных условиях вивария Медицинского института ФГБОУ ВПО «МГУ им. Н.П.Огарева», в соответствии со статьей 11 Хельсинской декларации Всемирной медицинской ассоциации (1964г.), «Международными рекомендациями по проведению медико-биологических исследований с использованием животных» (1985г.) и «Правилами лабораторной практики в Российской Федерации» (приказ МЗ и СР РФ № 708н от 23.08.2010 г.).
В первом разделе экспериментов в качестве модели язвообразования использовали 5-дневное введение индометацина в дозе 10 мг/кг внутрижелудочно зондовым способом после двух часов без пищи и воды. Контрольную группу составили 10 животных. Летальность в контрольной группе составила 20%. Животным опытной группы (п=8) в течение 5 суток эксперимента вводили внутрижелудочно зондовым способом этоксидол в дозе 25 мг/кг один раз в день. Животным группы сравнения (п=8) вводили деанола ацеглумат в условно изотоксической дозе 250 мг/кг через 30 минут после введения индометацина. Оценку результатов проводили на 11 сутки эксперимента. В опытных группах летальность отсутствовала.
Во втором разделе экспериментов животным опытной группы вводили этоксидол в дозе 25 мг/кг внутримышечно в течение 5 суток (п=12), животным группы сравнения вводили внутримышечно деанола ацеглумат в дозе 250 мг/кг в течение 5 суток. Язвенное поражение желудочно-кишечного тракта воспроизводили путем внутримышечного введения диклофенака в дозе 50 мг/кг на 5 и 6 сутки эксперимента. Животные контрольной группы (п=12) не получали какой-либо профилактической фармакологической коррекции. Оценка результатов проводилась на 7 сутки эксперимента.
Все манипуляции с причинением боли проводились под общим обезболиванием в виде внутрибрюшинного введения тиопентала натрия в дозе 50 мг/кг. Выведение животных из опыта осуществлялось после исчезновения роговичного рефлекса гильотинным способом. Кишечник вскрывался на всем протяжении. Визуально оценивалось язвенное поражение слизистой оболочки тонкой и толстой кишки по методике Н.Е. Чернеховской с соавт., (2006) [3]. Проводили оценку количества язв, общей площади язвенного поражения, рассчитывали количество и площадь язв на 1 см длины тонкой кишки, оценивали количество и площадь язв с гемосидерином, количество и площадь прободных язв. Сравнивали долю животных с признаками кровотечения, долю животных с наличием прободных язв, летальность животных в группах.
Полученные данные обрабатывались методами вариационной статистики с использованием программ StatPlus 2009 Professional. Вычисляли среднее арифметическое (М) и среднюю квадратическую ошибку (m), представляя данные в виде M±m. Для оценки значимости различий двух выборок применяли параметрический (t-критерий Стьюдента) и непараметрические (χ2, Фишера) критерии. Различия считались достоверными при уровне значимости р<0,05.
Результаты и их обсуждение
Введение индометацина привело к выраженному язвообразованию в слизистой оболочке тонкой и толстой кишки. У всех животных контрольной группы регистрировались прободные язвы, признаки кровотечения из язв тонкой и толстой кишки. На фоне введения индометацина наблюдалась гибель 20 % животных.
В серии сравнения введение деанола ацеглумата в изученной дозе привело к сокращению количества язв в тонкой кишке на 85 % (с 1,55±0,142 до 0,234±0,150 язв/см, р<0,05). При этом площадь язвенного поражения тонкой кишки сократилась на 66 % (с 1,788±0,208 мм2/см до 0,599±0,056 мм2/см, р<0,05).
В серии с применением деанола ацеглумата не регистрировалось язв с гемосидерином (χ2=3,961, р=0,047, по критерюй Фишера р=0,022). Доля животных с прободными язвами уменьшилась со 100% до 57 % (р>0,05). Количество прободных язв сократилось на 95 % (с 25,75±2,48 до 1,286±0,567, р<0,001) на 1 животное, а площадь – на 94 % (с 54,11±5,18 до 3,31±1,21 мм2, р<0,001). В толстой кишке введение деанола ацеглумата уменьшило количество язв на 54 % (с 22,5±1,35 до 10,38±1,59, р<0,05), а их площадь – на 69,4 % (со 157,89±18,91 до 48,28±4,88 мм2, р<0,01).
Этоксидол при внутрижелудочном введении в дозе 25 мг/кг также оказал выраженное энтеропротекторное действие. Препарат уменьшал количество язв в тонкой кишке на 80 % (до 0,315±0,065 язв/см, р<0,001). Площадь язвенного поражения тонкой кишки сокращалась на 73 % (до 0,479±0,116 мм2/см, р<0,001). У всех животных опытной группы предотвращалось развитие кровотечения (χ2=3,961, р=0,047, по критерию Фишера р=0,022).
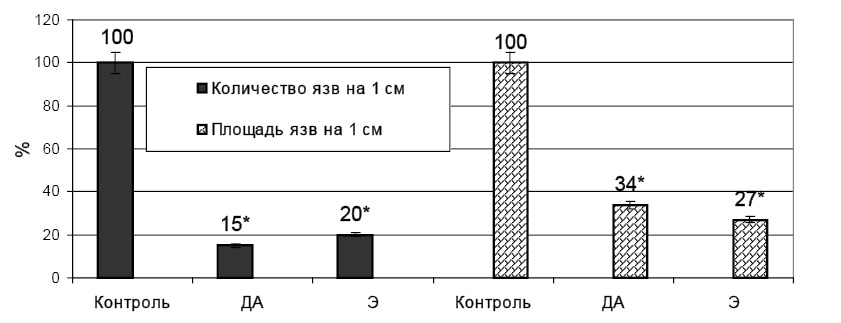
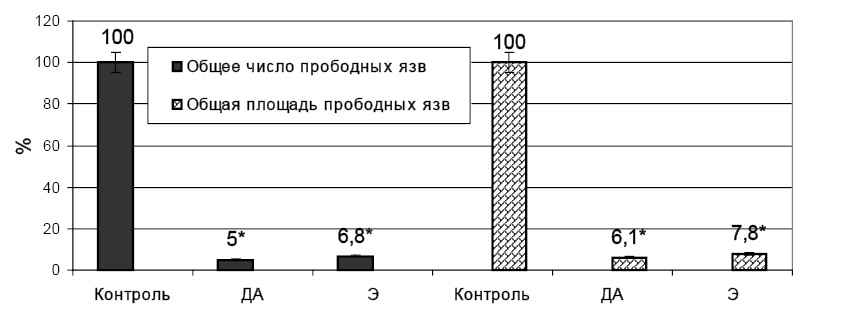
Рис. 1. Влияние деанола ацеглумата (250 мг/кг) и этоксидола (25 мг/кг) при внутрижелудочном введении зондовым способом на процессы язвообразования в тонкой кишке, индуцированные введением индометацина 10 мг/кг (в % к данным контроля); * – достоверность различия р<0,05 по отношению к данным контрольной группы
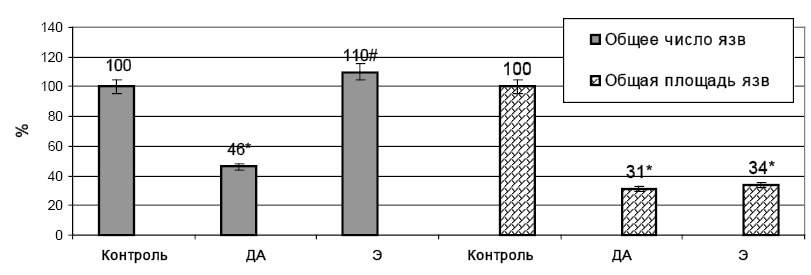
Рис. 2. Влияние деанола ацеглумата (250 мг/кг) и этоксидола (25 мг/кг) при внутрижелудочном введении зондовым способом на процессы язвообразования в толстой кишке, индуцированные введением индометацина 10 мг/кг (в % к данным контроля); * – достоверность различия р<0,05 по отношению к данным контрольной группы, # – к данным группы сравнения
Количество прободных язв уменьшилось на 93,2 % (до 1,75±1,08, р<0,05), площадь – на 92,2 % (р<0,01). Доля животных с прободными язвами уменьшилась до 50 % (χ2=0,246, р=0,620). В толстой кишке введение этоксидола не повлияло на количество язв (24,75±5,93, р>0,05), но площадь язвенного поражения уменьшилась на 66 % (54,04±11,38 мм2, р<0,05).
Во втором разделе экспериментов в контрольной группе на фоне введения диклофенака летальность животных составила 25 %. Процессы язвообразования в кишечнике, признаки кровотечения и развитие прободных язв наблюдалось у всех животных контрольной серии. Количество язв составило на 1 см длины тонкой кишки – 1,357±0,136 язв/см. Площадь язвенного поражения достигла 7,307±1,386 мм2/см. Кол-во прободных язв составило 8,25±0,881 в среднем на 1 животное в группе, по площади – 22,91±3,06 мм2. Количество язв с гемосидерином составило 40±6,84. Их площадь достигла 71 % от общей площади язвенного поражения (318,8±95,53 мм2). В толстой кишке количество язв достигало 29,25±2,23 на 1 животное, площадь их составила 320,19±26,69 мм2. У 5 из 8 животных наблюдались признаки кровотечения из язв толстой кишки.
В группе сравнения на фоне внутримышечного введения деанола ацеглумата количество язв в тонкой кишке уменьшалось на 48 % (до 0,704±0,086 язв/см, р<0,05). Площадь язв в тонкой кишке также сокращалась на 83 % (до 1,220±0,123 мм2/см, р<0,001). У 3 животных из 12 наблюдалось образование прободных язв, однако их среднее количество уменьшилось на 97% (р<0,001), а площадь – на 96 % (р<0,001). У 10 из 12 животных в группе регистрировались признаки кровотечения. По сравнению с контрольной серией количество язв с гемосидерином в тонкой кишке уменьшилось на 73 % (р<0,05), а площадь – на 91 % (р<0,001). В толстой кишке количество язв на фоне предварительного введения деанола ацеглумата не снижалось, но площадь уменьшалась на 46 % (до 171,56±8,59 мм2, р<0,05). Количество язв с тромбом также сократилось на 32 % (с 19,00±2,31 до 13,00± 2,59), а их площадь – на 68 % ( с 292,0±27,9 мм2 до 93,63±19,96 мм2).
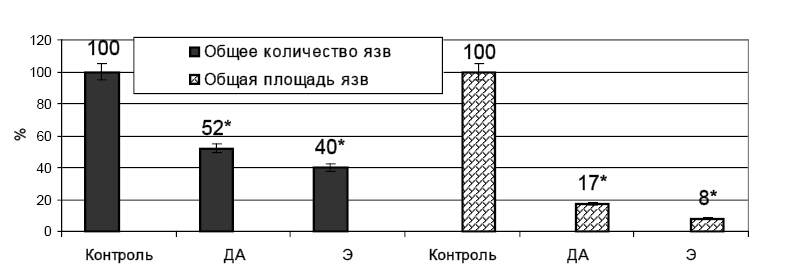
Рис. 3. Влияние деанола ацеглумата (250 мг/кг) и этоксидола (25 мг/кг) при внутримышечном введении на процессы язвообразования в тонкой кишке, индуцированные введением диклофенака 50 мг/кг в/м (в % к данным контроля); ДА – деанола ацеглумат; Э – этоксидол; * – достоверность различия р<0,05 по отношению к данным контрольной группы
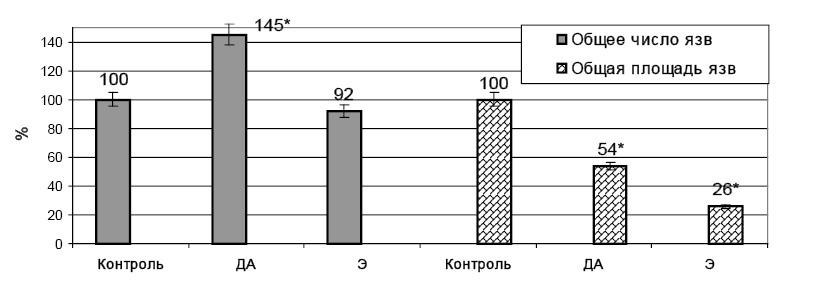
Рис. 4. Влияние деанола ацеглумата (250 мг/кг) и этоксидола (25 мг/кг) при внутримышечном введении на процессы язвообразования в толстой кишке, индуцированные введением диклофенака 50 мг/кг в/м (в % к данным контроля); ДА – деанола ацеглумат; Э – этоксидол; * – достоверность различия р<0,05 по отношению к данным контрольной группы
В опытной группе на фоне предварительного внутримышечного введения этоксидола в дозе 25мг/кг наблюдалось снижение общего количества язв в тонкой кишке на 60 % (до 0,537±0,125 язв/см, р<0,05) и площади язвенного поражения – на 92 % (до 0,577±0,142 мм2/см, р<0,001). В толстой кишке у животных опытной группы количество язв составило 92 % от показателя контроля, площадь язвенного поражения уменьшалась на 74 % (р<0,001). У всех животных полностью предотвращалось развитие кишечных кровотечений и прободных язв (r=6,129, р=0,013 по χ2, по критерию Фишера р=0,008).
Заключение
Таким образом, полученные результаты подтверждают достоверное энтеропротекторное действие деанола ацеглумата и этоксидола в условиях введения нестероидных противовоспалительных препаратов. Причем, при внутрижелудочном введении на модели индометацинового повреждения желудочно-кишечного тракта у изученных препаратов наблюдается одинаковый противоязвенный эффект в тонкой кишке, но в толстой кишке деанола ацеглумат оказывает более выраженное противоязвенное действие. При профилактическом внутримышечном введении препаратов в изученных дозах во 2-й модели энтеропротекторный эффект этоксидола более выражен, чем у деанола ацеглумата. Так, площадь язвенного поражения в тонкой кишке в группе животных, получавших этоксидол в/м, на 53% меньше. Кроме того, в отличие от серии с в/м введением деанола ацеглумата, полностью предотвращается развитие кровотечения и прободных язв.
Рецензенты:
Инчина В.И., д.м.н., профессор, заведующий кафедрой фармакологии Медицинского института ФГБОУ ВПО «Мордовский государственный университет имени Н.П. Огарева», г. Саранск;
Лещанкина Н.Ю., д.м.н., профессор, заведующий кафедрой госпитальной терапии Медицинского института ФГБОУ ВПО «Мордовский государственный университет имени Н.П.Огарева», г. Саранск.
Работа поступила в редакцию 24.06.2014.
Библиографическая ссылка
Зорькин М.В, Аткарская О.А, Зорькина А.В СРАВНИТЕЛЬНОЕ ИССЛЕДОВАНИЕ ЭНТЕРОПРОТЕКТОРНОГО ДЕЙСТВИЯ ДЕАНОЛА АЦЕГЛУМАТА И ЭТОКСИДОЛА НА ФОНЕ ВВЕДЕНИЯ ИНДОМЕТАЦИНА И ДИКЛОФЕНАКА // Фундаментальные исследования. 2014. № 7-4. С. 706-710;URL: https://fundamental-research.ru/en/article/view?id=34965 (дата обращения: 10.06.2026).



