Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
NEURAL NETWORK-BASED PATHOLOGY PREDICTION IN PERINATAL CENTER
Для решения задач автоматизации деятельности лечебно-профилактических учреждений (ЛПУ) в последнее время разрабатывается достаточно большое количество медицинских информационных систем (МИС) различного назначения. Актуальным направлением и особенностью настоящего этапа развития МИС является создание систем поддержки принятия решений (СППР), которые обеспечивают интеллектуальную поддержку врача при выполнении основных функций, связанных с прогнозированием, диагностикой заболеваний и выбором оптимальной тактики их коррекции. Решение подобных задач может быть обеспечено путём разработки СППР, функционирующих автономно либо интегрированных в МИС. Разработка СППР является наиболее сложной задачей при создании МИС, учитывая чрезвычайную сложность человеческого организма, неоднозначность и нечёткость представления медицинской информации, сложность формализации медицинских знаний и процедур принятия врачебных решений, отнесение медицинских задач к слабоструктурированным или неструктурированным проблемам. В этой связи при создании СППР немаловажная роль отводится медицинским экспертным системам (ЭС), позволяющим оценивать состояние пациента путём сравнения со стандартными ситуациями и обеспечивать помощь в постановке диагноза, используя накопленный опыт практикующих врачей и ведущих учёных в данной предметной области (экспертов). Подход к созданию медицинских СППР, в т. ч. на базе экспертных систем, рассмотрен в многочисленной литературе, посвящённой данной проблематике, в частности, в [1 – 4].
В настоящей работе рассматривается подход к разработке СППР как составной части АСУ лечебно-диагностическим процессом (ЛДП), создаваемой для узкоспециализированных ЛПУ – перинатальных центров (ПЦ), на примере ГБУЗ ТО «Перинатальный центр» (г. Тюмень). Результаты отдельных этапов исследований приведены в [5, 6].
Целью исследований на данном этапе являлся анализ методов и моделей представления данных при разработке медицинских систем поддержки принятия решений и обоснованный выбор модели для прогнозирования вероятности развития патологий беременности. Задача, решаемая в ходе данной работы, состоит в поиске действенного метода представления медицинской информации при прогнозировании заболеваний пациентов ПЦ с учётом наиболее распространённых в Тюменской области патологий.
Материалы и методы исследований
В ходе работы в качестве основного метода исследования использовался метод экспертных оценок как наиболее приемлемый с учётом сложности формализации методов интерпретации данных при прогнозировании патологий. Кроме того, решение многих задач диагностирования и классификации возможно исключительно на основе опыта экспертов.
Путём информационного поиска в качестве базовой модели медицинской экспертной СППР выбрана нейронная сеть, проектируемая по принципу многослойного персептрона. С реализационной точки зрения нейросетевая модель разрабатывается на базе языка программирования JavaScript и фреймворка Node.JS, что позволяет интегрировать её в состав разрабатываемой на базе JavaScript АСУ ЛДП перинатального центра.
Результаты исследований и их обсуждение
Основываясь на анализе литературы, для обеспечения интеллектуальной поддержки врача в перинатальном центре в настоящей работе выбраны экспертные системы, в основе которых лежит анализ уже накопленной медицинской информации. При этом ЭС интегрирована в состав АСУ ЛДП перинатального центра, которая разбита на две составляющие – информационно-аналитическая система (ИАС) и экспертная СППР. Общая принципиальная схема разрабатываемой системы приведена на рис. 1.
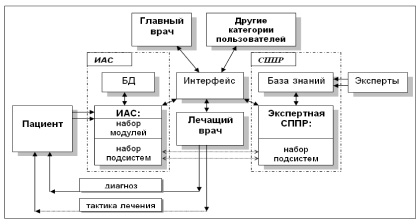
Рис. 1. Общая структура АСУ ЛДП с поддержкой принятия решений
Взаимодействие врача с пациентом осуществляется посредством ИАС с собственной базой данных (БД), с использованием данных, предоставляемых СППР с собственной базой знаний. При проектировании ЭС были выделены следующие ключевые её подсистемы: постановки диагноза; оценки риска; определения вариантов лечения. Подсистемы ЭС взаимодействуют с её базой знаний и используются в ИАС – подсистемами диагностики и назначения лечения.
Для реализации основных функций ЭС можно использовать различные модели представления знаний, основанные на эмпирическом и теоретическом подходах [4, 7], с применением разнообразных направлений и методов обработки данных. Задача при этом заключается в формализации способа представления медицинских данных и знаний при разработке моделей диагностики и принятия решений.
Для выбора метода представления данных при решении поставленных в работе задач были проанализированы следующие подходы: продукционная модель представления знаний, решающее дерево (дерево решений) и нейросетевая модель, достаточно часто используемые в медицинских системах.
Продукционные модели наиболее просты. Их целесообразно использовать при диагностике заболеваний (в частности, патологий беременности), когда исходные данные можно интерпретировать однозначно. При этом довольно просто построить модель из правил-продукций вида Rel = {if (условие) then (заключение)}. Но в условиях невозможности формализации знаний и вероятной неполноты исходных данных попытка создания продукционной модели привела к появлению бесконечной череды правил, чрезмерно усложняющих модель без возможности последующего самообучения и самокоррекции.
Дерево решений используется в области статистики и анализа данных для прогнозных моделей. Для классификации новой полученной информации необходимо спуститься по дереву решений до результирующего листа, чтобы получить соответствующее значение. Этот подход широко используются в интеллектуальном анализе данных. Попытка построить такое решающее дерево в рамках настоящей работы не была успешной, так как при прогнозировании невозможно выстроить чёткий порядок анализа информации. К тому же этот подход не имеет методов решения задач с зашумлёнными или неполными входными данными.
Среди экспертных медицинских систем особое место занимают самообучающиеся интеллектуальные системы – искусственные нейронные сети, являющиеся одним из основных инструментов поддержки принятия решений в условиях отсутствия точных моделей реальных процессов и явлений. В приложении к медицинской диагностике они обеспечивают повышение специфичности метода, быстроты и точности постановки диагноза, параллельный учет множества различных факторов, характеризующих состояние больного (в т. ч. и не поддающихся формализации), повышенную гибкость при решении задач, связанных с неполными, зашумлёнными, искажёнными данными [7, 8]. Несомненные преимущества нейросетевых моделей и определили выбор их в качестве метода обработки информации в настоящей работе.
Предлагаемый в работе метод прогнозирования патологий на самом деле не относится к общепринятым методам прогнозирования на базе нейросети, которые направлены в основном на прогнозирование тренда и предугадывание одного или нескольких последующих значений на основе ранее накопленного опыта. В рассматриваемом случае – при прогнозировании патологий беременности – решаются, по сути задачи классификации, то есть, отнесение данного пациента к определённой группе риска с какой-либо долей вероятности на основе входного вектора данных о пациенте. При этом решаются задачи построения решающего правила для отнесения i-го объекта (i = 1…m) – пациента с определенным набором признаков j (j = 1...n) – к одному из имеющихся классов yi (i =1...k) – диагнозов. В решении подобного рода задач прекрасно показали себя многослойные нейронные сети, используемые, в частности, для решения задач прогнозирования, когда экспертная оценка уже содержится в исходных данных и может быть выделена при их обработке.
Независимо от того, как выбирается архитектура сети, знания о предметной области выделяются нейронной сетью в процессе обучения. Эти знания представляются в компактно распределенном виде весов синаптических связей сети, что позволяет нейросети адаптироваться и выполнять обобщение [8].
При выборе функции активации проанализированы функции класса сигмоид – функция Ферми, рациональная сигмоида, гиперболический тангенс, логистическая функция. Последняя (рис. 2) выбрана в настоящей работе в связи с простотой расчётов как самой функции, так и её производной (f`(x) = x(1–x)), используемой в механизме обратного распространения ошибки для корректировки весов сети.
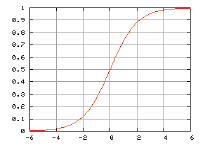
Рис. 2. График логистической функции вида 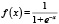
С реализационной точки зрения нейросеть в работе проектируется на базе языка программирования JavaScript и фреймворка Node.JS, что обеспечивает полную её совместимость с разрабатываемой для перинатального центра АСУ ЛДП. Реализация такого подхода является узконаправленной, т. к. возможности специализированных математических пакетов MATHLAB и STATISTICA позволяют более легко выполнить подобную задачу классификации, но эти пакеты не могут быть интегрированы в МИС для выдачи врачу информации о прогнозах в режиме реального времени. Интегрированная в АСУ ЛДП нейросеть позволит создать информационно-советующую подсистему, способную на основе всей имеющейся в системе информации о пациенте выдавать релевантные сведения о прогнозах относительно вероятности развития патологий. Полученные в результате работы нейросети значения выходного слоя могут быть переданы в систему для дальнейшей обработки и визуального представления. Интеграция с нейросетью для выбора тактики лечения пациента позволит автоматизировать процесс подбора индивидуальной терапии с учётом диагнозов, анамнеза, риска возникновения осложнений, личных или групповых противопоказаний. Такая советующая подсистема может выдавать врачу как комплексную подсказку в виде готовой терапии, так и анализировать его действия и предлагать корректировки.
Рассмотрим реализацию нейронной сети, построенной по принципу многослойного персептрона. В состав тестовой сети входит входной слой из 4-х нейронов, скрытый слой из 3-х нейронов, а также выходной слой из 4-х нейронов (рис. 3). Для обучения сети были применены синтетические данные.
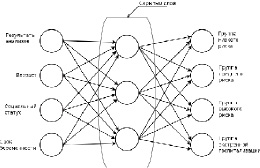
Рис. 3. Общий вид нейронной сети
После многократного повторения обучения на тестовых наборах значений сеть получила способность на 100 % точно классифицировать обучающие примеры, а также принимать корректные решения на наборах данных, не вошедших в обучающую выборку. График изменения ошибки в процессе обучения (рис. 4) показывает, что сеть обучается успешно, постепенно снижая вероятность ошибки, и в конечном итоге сводит ошибку до 0.
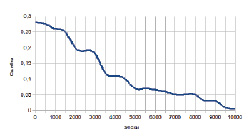
Рис. 4. График изменения ошибки
На данном этапе нейросеть позволит МИС автоматически определять вероятные «группы риска» для пациентов на основе анализа их данных. Это не освобождает врача от задач по проверке групп риска пациентов, но может заметно облегчить его работу.
Наиболее сложным и ёмким этапом построение нейронной сети является сбор и подготовка данных для обучения, которые должны быть преобразованы к виду, пригодному для подачи на входы сети. Для использования нейросети применительно к решению поставленных в работе задач ранее были выявлены значимые для региона патологии – заболевания щитовидной железы [6]. Также были определены наиболее информативные методы их диагностики, граничные значения диагностируемых показателей и критерии диагностики, методы и схемы лечения и факторы, оказывающие влияние на выбор оптимальной тактики коррекции заболевания, что может быть использовано для формирования обучающей выборки.
Заключение
- Выполнен анализ методов и моделей представления данных при разработке медицинских систем поддержки принятия решений и обоснован выбор нейросетевой модели для прогнозирования вероятности развития патологий беременности.
- Выполнена реализация нейросети, построенной по принципу многослойного персептрона, на языке JavaScript, приведены результаты её обучения, показавшие потенциальную возможность её использования при решения задач определения групп риска пациентов в перинатальном центре.
- Предложена структура АСУ ЛДП для перинатального центра с экспертной системой поддержки принятия решений.
Рецензенты:
Борзых В.Э., д.ф-м.н., профессор, заведующий кафедрой автоматизации и вычислительной техники ФГБОУ ВПО «Тюменский государственный нефтегазовый университет», г. Тюмень;
Ивашко А.Г., д.т.н., профессор, директор Института математики и компьютерных наук, проректор по информационным технологиям ФГБОУ ВПО «Тюменский государственный университет», г. Тюмень.
Работа поступила в редакцию 04.06.2014.
Библиографическая ссылка
Таранов Ю.А. ПРОГНОЗИРОВАНИЕ ПАТОЛОГИЙ В ПЕРИНАТАЛЬНОМ ЦЕНТРЕ НА ОСНОВЕ НЕЙРОННОЙ СЕТИ // Фундаментальные исследования. 2014. № 9-1. С. 50-54;URL: https://fundamental-research.ru/en/article/view?id=34640 (дата обращения: 17.05.2026).



