Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
CARDIOMETABOLIC FORMING PATTERN OF ISCHEMIC EVENT RISK IN PATIENTS WITH DIABETES MELLITUS TYPE II: APPEARANCE AT KEY METABOLIC FACTORS
В развитие кардиоваскулярных событий у пациентов с СД 2 т существенный вклад вносит каскад метаболических и сосудистых нарушений, в основе которых лежат ИР, компенсаторная гиперинсулинемия, оксидативный стресс, ДЭ, АГ и воспаление, которые также рассматриваются в качестве независимых факторов кардиоваскулярного риска [1, 7, 8]. Одними из основных сердечно-сосудистых исходов являются ишемические события. С целью изучения влияния множественных факторов риска на оценку сердечно-сосудистого прогноза используются таблицы, шкалы, индексы, основанные на анализе традиционных модифицированных факторов риска, таких как АГ, гиперхолестеринемия (ГХС), курение, так и дополнительных: абдоминальное ожирение, алкоголь, стресс/депрессия, гиподинамия, нарушение углеводного обмена, низкий социальный и образовательный статус, а также немодифицируемых: пол, возраст, наследственный анамнез по сердечно-сосудистой патологии параметров [2, 6, 10]. Традиционной моделью, используемой в России и в европейских странах с целью оценки риска ишемических событий для пациентов с СД 2 т, является шкала PROCAM. Однако шкала PROCAM имеет ряд ограничений в объективизации оценки, влияющих на ишемический прогноз [4, 5, 9]. К таким ограничениям относятся биполярная оценка нарушений углеводного обмена (наличие либо отсутствие СД), без таких значимых прогностических показателей, как уровни гликемии натощак (ГН), постпрандиальной гликемии (ППГ), НвА1с, индекс инсулинорезистентности (НОМА), а также их динамика в процессе терапии. Отсутствуют такие высокоинформативные параметры, как С-реактивный белок (СРБ), масса тела (МТ), индекс массы тела (ИМТ), объем талии (ОТ). В современных подходах к стратификации риска сердечно-сосудистого риска заболеваний выделены высоко информативные критерии прогноза, такие как ТКИМ/ОСА, ЭАМ, а также общепринятые параметры ДЭ: NO, эндотелийзависимой вазодилатации (ЭЗВД), во многих исследованиях также отмечена весомая роль ПОЛ-АОС [3].
В связи с чем целью исследования являлась оценка вклада ключевых показателей, формирующих метаболические и сосудистые нарушения, на риск ишемических событий у пациентов с СД 2 т.
Материалы и методы исследования
Обследовано 90 пациентов с СД 2 т, в том числе 22 (24 %) – мужчин и 68 (76 %) – женщин, за период с 2006 по 2008 гг., диагноз сахарный диабет 2 типа был верифицирован согласно диагностическим критериям сахарного диабета и других нарушений углеводного обмена (ВОЗ, 1999 г). Из 90 пациентов 22 (24 %) пациента было включено в исследование с впервые выявленным СД 2 т. Диагноз артериальной гипертензии был верифицирован у 88 пациентов согласно рекомендациям ВОЗ 1999 г. Продолжительность АГ у пациентов от 3 мес. до 46 лет. В изучаемой группе 13 (14,4 %) пациентов курили. Средний возраст пациентов составлял 54,97 ± 0,65 лет, стаж СД 2 т 1,53 ± 0,21 лет.
Изучались параметры состояния липидного обмена: общий холестерин (ОХС), ТГ, липопротеиды низкой плотности (ЛПНП), липопротеиды высокой плотности (ЛПВП), ИА; углеводного обмена: ГН, НвА1с, иммуннореактивный инсулин (ИРИ); инсулинорезистентности: индекс НОМА-IR; ПОЛ в абсолютных значениях и единицах индекса окисления: общие полиеновые (ОП,Е220) гептановая / изопропанольная фазы (гпт/изп.фф.), диеновые конъюгаты гидроперекисей (ДК,Е232 гпт./изп.фф.), кетодиенов с сопряженными триеновыми (КДсСТ,Е278 гпт./изп.фф.), оснований Шиффа (ОШ,Е400 гпт./изп.фф.), малонового альдегида (МДА); АОС: каталаза эритроцитов и сыворотки, мочевая кислота (МК); нитроксидэргического статуса: NO, нитраты (NO3), нитриты (NO2); комплексной оценки функции эндотелия: эндотелийзависимая и эндотелийнезависимая дилатация (ЭЗВД-30», -60», -90», ЭНВД), ТКИМ/ОСА, ЭАМ; гемодинамические: САД, диастолическое артериальное давление (ДАД); маркера воспаления: СРБ, и антропометрические параметры: ИМТ, МТ, ОТ, отношение объема талии к объему бедер (ОТ/ОБ) у наблюдаемых пациентов. Риск ишемических событий оценивался в соответствии со шкалой PROCAM. Критериями включения в исследование были: СД 2 типа у пациентов в возрасте от 18 до 65 лет, с индексом массы тела 25,0–39,9 кг/м², без инсулинотерапии; согласие пациента и подписание пациентом информированного согласия на участие в исследовании. Критериями исключения были: СД 1 типа и СД 2 типа, инсулинопотребный у пациентов, наличие у пациентов с СД 2 т документированных острых и хронических церебро- и кардиоваскулярных нарушений; состояние кетоацидоза на момент исследования и в предыдущие 6 месяцев. Обработка данных выполнялась с использованием программ Statistica, статистического пакета SPSS, с проведением факторного, регрессионного, корреляционного анализа и методов вариационной статистики. Представлены связи с уровнем достоверности р < 0,05. Результаты исследования представлены в виде: М ± δ, ДИ.
Результаты исследования и их обсуждение
Исходное значение риска ишемических событий по шкале PROCAM у пациентов с СД 2 т составило 14,25 ± 15,74 балла, ДИ 10,95–17,54, находилось в диапазоне умеренного риска (до 20 баллов). В том числе у 70 (77,8 %) пациентов риск ишемических событий по PROCAM менее 20 баллов и у 20 (22,2 %) более 20 баллов (22,2 %), что, возможно, объясняется наличием целевых уровней САД у 53,3 %, ЛПВП у 38,9 %, ТГ у 54,4 % пациентов и подавляющим количеством некурящих пациентов (86 %) в группе. При этом в группе с умеренным риском выявлено бессимптомное поражение органов-мишеней: увеличение ТКИМ/ОСА у 74,29 %, наличие атеросклеротических бляшек (АСБ) у 34,29 % и повышение ЭАМ у 48,57 % пациентов, из них отмечено увеличение ТКИМ/ОСА и ЭАМ у 21,43 %, увеличение ТКИМ/ОСА и наличие АСБ у 35,71 %, увеличение ЭАМ и наличие АСБ у 18,57 % пациентов, наличие всех 3 отягощающих факторов у 12,85 % пациентов.
При проведении факторного анализа были выявлены 16 независимых переменных, из которых характеризуют функцию эндотелия: ЭЗВД-30», ЭЗВД-60», ЭНВД, САД; ПОЛ: Е278гпт.ф., Е232/220изп., Е278/220изп.фф., МДА; АОС: МК; липидный статус: ЛНПН, ИА; нитроксидэргический баланс: NO, NO3; структурную характеристику сосудистой стенки: ТКИМ/ЛОСА; антропометрические данные: МТ, ИМТ.
При проведении регрессионного анализа получена зависимость риска по шкале PROCAM от следующих независимых переменных:
PROCAM = – 64,55 + 15,76ТКИМ/ПОСА + 4,33ИА + 2,73D,ЛОСА + + 1,37НвА1с + 0,24ДАД – 0,03ЭАМ.
Все коэффициенты и константа значимы (таблица).
Таблица регрессионного анализа
|
№ п/п |
Модель |
Нестандартные коэффициенты |
р |
Доверительный интервал для В |
||
|
В |
Стандартная ошибка |
Нижняя граница |
Верхняя граница |
|||
|
1 |
Константа |
–64,55 |
10,64 |
0,0001 |
–85,71 |
–43,39 |
|
2 |
ТКИМ/ПОСА, мм |
15,76 |
4,58 |
0,001 |
6,64 |
27,87 |
|
3 |
ИА |
4,33 |
0,50 |
0,0001 |
3,34 |
5,32 |
|
4 |
D, ЛОСА, мм |
2,73 |
1,03 |
0,01 |
0,68 |
4,78 |
|
5 |
НвА1с, % |
1,37 |
0,46 |
0,004 |
0,46 |
2,28 |
|
6 |
ДАД, мм рт.ст. |
0,24 |
0,10 |
0,02 |
0,04 |
0,44 |
|
7 |
ЭАМ, мг/сут |
–0,03 |
0,01 |
0,04 |
–0,06 |
–0,001 |
Согласно выявленной закономерности, ведущую роль в формировании риска ишемических событий имеет характеристика структурного ремоделирования сосудистой стенки (ТКИМ/ПОСА), значимое влияние оказывают показатель атерогенности липидного спектра (ИА), морфологический параметр сосуда (D,ЛОСА), интегральный показатель углеводного обмена (НвА1с), минимальное значение имеют циркуляторный показатель функции эндотелия (ДАД) и маркер структурного поражения эндотелия (ЭАМ).
Установленный вклад показателей в развитии риска ишемических событий по шкале PROCAM, полученных при регрессионном анализе, не дает представления об их взаимосвязях и последовательности формирования. В связи с этим нами проведен пошаговый корреляционный анализ с использованием непараметрического критерия Спирмена, где в качестве системообразующего фактора выступает риск по PROCAM, а в качестве независимых переменных ‒ анализируемые параметры функции эндотелия, углеводного и липидного обменов, ИР с попыткой максимально охватить горизонтальные и вертикальные связи. При каждом последовательном шаге отбирались независимые параметры с наибольшим значением коэффициента корреляции и уровнем достоверности р < 0,05. Модель формирования риска ишемических событий представлена на рисунке. Полученная модель представлена 3 горизонтальными уровнями.
Базовый, 3-й уровень представлен 7 параметрами, которые можно распределить на 4 группы. Первая группа характеризует выраженность углеводных нарушений: НвА1с и стаж СД 2 т. Вторая группа акцентирует внимание на напряженность состояния ПОЛ-АОС: скорость окисления конечных продуктов пероксидации липидов (Е400/220гпт.ф) и второй этап утилизации перекисей – каталаза эритроцитов. Третья группа отражает формирование циркуляторных и структурных нарушений сосудистой стенки: стаж АГ и САД. Четвертая группа характеризует состояние нитроксидэргического статуса: NO2. Второй горизонтальный уровень представлен 4 показателями и продолжает преемственно 3-й уровень с акцентом на скорость окисления начальных продуктов пероксидации липидов (Е232/220изп.ф), на состояние общей антиоксидантной активности (МК), на углубление эндотелиального поражения в виде структурного ремоделирования сосуда (ТКИМ/ЛОСА) и структурного поражения эндотелия (ЭАМ). Второй уровень завершает каскад метаболических процессов в итоговом горизонтальном уровне, с выходом на интегральные параметры сосудистого ремоделирования (D,ЛОСА), субстрата ПОЛ (Е220гпт.ф), липидного обмена – ТГ. Интерес представляют и вертикальные связи, которые представлены 3-я ветвями. Первая вертикальная ветвь характеризует связь PROCAM с комплексом структурно-функциональных характеристик сосуда (D,ЛОСА – ТКИМ/ЛОСА – Стаж АГ – САД). Вторая вертикальная ветвь характеризует связь PROCAM с комплексом, отражающим липидные нарушения и ассоциирующимся с активностью ПОЛ-АОС, состоянием углеводного обмена, ДЭ (ТГ – ЭАМ – МК – НbА1с – Е400/220гпт.ф – Каталаза эритроцитов). Третья вертикальная ветвь характеризует связь PROCAM непосредственно с комплексом показателей, характеризующих состояние ПОЛ и нитроксидэргического статуса (Е220гпт.ф. – Е232/220изп.ф. – NO2).
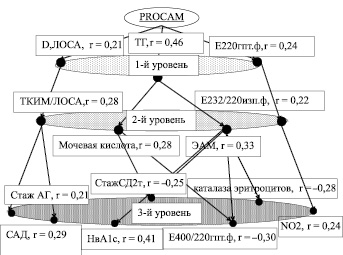
Модель формирования риска ишемических событий по шкале PROCAM у пациентов с сахарным диабетом 2 типа. Примечание. Представлены анализируемые показатели, формирующие риск ишемических событий и значения коэффициента корреляции Спирмена (r)
Полученные результаты характеризуют 2 методологических подхода к созданию модели формирования риска ишемических событий. Первая модель имеет плоскостной характер и четко ориентирована на традиционные факторы сердечно-сосудистого риска, с устойчивыми характеристиками кардиометаболического статуса. Вторая, пространственная модель акцентирует внимание не столько на факторы кардиоваскулярного риска, сколько на их модуляторы, в качестве которых выступает ПОЛ. При оценке многоуровневого формирования ишемического риска представленным уровням можно придать определенный статус: 3-й уровень можно обозначить как инициирующий (триггерный), являющийся пусковым моментом развития, 2-й как стабилизирующий и 1-й как состояние структурно-метаболического ремоделирования.
Выводы
1. В исследуемой группе пациентов при использовании традиционной модели формирования риска ишемических событий на базе PROCAM выявлено занижение риска сердечно-сосудистых осложнений у 77,78 % пациентов, в среднем на 57,15 %.
2. Регрессионная модель отражает иерархию формирования ишемического риска по интегральным характеристикам структурного и морфологического сосудистого ремоделирования, а также липидных и углеводных нарушений. В данной регрессионной модели сосудистое ремоделирование занимает ведущее место.
3. Пространственная корреляционная модель ишемического риска отличается более фундаментальным подходом, в котором имеются как регулируемые процессы, так и их регуляторные механизмы, причем последние присутствуют на всех этапах формирования модели PROCAM. Принципиально то, что получены 3 независимые вертикальные ветви формирования ишемических событий, одна из которых характеризует преимущественно сосудистые изменения, вторая ветвь отражает связь с комплексом метаболических нарушений, третья ветвь характеризует процессы ПОЛ и АОС. Каждая из ветвей имеет равнозначное влияние на формирование ишемического риска.
4. Сходство в полученных моделях заключается в выявлении значимости одних и тех же показателей, в формировании ишемического риска, а различие ‒ в наличии особой регуляторной ветви, характеризующей состояние ПОЛ-АОС, которая тождественна по силе как структурным, так и метаболическим ветвям формирования PROCAM.
5. В корреляционной модели ярко продемонстрирована этапность становления риска ишемических событий, в виде формирования АГ и СД 2 т и связанных с ними нарушений метаболизма. Далее следует стабилизация с формированием как начальной морфологической перестройки сосудистой системы, так и углубления метаболических нарушений в виде дисфункции эндотелия и оксидативного стресса. Конечный этап определяется непосредственными предшественниками ишемических событий в виде структурного метаболического ремоделирования с выходом на ключевой морфологический параметр сосудистой стенки и свободнорадикальное окисление ТГ.
Рецензенты:
Вардугина Н.Г., д.м.н., профессор кафед ры клинической фармакологии и терапии факультета дополнительного профессионального образования, ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Челябинск;
Шапошник И.И., д.м.н., профессор, заведующий кафедрой пропедевтики внутренних болезней, ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Челябинск.
Работа поступила в редакцию 28.05.2014.
Библиографическая ссылка
Чернышева С.Ю., Кузин А.И., Камерер О.В. КАРДИОМЕТАБОЛИЧЕСКАЯ МОДЕЛЬ ФОРМИРОВАНИЯ РИСКА ИШЕМИЧЕСКИХ СОБЫТИЙ У ПАЦИЕНТОВ С САХАРНЫМ ДИАБЕТОМ 2 ТИПА: ВЫХОД НА КЛЮЧЕВЫЕ МЕТАБОЛИЧЕСКИЕ ПАРАМЕТРЫ // Фундаментальные исследования. 2014. № 7-3. С. 590-594;URL: https://fundamental-research.ru/en/article/view?id=34492 (дата обращения: 16.05.2026).



