Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
CLARIFICATION OF IRON ORE WITH MOLTEN SODIUM HYDROXIDE
Продукт обогащения железной руды методом магнитной сепарации, предназначенный для получения железа доменным способом, называется рядовым концентратом. Рядовые концентраты содержат от 60 до 70 % железа и до 10 % примесей, в которых преобладает кремний в виде кварца и других кремнийсодержащих минералов, а также алюминий, кальций, магний и другие примеси. Более полная очистка рядового концентрата от примесей не требуется, так как процессы очистки происходят в самом доменном процессе: в расплавленном состоянии примеси переходят в шлак при взаимодействии с карбонатом кальция, который в виде известняка вводится в домну вместе с концентратом.
Положение кардинально меняется при самостоятельном использовании железорудного концентрата для получения порошкового и губчатого железа, синтеза ферритов, в производстве щелочных аккумуляторов, в химических процессах (получение гидроксида натрия ферритным методом, переработка нитрата натрия и др.), Для этих целей производятся чистые концентраты, в которых общее содержание примесей снижено до 2–3 %, в том числе кремния до 0,4–1,3 %. Чистые концентраты получают из рядовых, применяя дополнительное измельчение, обработку в сильных магнитных полях, флотацию.
Но уже сейчас необходимы и в ближайшей перспективе технического прогресса потребуются в большом количестве сверхчистые концентраты, в которых содержание примесей должно быть на уровне сотых долей процента. Их получение традиционными методами магнитной сепарации и флотации чрезвычайно затруднено и практически невозможно, так как потребуется сверхтонкое, технически не достижимое, измельчение исходного материала.
Производство сверхчистых концентратов возможно методами химического обогащения либо непосредственно железной руды, либо её концентратов. Более целесообразно использование в качестве исходного материала рядовых или чистых концентратов, так как в этом случае снижается расход химических реагентов.
Исследования по химическому обогащению железных руд проводятся во многих промышленно развитых странах [1]. В России наиболее полные исследования по химическому обогащению железных руд и по получению сверхчистых концентратов химическими методами проведены в Томском политехническом университете [2]. Изучена растворимость рядовых концентратов в кислотах [3] и очистка от кальция и магния азотной кислотой в стационарном режиме [4] и при совмещении кислотной обработки с измельчением [5].
Особое внимание в этих исследованиях уделено очистке от кремния, который во всех железных рудах является основной примесью. Для его удаления из рядовых концентратов использовались растворы гидроксида натрия, эффективность которых примерно на порядок выше, чем гидроксида калия. Установлено, что при температурах, значения которых ниже температур кипения растворов щёлочи (80–125 °С), полной очистки от этой примеси не происходит из-за резкого замедления после выщелачивания небольшой части (10–20 %) за первое время (до 30 мин) от начала процесса [6]. Другие результаты получены при автоклавном выщелачивании – при температурах выше температур кипения растворов (при 140–200 °С): в этих экспериментах установлено практически полное выщелачивание кремния, а также очистка от других примесей [7, 8].
Предметом настоящего исследования является изучение возможности очистки железной руды от примесей кремния расплавленным гидроксидом натрия.
Материалы и методы исследований
В учебной литературе по химии указывается [9], что кремнезём SiO2 необратимо взаимодействует с расплавленным гидроксидом натрия при 400–500 °С по реакции:
SiO2 + 2NaOH = Na2SiO3 + H2O
В производстве алюминия вскрытие алюминийсодержащих минералов производят расплавленным карбонатом натрия, но в исходную шихту часто добавляется гидроксид натрия NaOH для снижения температуры процесса [10].
Сплавление кремний- и алюминийсодержащих минералов со щелочами применяется в аналитических лабораториях при химическом анализе многих природных веществ – эта классическая операция называется «вскрытием» минералов [11].
В нашем литературном обзоре [1, 2] отмечено, что обработка расплавленным карбонатом натрия (кальцинированной содой) изучается как один из возможных способов очистки железных руд от примесей. Например, известен японский патент, по которому железную руду для удаления из неё алюминия, хрома и других примесей спекают с содой, а затем обрабатывают спеки водой [12], но условия этой операции в патенте не указываются.
Способ спекания с карбонатом натрия изучался в России. В лабораторных опытах рядовой железорудный концентрат спекали с содой при 850 °С, затем спек измельчали и промывали водой, затем 1 %-й соляной кислотой и опять водой [13]. Но в промышленности эта технология не применяется из-за недостаточно полной очистки от кремния.
При изучении этих литературных данных возникает вопрос: почему исследователи применяют карбонат натрия и не применяют гидроксид натрия? На этот вопрос нет чёткого обоснованного ответа. По нашему мнению, возможны следующие причины.
1. Стоимость гидроксида натрия в несколько раз выше стоимости карбоната натрия. Это действительно так, но при обработке чистых железорудных концентратов, в которых содержание SiO2 и Al2O3 находится на уровне 1–2 %, расход щёлочи небольшой, а главное, её можно регенерировать при обработке получаемых растворов силиката и алюмината натрия гашёной известью (гидроксидом кальция):
Na2SiO3 + Ca(OH)2 = CaSiO3+ 2NaOH;
2NaAlO2 + Ca(OH)2 = Ca(AlO2)2+ 2NaOH
2. Более высокие требования по технике безопасности при работе с твёрдым гидроксидом натрия, так как опасно попадание пылевидных частиц этой щёлочи в органы дыхания человека. Но в современных технологиях весь технологический процесс можно проводить в автоматическом программированном режиме с помощью роботов без участия человека.
Исходя из этих соображений, мы провели исследование по применению расплавленного гидроксида натрия для выщелачивания примесей кремния из железной руды.
В опытах использовался рядовой Криворожский концентрат, который применялся в исследованиях по его очистке растворами гидроксида натрия [6]. Приводим его состав: ( %): Fe2O3 - 92,5, SiO2 - 4,31, Al2O3 - 0,76, CaO - 0,38, MgO - 0,020, TiO2 - 1,81, сера – 0,051, фосфор – 0,042. Концентрат состоит из частиц, прошедших через сито 2 мм. В опытах использовался гидроксид натрия по ГОСТ 2263-79: содержание NaOH – 98,5 %, содержание примесей ( %): карбонат натрия – 0,8 %, хлорид натрия – 0,05 %, сульфат натрия – 0,03 %, кремний в расчёте на SiO2 – 0,02 %, сумма кальция и магния – 0,01 %.
Смесь концентрата с гидроксидом натрия размещали в 5 одинаковых тиглей, изготовленных из обычной углеродистой стали, которая до температуры 600 °С достаточно устойчива к коррозии в расплавленных щелочах. Тигли одновременно помещали в разогретую муфельную печь, а вынимали из неё последовательно через 1, 2, 3, 4 и 5 часов. Продукт реакции (спек) измельчали и отмывали от щёлочи и продуктов реакций горячей водой. Контроль процесса проводили анализом концентрата на остаточное содержание в нём кремния.
Результаты исследований и их обсуждение
Вначале все опыты были проведены при температуре 450 °С. Эта температура более чем на 100 градусов превышает температуру плавления гидроксида натрия (322 °С), поэтому расплав обладает текучестью, небольшой вязкостью и хорошо смачивает частицы концентрата. С другой стороны, эта температура уменьшает вероятность взаимодействия гидроксида натрия с основным рудным минералом гематитом. При этой температуре было проведено пять опытов, в которых изменялось соотношение щёлочи к концентратe: от 0,1:1, затем 0,5:1, и далее 1:1, 2:1 и 3:1. Полученные результаты приведены в табл. 1.
Таблица 1
Показатели очистки Криворожского концентрата расплавленным гидроксидом натрия при различном соотношении щёлочь:концентрат.
Постоянные условия: температура – 450 °С, размер частиц концентрата – до 2 мм, исходное содержание SiO2 – 4,31 %
|
Соотношение щёлочь: концентрат |
Степень очистки от SiO2 за время (ч) |
||||
|
1 |
2 |
3 |
4 |
5 |
|
|
0,1:1 |
9,8 |
15,6 |
20,1 |
22,6 |
24,8 |
|
0,5:1 |
14,7 |
28,0 |
37,1 |
45,2 |
50,1 |
|
1:1 |
22,2 |
39,8 |
51,3 |
64,0 |
71,8 |
|
2:1 |
34,6 |
57,5 |
75,0 |
86,6 |
93,6 |
|
3:1 |
70,3 |
92,4 |
98,5 |
100 |
100 |
Из табл. 1 видно, что соотношение щёлочь:концентрат сильно влияет на степень выщелачивания. Соотношения 0,1:1, 0,5:1 и 1:1 применять нецелесообразно, так как даже за 5 ч процесс выщелачивания кремния далеко не заканчивается. При соотношении 2:1 за 5 ч выщелачивается 93,6 % SiO2, при соотношении 3:1 через 3 ч степень выщелачивания достигает 98,5 %, а за 4 ч наблюдается полная 100 %-я очистка от кремния. Но высокая степень выщелачивания кремния при соотношении 2:1 и 3:1 осложняется образованием такого прочного продукта спекания, что для его измельчения требовались значительные усилия. При меньших соотношениях продукты спекания были менее прочными, они легко измельчались, но степень выщелачивания примесей кремния недостаточна (23–70 %) даже за 5 ч.
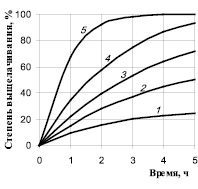
Рис. 1. Выщелачивание кремния из Криворожского концентрата расплавленным гидроксидом натрия при соотношении щёлочь:концентрат 0,1:1 (1), 0,5:1 (2), 1:1 (3), 2:1 (4), 3:1 (5). Температура 450 °С
Для наглядного представления о процессе эти результаты представлены на графике в координатах время процесса – степень выщелачивания (рис. 1). Видно, что эта зависимость имеет вид, характерный для реакций первого порядка, поэтому средняя скорость процесса максимальна в течение первого часа, но при дальнейшей выдержке она быстро уменьшается.
Была изучена возможность улучшения показателей процесса за счёт повышения температуры. С этой целью проведены опыты при 500, 550 и 600 °C при соотношении щёлочь:концентрат, равном 1:1. Полученные результаты приведены в табл. 2 и на рис. 2.
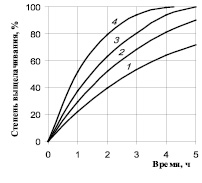
Рис. 2. Выщелачивание кремния из Криворожского концентрата расплавленным гидроксидом натрия при 450 (1), 500 (2), 550 (3) и 600 °С (4)
Полученные результаты свидетельствуют о том, что при температурах 550–600 °С Криворожский рядовой концентрат полностью очищается расплавленным гидроксидом натрия от примесей кремния за время реакции 4–5 часов в стационарном режиме (без перемешивания). Можно ожидать, что при перемешивании скорость выщелачивания будет более высокой, и за счёт этого время процесса уменьшится.
Таблица 2
Влияние температуры процесса на степень очистки Криворожского рядового концентрата от кремния при соотношении щёлочь:концентрат 1:1
Постоянные условия: размер частиц концентрата – до 2 мм, исходное содержание SiO2 – 4,31 %.
|
Температура, °C |
Степень выщелачивания SiO2 за время (ч) |
||||
|
1 |
2 |
3 |
4 |
5 |
|
|
450 |
22,2 |
39,8 |
51,3 |
64,0 |
71,8 |
|
500 |
31,6 |
52,3 |
67,5 |
81,2 |
90,1 |
|
550 |
37,5 |
61,8 |
80,3 |
94,0 |
99,8 |
|
600 |
51,6 |
79,5 |
94,1 |
99,6 |
100 |
Выводы
- Обработка расплавленным гидроксидом натрия может рассматриваться как метод очистки железных руд от примесей кремния, альтернативный методам, основанным на использовании растворов щёлочи.
- Для Криворожского концентрата полная очистка от примесей кремния при использовании расплавленного гидроксида натрия достигается при соотношении щёлочь:концентрат, равном 1:1, температуре процесса 550–600 °С, времени обработки 4–5 часов.
- В технологическом плане обработка расплавленным гидроксидом натрия может быть осложнена образованием прочного продукта спекания и большими трудностями по его дальнейшей обработке (измельчение, отделение избыточной щёлочи, промывка и т.д.).
- Для других железных руд условия проведения процесса очистки расплавленными щелочами необходимо уточнять проведением дополнительных исследований.
Рецензенты:
Саркисов Ю.С., д.т.н., профессор, заведующий кафедрой химии Томского государственного архитектурно-строительного университета, г. Томск;
Лотов В.А., д.т.н., профессор кафедры силикатов и наноматериалов Томского политехнического университета, г. Томск.
Работа поступила в редакцию 01.04.2014.
Библиографическая ссылка
Стась Н.Ф. ОЧИСТКА ЖЕЛЕЗНОЙ РУДЫ ОТ ПРИМЕСЕЙ РАСПЛАВЛЕННЫМ ГИДРОКСИДОМ НАТРИЯ // Фундаментальные исследования. 2014. № 5-6. С. 1187-1190;URL: https://fundamental-research.ru/en/article/view?id=34064 (дата обращения: 13.05.2026).



