Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
STATE OF MECHANICAL STRENGTH INTESTINAL ANASTOMOSIS FORMED WITH IMPLANTS MADE OF NITINOL OBTAINED FIBREWISE ELECTRON BEAM SYNTHESIS
В практике абдоминальной хирургии часто возникает необходимость соединения между собой различных отделов желудочно-кишечного тракта (наложения анастомозов). Известен способ создания компрессионных желудочно-кишечных и межкишечных соустий при помощи имплантатов из нитинола с эффектом памяти формы. Восстановление непрерывности кишечной трубки с использованием данной методики упрощает выполнение операции и повышает надёжность сформированных соединений [1, 4].
Способность нитиноловых имплантатов запоминать форму (восстанавливать исходную форму при нагреве) находит достаточно широкое применение в медицине. Сплавы на основе нитинола выдерживают сотни тысяч циклов знакопеременной деформации без разрушения, обладают высокой прочностью, коррозионной стойкостью и биологической совместимостью с тканями организма [3, 4].
В настоящее время в России наблюдается острая нехватка технологического плавильного оборудования для получения нитиноловых сплавов, в связи с чем изготовленные из этих сплавов устройства для наложения анастомозов не всегда соответствуют требованиям, гарантирующим безопасность хирургического вмешательства. В частности, недостаточная степень компрессии имплантатом стенки кишки в месте его установки может привести к механической негерметичности наложенного соустья.
Процесс послойного электронно-лучевого синтеза обеспечивает изготовление полнофункциональных имплантатов из гранул нитинола с помощью электронного луча. Высокая энергия электронного пучка позволяет добиться высокой скорости наплавки и малого времени кристаллизации расплавленного нитинола. Это позволяет получить имплантаты с высокими механическими и теплофизическими свойствами, в первую очередь с более надёжной степенью компрессии и полным возвращением изделия к исходной форме.
Вышеуказанные данные говорят об актуальности изучения вопросов применения имплантатов, полученных с помощью новой технологии, при анастомозировании полых органов желудочно-кишечного тракта.
Целью настоящей работы явилось изучение в эксперименте механической прочности анастомозов кишечной трубки, сформированных при помощи имплантата из нитинола, полученного послойным электронно-лучевым синтезом.
Материал и методы исследования
Экспериментальное исследование проведено на 30 взрослых беспородных собаках. Собака имеет схожее с человеком строение кишечника, в связи с чем и была выбрана для эксперимента [5]. Хирургические операции выполнены на тонкой кишке. Осуществлялось формирование межкишечных анастомозов по типу «бок в бок».
Исследование было одобрено этическим комитетом ГБОУ ВПО «Тверская ГМА» МЗ России соответствующим протоколом. Все эксперименты на лабораторных животных были выполнены в соответствии с «Правилами проведения работ с использованием экспериментальных животных», утверждёнными приказом МЗ СССР № 755 от 12.08.1977 года, и основываясь на положениях Хельсинкской Декларации Всемирной Медицинской Ассоциации от 1964 года, дополненной в 1975, 1983, 1989 и 2000 годы [3]. Исследовательская работа проводилась на базе экспериментальной лаборатории и вивария ГБОУ ВПО «Тверская ГМА» МЗ России. Животные прооперированы с соблюдением всех правил асептики и с использованием комбинированной анестезии.
Все животные ранее были вакцинированы от бешенства и дегельминтизированы. В опыте использовались собаки массой 10–20 кг. Выбраковывались длинношерстные особи, чрезмерно агрессивные, с кожными и другими заболеваниями, беременные, а также животные моложе 1 года и старше 6 лет. Возраст собак определялся по зубной таблице, предложенной Западнюк И.П. [1, 3].
Всего наложено 60 тонко-тонкокишечных анастомозов. Сформированные соустья были разделены на 3 исследовательские группы (по 20 в каждой группе). Группу 1 составили анастомозы, наложенные с помощью хирургической шовной нити и кишечной иглы; группу 2 – компрессионные анастомозы, наложенные с помощью имплантата из нитинола, полученного традиционным способом; группу 3 – компрессионные анастомозы, наложенные с помощью имплантата из нитинола, полученного послойным электронно-лучевым синтезом.
Механическую прочность межкишечных анастомозов, сформированных различными способами, оценивали на 1-е, 3-е, 14-е и 30-е сутки после хирургической операции методом пневмопрессии по методике Матешука B.П. [4, 7]. Для этого использовали пневмопрессор, который состоял из манометра, груши для накачивания воздуха и раздувающейся головки на конце силиконового шланга. Манометр позволял измерять давление в пределах от 10 до 260 ± 5 мм рт.ст. По данным литературы, давление в желудочно-кишечном тракте находится в пределах 3330–4660 Па (25–35 мм рт.ст.) [8].
Измерение выполняли следующим образом: в просвет иссечённого участка кишки с анастомозом вводили силиконовый шланг, соединённый с манометром, кишку с обеих сторон стягивали прочной лигатурой. Макропрепарат помещали под воду и затем медленно нагнетали воздух, контролируя показания манометра.
Пределом механической прочности анастомоза считалось давление, при котором в воде, над швом соустья, появлялись пузырьки воздуха (рисунок). Если при достижении максимального давления манометра пузырьки воздуха не появлялись, то считали, что межкишечный анастомоз сохраняет механическую герметичность при давлении в 34668 Па (260 мм рт.ст.). Анастомоз считали механически герметичным, если он выдерживал давление не менее 6667 Па (50 мм рт.ст.) [8, 10]. Полученные данные переводили в единицы СИ (Па) согласно ГОСТ 8.417–2002 «Единицы величин» (от 01.09.2003), при этом 1 мм рт.ст. = 133,34 Па [2].
Статистическая обработка данных осуществлялась расчётом распределения признака М ± m, где М – средняя арифметическая и m – средняя ошибка средней арифметической анализируемых показателей. Поскольку объём выборки не соответствовал закону нормального распределения, то для оценки одинакового признака в трёх независимых группах использовался непараметрический ранговый Н – критерий Крускала – Уоллиса. При этом если выявлялось различие между исследуемыми группами (отвергалась нулевая гипотеза), то дополнительно определялось, между какими именно попарными группами (I–II; I–III; II–III) есть достоверные статистически значимые различия при помощи непараметрического рангового Q – критерия Данна. Различия считались статистически значимыми при уровне значимости p < 0,05.
Результаты исследования и их обсуждение
Результаты исследования механической прочности анастомозов методом пневмопрессии представлены в таблице.
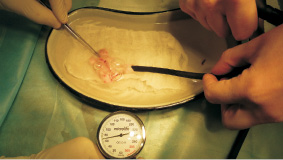
Метод пневмопрессии
Результаты исследования механической прочности анастомозов методом пневмопрессии (Па)
|
Срок исследования, сутки |
Показатель давления разрыва анастомоза, Па |
||
|
группа I (n = 20) |
группа II (n = 20) |
группа III (n = 20) |
|
|
1-е |
20000 |
18700 |
19390 |
|
19880 |
19500 |
19470 |
|
|
19550 |
18900 |
19850 |
|
|
18000 |
19330 |
18900 |
|
|
18400 |
20000 |
20010 |
|
|
М + m |
19166 ± 406 (р1-2 > 0,05) |
19286 ± 229 (р2-3 > 0,05) |
19524 ± 194 (р1-3 > 0,05) |
|
3-и |
12010 |
15450 |
16550 |
|
11930 |
14900 |
16010 |
|
|
11970 |
14600 |
15430 |
|
|
13000 |
15550 |
16020 |
|
|
12000 |
13600 |
15010 |
|
|
М ± m |
12182 ± 205 (р1-2 < 0,05) |
14820 + 352 (р2-3 > 0,05) |
15804 ± 266 (р1-3 < 0,05) |
|
14-е |
21670 |
25630 |
26300 |
|
22330 |
24760 |
26760 |
|
|
21000 |
25040 |
27590 |
|
|
22570 |
24050 |
27760 |
|
|
22450 |
24870 |
26470 |
|
|
М + m |
22004 ± 295 (р1-2 < 0,05) |
24870 ± 254 (р2-3 < 0,05) |
26976 ± 296 (р1-3 < 0,05) |
|
30-е |
32630 |
34668 |
34668 |
|
31320 |
32870 |
34668 |
|
|
31430 |
32670 |
34668 |
|
|
31480 |
33590 |
34668 |
|
|
32570 |
34600 |
34668 |
|
|
М + m |
31886 ± 293 (р1-2 < 0,05) |
33680 ± 419 (р2-3 < 0,05) |
34668 ± 0 (р1-3 < 0,05) |
По литературным данным, в раннем послеоперационном периоде изменение внутриполостного давления носит однотипный характер: в течение первых 24–36 часов оно составляет для тонкой кишки 1080 ± 93 Па, а затем в течение суток возвращается к исходному значению. Критический уровень приводящего к недостаточности анастомоза внутриполостного давления, сохраняющегося в течение 10 и более часов, при этом составляет 1667–1733 Па [6, 7].
Известно, что в первые сутки все анастомозы, как ручные, так и компрессионные, физически герметичны. Наименьшая механическая герметичность соустья, как ручного, механического, так и компрессионного, наблюдается на 3–5-е сутки [4, 8]. Это объясняется тем, что на фоне окончательно несформированной соединительнотканной спайки к этому времени в кишечном шве фиксация тканей нитями или устройствами значительно уменьшается за счёт релаксации тканей, некроза и ишемии. При этом на 6–7-й день давление разрыва значительно возрастает, а к 8–14-му дню приближается к величине давления разрыва интактной стенки кишки [6] за счёт активного синтеза нового коллагена, организации фибрина, стихания воспаления.
Традиционные устройства из нитинола с эффектом памяти формы в виде канцелярской скрепки, где 15 % периметра выполняется ручным лигатурным швом, показали, что механическая герметичность компрессионного шва со 2-х по 5-е сутки снижается до 12267 Па, и в этот период он уступает по прочности ручному [4]. В исследованиях В.В. Спирева и О.А. Фатюшиной [2], посвящённых применению компрессионных циркулярных анастомозов, давление разрыва не снижалось на 3-и сутки ниже 13340 Па и значительно превышало подобные показатели для ручного шва, что объясняется отсутствием лигатурной порции.
В проведённых нами исследованиях несостоятельной была ручная лигатурная часть периметра компрессионного анастомоза, причём пузырьки воздуха появлялись в местах проколов иглы, а не между стежками. Объяснение данного факта изложено в работах, посвящённых механической герметичности кишечного шва [3, 5]. В этом заключается ключевая особенность любого компрессионного анастомоза по типу «бок в бок»: прочность соустья определяется ручной лигатурной порцией периметра.
Результаты нашего исследования показывают, что статистически значимых различий анастомозов по степени прочности в первые сутки после операции между группой I, группой II и группой III не было (р > 0,05), исключая 3-и сутки эксперимента, когда прочность анастомозов группы III превышала таковую соустий группы I и группы II (р < 0,05).
По данным литературы, заживление анастомозов полых органов желудочно-кишечного тракта напрямую зависит от выраженности воспалительных изменений в кишечном шве [3]. Снижение механической герметичности анастомоза на 3–5-е сутки объясняется прогрессированием альтерации, которая преобладает над процессами репаративной регенерации. При формировании компрессионного анастомоза, как было подтверждено, выраженность воспалительной реакции ниже, чем в ручном лигатурном шве.
Механическая прочность анастомозов, сформированных нитиноловыми имплантатами, изготовленными по новой технологии, превосходила таковую на 14-е и 30-е сутки после операции в группе I и в группе II (р < 0,05).
Заключение
Таким образом, изучение компрессионных межкишечных анастомозов показало их высокую механическую прочность. Во все сроки исследований она была выше прочности соустий, сформированных традиционным ручным способом, исключая 1-е сутки после операции. Кроме того, механическая прочность анастомозов группы III превышала таковую в группе II, за исключением третьих суток.
Результаты исследования свидетельствуют о том, что имплантаты из нитинола, полученные электронно-лучевым синтезом, обеспечивают более надёжную компрессию кишечных стенок, обеспечивая достаточную герметичность формируемых соединений. В связи с этим имеются основания считать, что использование новых имплантатов при наложении анастомозов кишечной трубки в клинике приведёт к снижению числа послеоперационных осложнений, обусловленных развитием несостоятельности сформированных соустий.
Рецензенты:
Цай Г.Е., д.м.н., профессор кафедры топографической анатомии и оперативной хирургии, ГБОУ ВПО «Тверская ГМА» МЗ России, г. Тверь;
Никольский А.Д. д.м.н., профессор кафедры госпитальной хирургии с курсом урологии, ГБОУ ВПО «Тверская ГМА» МЗ России, г. Тверь.
Работа поступила в редакцию 03.04.2014.
Библиографическая ссылка
Мохов Е.М, Розенфельд И.И, Соколов Ю.А СОСТОЯНИЕ МЕХАНИЧЕСКОЙ ПРОЧНОСТИ МЕЖКИШЕЧНЫХ АНАСТОМОЗОВ, СФОРМИРОВАННЫХ ПРИ ПОМОЩИ ИМПЛАНТАТОВ ИЗ НИТИНОЛА, ПОЛУЧЕННОГО ПОСЛОЙНЫМ ЭЛЕКТРОННО-ЛУЧЕВЫМ СИНТЕЗОМ // Фундаментальные исследования. 2014. № 4-3. С. 564-568;URL: https://fundamental-research.ru/en/article/view?id=33961 (дата обращения: 11.06.2026).



