По данным Международного агентства по изучению рака (МАИР), к 2030 году ежегодное количество новых случаев заболевания раком в мире превысит 21 млн человек, а число смертей от рака достигнет 13 млн На современном этапе рак остается главным заболеванием развитых стран. В Африке умирают от рака 4 % людей по сравнению с 19 % в Европе. По данным группы онкологической статистики Российского онкологического научного центра РАМН им. Н.Н. Блохина, в 2007 году скончалось от рака 288,6 тыс. человек, в день это заболевание уносит около 780 россиян. Мужчины гибнут в основном от рака легкого, желудка и предстательной железы. А женщины – от рака молочной железы, желудка, ободочной и прямой кишки и яичников. С 1997 по 2007 год прирост числа заболевших онкологическими заболеваниями составил 13 %. Эти цифры свидетельствуют об актуальности изучения причин и механизмов развития онкозаболеваний [2, 34]. В последнее время появилось множество работ, на основе молекулярно-генетических методов свидетельствующих о вовлечении в онкопроцесс различных структур организма под воздействием ПВЧ (НPV) инфекции: рак шейки матки, колоноректальный рак, рак носоглотки, и даже рак молочной железы [2, 7, 12, 18]. По данным Всемирной организации здравоохранения, ежегодно в мире вирусы папилломы человека вызывают до 500 000 новых случаев рака шейки матки и ежегодно около 240 000 женщин умирают от цервикального рака [http://www.who.int/mediacentre/factsheets/fs297/ru/]. Несмотря на огромное количество работ, посвящённых изучению папилломовирусной инфекции (НPI), разработку профилактики заражения папилломавирусом человека (НPV) и носительства у людей различных возрастных групп, получение исчерпывающих данных о более, чем 150 видах вируса НPV, определение степени их патогенности, вопрос о ранней диагностике онкогенеза в структурах организма человека, повреждаемых НPV, до сих пор не решён окончательно [26]. Открытие эндогенных вирусов, ознаменовавшее новый этап в развитии вирусогенетической теории возникновения рака, сформулированной Л.А. Зильбером (1938), потребовало по-новому пересмотреть всю проблему онкогенеза в целом [24]. Появившиеся в последние годы более общие концепции и гипотезы уже включают в себя все положения и постулаты вирусогенетической теории как неотъемлемую часть, а в качестве индукторов рассматриваются как различные причины, так и различные микроорганизмы [6, 14, 17, 21, 22]. Попытки разработки вакцинации дендритными клетками пока не дают желаемых результатов, а указывают на необходимость пересмотра современных стратегий по изучению канцерогенеза [11, 19.] Тем более, что 98 % спонтанно выздоравливающих пациентов без лечения при НPV-инфекции свидетельствуют о некоторой спекулятивности в необходимости вакцинации для профилактики онкогенеза HPV ассоциированной этиологии, а также об отсутствии исчерпывающих доказательных данных о том, что определённые штаммы, чаще встречающиеся на фоне онкологии шейки матки, более патогенны, чем другие. Несмотря на многочисленные полученные сведения о биологии вируса, путях заражения, патогенезе, клинических проявлениях инфекции, поражённости HPV-инфекцией, природа и механизмы развития разрастаний структур кожи, подвергшихся контаминации вируса, до сих пор не известны, а также не доказано, что именно папилломавирусы вырабатывают пусковые для канцерогенеза веществa [9]. Обсуждается роль иммуноцитов при ПВЧ (НPV)-инфекции различных структур организма человека [12, 20]. На современном этапе рассматриваются различные концепции канцерогенеза, на которых должны базироваться диагностические стратегии, обсуждаются подходы к лечению ПВИ (PVI), включающие деструктивные (физические, химические), хирургические, иммунологические и комбинированные методы [10, 15, 23]. Также пока не установлены точные механизмы повреждения НPV кожи и слизистых оболочек человека. До сих пор не решён вопрос, от чего зависит глубина контаминации в эпителиальные пласты вируса, каков механизм канцерогенеза при HPV [7]. Убедившись в несостоятельности концепций онкогенов, протоонкогенов, антионкогенов, стратегия поиска на современном этапе направлена на выявление HPV-индуцированных онкогенетических нарушений в последовательности нуклеотидов в ДНК соматических клеток человека [27]. Также на современном этапе открыт вопрос о происхождении опухолевых клеток [24]. Учитывая высокую инфицированность населения HPV, актуальность изучения особенностей развития альтерации кожи при длительной вирусной контаминации в коже человека является чрезвычайно высокой, что определило направление нашей работы.
Цель исследования – установить особенности повреждения структур кожи человека при хронической HPV-инфекции.
Задачи исследования – дать характеристику морфологических особенностей альтерации структур кожи при HPV-инфекции.
Материалы и методы исследования
Исследование было проведено с учётом положений Хельсинкской декларации (2000) и с разрешением этического комитета ФГАОУ ВПО «Дальневосточный федеральный университет». По клиническим показаниям и с письменного информированного согласия пациентов произвели забор биоптатов кожи у 129 пациентов в возрасте от 45 до 78 лет, которых распределили с учётом возрастных групп, принятых Международным симпозиумом по возрастной периодизации в Москве (1965 г.) и сроков заболевания HPV-инфекцией (таблица).
Распределение больных с учётом возрастной периодизации и сроков давности HPV-инфекции
|
Количество больных в возрастных группах |
Всего больных |
Длительность заболевания |
|||
|
2 года |
3 года |
4 года |
5 лет и более |
||
|
VI |
12 |
3 |
3 |
3 |
3 |
|
VII |
14 |
4 |
3 |
4 |
3 |
|
VIII |
22 |
7 |
5 |
7 |
3 |
|
IX |
23 |
8 |
5 |
7 |
3 |
|
X |
29 |
5 |
9 |
11 |
4 |
|
XI |
16 |
3 |
5 |
4 |
4 |
|
XII |
13 |
3 |
3 |
6 |
1 |
|
Итого |
129 |
33 |
33 |
42 |
21 |
По клиническим показаниям и с согласия пациентов производили забор биоптатов кожи в зоне разрастаний предполагаемой папилломавирусной этиологии. Полученные биоптаты фиксировали в 10 %-м формалине на фосфатном буфере с рН 6,8–7,2 в течение 24 часов, затем промывали в воде в течение 2-х часов и обезвоживали в спиртах возрастающей концентрации в течение 1 часа в каждой порции. В спирте 96 °С выдерживали в течение 1, 2, 4 часов, а затем помещали в абсолютный спирт 5 раз по 30 минут, потом оставляли в последней порции на всю ночь. После этого материал помещали в смесь абсолютного спирта и ксилола в соотношении 1:1 на 30 минут, а затем в сменах ксилола в термостате при 37 °С по 30 минут в каждой. После этого использовали смесь ксилола с парафином (1:1) при 56 °С по 20 минут в 2 порциях, а затем в двух порциях парафина при 56 °С (по 1 часу в каждой порции), после чего проводили заливку. Парафиновые блоки выдерживали в течение суток в термостате при 37 °С, после чего производили срезы толщиной 3–5 мкм. Срезы и вся дальнейшая обработка материала (депарафинирование и обезвоживание) выполнялась на автоматизированной аппаратуре лаборатории патоморфологии Медицинского университета Ниигата (Япония). Идентификация иммунокомпетентных клеток проводилась по одинаковой схеме, несмотря на различную локализацию антигена в клеточных структурах: мембраны, лизосомы, комплекс Гольджи. Иммуногистохимическими методами на определение CD68 в биоптатах кожи, сохраненных в растворе Митчела, с помощью экспрессии GDI-антигена – гликопротеина, являющегося высокоспецифичным маркером для клеток Лангерганса (Dendriticcells, DC, клетки Steinman RalphM., 1973, [42]) и их пролиферирующих форм, произвели фенотипирование иммуноцитов и проанализировали их количественные соотношения, а также выявили особенности топографии иммуноцитов при НPV. С помощью моноклональных антител (клон КР1, код № М 0814, лот 119) выявляли макрофаги по маркёру CD68 (высокогликозилированный трансмембранный гликопротеин, который локализуется в лизосомах). Молекулярный клон CD68 показал, что семейство лизосомальных гликопротеинов с плазматическими мембранными белками играют роль в лизосомальном трафике и эндоцитозе, включая лизосомальные ассоциации мембранных протеинов 1 и 2 (LAMP- 1 и LAMP-2). Демаскировка антигенных детерминант проводилась в стеклянном контейнере, заполненном восстанавливающим раствором, с созданием водяной бани в течение одного часа. Часть препаратов была обработана в течение 30 минут с помощью микроволнового излучения, которое даёт лучший демаскировочный эффект. Для демаскировки антигенов использовали 10 ммоль/л цитратный буфер с рН 6,0 или DAKO TRS (Targetretrievalsolution, code № S1700). Остывшие препараты промывали в дистиллированной воде. Антитела применяли в разведении 1:50 и 1:100. Анализ материала проведён с помощью микроскопа Olympus – Bx82 и цифровой камеры РDх25.
Результаты исследования и их обсуждение
Нами установлено, что при хронической HPV-инфекции с длительностью заболевания более чем 2 года, в возрастной группе старше 45 лет, в коже некоторых больных происходит некротизация части эпидермиса как на поверхности, так и в глубине папилломатозных разрастаний (рис. 1, а). Нами отмечено, что CD68 клетки с антигенпрезентирующей функцией идентифицируются исключительно только в соединительной ткани сосочкового слоя дермы (рис. 1, б). При появлении воспалительного инфильтрата под блестящим слоем в сочетании с разрушением базальной мембраны эпидермиса и гибели базальных и шиповатых клеток происходит их замещение клетками крови, не способными дифференцироваться в эффекторные клетки (рис. 1, в). Кроме этого, лейкоцитарная инфильтрация, которая при HPV-инфицированности до 2-х лет наблюдается только в пределах соединительной ткани дермы, при длительной инфекции сопровождается разрушением базальной мембраны. Также нами отмечено, что вследствие гибели кератиноцитов базального слоя и в отсутствие дифференцировки и специализации клеток эпидермиса, сохраняется только зернистый, блестящий и роговой слои (рис. 1, а-г).
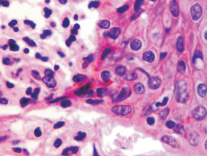
При наличии инфильтрации поверхность эпидермиса может быть сохранена, идентифицируется слой ороговевающих клеток, блестящий слой и слой зернистых клеток; под ними – инфильтрат. Клетки инфильтрата активно пролиферируют, видны фигуры амитозов, полицентрических митозов, а также клетки с двумя ядрами в цитоплазме (рис. 1, в), клетки с гантелеобразной неправильной формой ядра.
Нами отмечено, что клетки инфильтрата в зоне разрушенных кератиноцитов имеют ярко-базофильные ядра, наблюдаются не только многочисленные фигуры митозов и амитозов, но и полицентрические митозы. Это говорит о том, что в зоне гибели клеток с утратой обычных контактных информационных сигналов для торможения пролиферативной активности, в отсутствие условий для дифференцировки и специализации, под воздействием сигналов гибнущих кератиноцитов, лейкоциты устремляются в зону драматических для тканей кожи событий. Их миграция направлена на закрытие дефекта кожи без последующего выполнения защитных и барьерных функций кератиноцитов. При этом часть клеток соединительной ткани фибробластного дифферона также мигрирует в зону повреждения кожи. Благодаря их секреторной активности формируется нежная волокнистая коллагеновая сеть, которая не выполняет функций защиты, аналогичной разрушенным кератиноцитам (рис. 2).
а 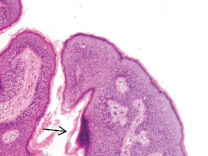 б
б 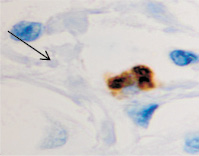
 г
г 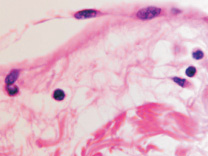
Рис. 1. Формирование инфильтрата (а, в, г) из делящихся клеток крови в коже при поражении HPV инфекцией; организация ткани опухоли (г); черной стрелкой указана фибробластоподобная клетка. Окраска а, в, г – гематоксилин-эозином; б – иммунная гистохимия. Микрофото. Ув. а – х100; б, в, г – х400; а – стрелкой указан очаг некроза в эпидермисе; в – лейкоцитарный инфильтрат при увеличении х400; базальная мембрана отсутствует, в основании инфильтрата крупные клетки с гигантскими гиперхромными ядрами
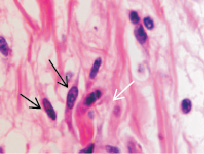
Рис. 2. Зона разрушенной базальной мембраны в коже человека, повреждённой HPV. Окраска гематоксилин-эозином. Микрофото. Ув. х 400. Фибробластоподобные клетки указаны чёрными стрелками, волокна – белыми стрелками
Учитывая тропность HPV к камбиальным клеткам эпидермиса, можно сделать вывод о том, что регенераторный потенциал стволовых кератиноцитов истощён, а также прекращена выработка кератиноцитами индукторов для созревания поступающих молодых недифференцированных лимфоцитов. Таким образом, можно сделать вывод, что формирующийся инфильтрат в дерме и эпидермисе кожи представлен клетками лейкоцитарного пула крови, поступившими из кровеносного русла кожи гематогенным путём. В месте формирования патологического процесса базальных стволовых кератиноцитов нет, базальная мембрана, производное этих клеток и прилежащих структур соединительной ткани соответственно отсутствует. Поэтому нами сделан вывод о том, что, возможно, гибнущие камбиальные клетки могли дать сигнал специфическими цитокинами к миграции молодых недифференцированных клеток крови в зону повреждения кожи для закрытия дефекта, но без выполнения функции разрушенных HPV-структур. Дифференцировка этих клеток в новых условиях контактных взаимодействий отсутствует, им присуща только высокая пролиферация – как адаптация на повреждающее влияние HPV, которая возможна, но в режиме бесконтрольного деления. Наши данные согласуются с данными Susman S., Tomuleasa C., Soritau O., Mihu C., Rus-Ciuca D., Sabourin J.C., Bibeau F., Irimie A., Buiga R. (2012), выявившими при развитии опухоли инфильтрацию лейкоцитами слизистой оболочки толстой кишки [23]. Эти авторы предположили, что вследствие инфильтрации развиваются генные мутации в эпителиоцитах, которые ведут к перестройке камбиальных клеток ткани слизистой оболочки кишки.
Borowicz K. Walczak L. (1990) подчёркивают важность морфологических исследований для подтверждения HPV в структурах различных систем организма [16]. На основе молекулярно-генетических исследований признано, что стойкая HPV-инфекция является центральным фактором риска для развития HPV-ассоциированной неоплазии. При этом авторы утверждают, что продолжение экспрессии вирусных E6 и E7 онкогенов разрушает механизмы контроля клеточного цикла в инфицированных клетках, тем самым приобретается безграничный пролиферативный потенциал и возникает сопротивление против апоптоз-индуцирующих сигналов. Последующее приобретение мутаций и геномной нестабильности может привести к злокачественной трансформации в этих клетках. Но ни один автор, изучающий механизмы онкогенеза, не ответил на вопрос о сущности пролиферативной активности перед карциногенезом. Необходимыми условиями для возникновения рака являются нарушения клеточного обновления – метаплазия или атрофия структур, создающие предпосылки для дисплазии эпителия – практически облигатного предракового состояния. Метаплазия, атрофия и рак – звенья одной цепи, в которой инициирующую роль играет микроорганизм; в ответ на инвазию у человека развивается хронический воспалительный процесс в структурах организма, сопровождающийся инфильтрацией, дисрегенераторными изменениями эпителия, создающими, в свою очередь, фон для развития рака, связанный с гибелью собственного камбия и заселением зоны гибели инфильтратом крови [31]. Действительно, сведений, достоверно подтверждающих синтез или секрецию HPV-мутагенных или канцерогенных субстанций нет. Поэтому современные представления состоят в том, что микроорганизмы скорее действуют в качестве промотора, чем инициатора канцерогенеза. При инфицировании микроорганизмами возникает воспалительная инфильтрация кожи, наблюдается продукция нейтрофильными лейкоцитами реактивных кислородных метаболитов и происходит высвобождение цитокинов клетками воспалительного инфильтрата, что приводит не к повреждению ДНК, а стимуляции пролиферации клеток.
Иммунологическая функция кератиноцитов при этом, очевидно, также нарушается, так как она, по данным Baeck M. et.al., (2013), реализуется за счёт того, что кератиноциты в постнатальномонтогенезе секретируют эпидермальный фактор дифференцировки лимфоцитов (ELDIF), ингибирующий пролиферацию и стимулирующий дифференцировку, специализацию и созревание в целом лимфоцитов, что подтверждает наши выводы о невозможности клеток инфильтрата крови выполнить барьерные функции в условиях отсутствия дифференцировки. Истощение CD68 в невоспалительных папилломах при ВПЧ ассоциируется с повышением пролиферации эпителия эпидермиса, затем снижением дифференцировки кератиноцитов, гибелью камбия, разрушением базальной мембраны, инфильтрацией зоны повреждения эпидермиса с последующим снижением дифференцировки мигрирующих лейкоцитов, что ведёт к канцерогенезу.
Сформулированная в начале 80-х гг. XX века концепция лимфоидной ткани кожи – skin-associated lymphoid tissue (SALT), продолжая развиваться на современном этапе, пополнила представления об иммунной системе кожи, включая в неё нейтрофилы, тучные клетки и эозинофилы, клетки Лангерганса или дендритные клетки Штейнмана и кератиноциты [1]. В cоединительной ткани кожи человека при HPV-инфекции нарушение хода физиологической регенерации и появление разрастаний в виде бородавок и кондилом связано с нарушением антигенпрезентации CD68, их расположением в подлежащей эпителию соединительной ткани на фоне полного их отсутствия в эпителиальных пластах.
Особенности распределения эффекторных иммуноцитов CD68 при HPV свидетельствуют о нарушении антигенпредставления в структурах кожи человека и последующем снижении контроля за физиологической и репаративной регенерацией в целом, что может привести к извращению клеточных взаимодействий в системе эффекторных иммуноцитов и запуску процесса онкогенеза в структурах кожи. Одной из причин нарушения является то, что кератиноциты в постнатальномонтогенезе секретируют эпидермальный фактор дифференцировки лимфоцитов (ELDIF), ингибирующий пролиферацию и стимулирующий дифференцировку, специализацию и созревание в целом лимфоцитов [12].
По нашим данным, канцерогенез в структурах кожи можно представить начинающимся с повреждения HPV-инфекцией кератиноцитов с последующим адаптивным повышением их пролиферативной активности для сохранения барьерных свойств эпителия. Высокая скорость пролиферации, отсутствие соответствия дифференцировки и специализации клеток дифферонакератиноцитов приводят к истощению регенераторного потенциала стволовых кератиноцитов. За пролиферацией следует антигенпредставление повреждённых клеток с вирусными контаминатами и с сопровождением макрофагальной инфильтрации эффекторными клетками, способными к фагоцитозу. Истощение регенераторного потенциала эпителиального камбия и хроническая инфильтрация лейкоцитами соединительной ткани, последующий выход лейкоцитов в эпидермальные слои приводит к исчезновению клеточного пула кератиноцитов и извращению взаимодействия эффекторных иммуноцитов. Секреторная активность клеток, ответственных за синтез, структуру и функцию базальной мембраны падает и исчезает, сопровождаясь разрушением базальной мембраны. Так как локальный регенераторный потенциал исчерпан и сохраняются только клетки, успевшие пройти дифференцировку, поверхность кожи в зоне контаминации HPV может иметь некоторое время признаки неповреждённой, но под блестящим слоем формируется воспалительный инфильтрат, который по составу отличается от инфильтрата в начале процесса вирусной контаминации. Место повреждённого эпидермиса занимают не клетки камбия кератиноцитов, а лимфоциты.
Выводы
1. Процесс апоптоза при HPV происходит тотально, затрагивая шиповатый слой и камбиальный. Разрушается базальная мембрана, прекращается дифференцировка клеток ткани. Исчезают факторы дифференцировки лимфоцитов.
2. Механизм разрастания эпидермиса с прилежащей к нему соединительной тканью сосочкового и сетчатого слоёв дермы связан с отсутствием иммуноцитов CD68 в эпидермисе кожи, скоплением их в прилежащей к базальной мембране пластинке соединительной ткани.
3. Перераспределение эффекторных иммуноцитов CD68 может служить индуктором для дисбаланса в системе кейлоны-некрогормоны, что является пусковым фактором для разрастания не только поверхностного эпителия, но и прилежащей к нему соединительной ткани.
4. Извращение антигенпредставления в соединительной ткани приводит к увеличению количества фибробластов, продуцирующих межклеточное вещество, что приводит к нерегулируемому разрастанию соединительной ткани и нарушению взаимодействия эпителиально-мезенхимных производных.
5. Повышение пролиферации кератиноцитов, атрофия камбиальных слоёв эпидермиса, инфильтрация клетками крови зоны повреждения, перераспределение CD68 в соединительную ткань являются начальными этапами канцерогенеза в коже на фоне HPV.
Работа выполнена при поддержке Научного фонда ДВФУ и Международного гранта ДВФУ (соглашение № 13-09-0602-м_а от 6 ноября 2013 г.
Рецензенты:
Храмова И.А., д.м.н., профессор, врач акушер-гинеколог, Приморский краевой диагностический центр, г. Владивосток;
Шульгина Л.В., д.б.н., профессор, заведующая лабораторией микробиологии ФГУП «ТИНРО-Центр», г. Владивосток.
Работа поступила в редакцию 16.12.2013.
Библиографическая ссылка
Рева И.В., Рева И.В., Рева Г.В., Ямамото Т., Ямамото Т., Толмачёв В.Е., Усов В.В., Болотная В.Н. РОЛЬ АНТИГЕНПРЕЗЕНТИРУЮЩИХ КЛЕТОК CD68 В КАНЦЕРОГЕНЕЗЕ HPV-АССОЦИИРОВАННОЙ ЭТИОЛОГИИ // Фундаментальные исследования. 2013. № 12-2. С. 306-313;URL: https://fundamental-research.ru/en/article/view?id=33326 (дата обращения: 27.04.2026).



