Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
ROLE OF ENTEROBACTERIACEAE FAMILY MICROORGANISMS IN ETIOLOGY OF WOUND BURN INFECTION
Раневая инфекция у пострадавших с термической травмой представляет собой одну из главных составляющих патогенеза ожоговой болезни и является серьезной проблемой в комбустиологии. Проведение рациональной антибактериальной терапии при этом невозможно без современных знаний об этиологической структуре раневой ожоговой инфекции и антибиотикорезистентности ее возбудителей. Раневая ожоговая инфекция отличается полиэтиологичностью. Результаты многочисленных исследований свидетельствуют, что первое место в структуре выделенных микроорганизмов традиционно принадлежит стафилококкам, второе место прочно занимают неферментирующие грамотрицательные бактерии [5]. Наряду с уже известными «проблемными» возбудителями инфекции у обожженных, такими как стафилококк, ацинетобактерии и синегнойная палочка, в настоящее время возрастает значение и других антибиотикорезистентных микроорганизмов, в частности, энтеробактерий. В литературе отсутствуют данные о значении энтеробактерий в этиологии раневой ожоговой инфекции. В этой связи нами проведено исследование, целью которого было изучение роли энтеробактерий в этиологии раневой ожоговой инфекции и определение молекулярных особенностей антибиотикорезистентных штаммов.
В задачи исследования входили анализ частоты обнаружения энтеробактерий, определение их видового спектра, изучение антибиотикорезистентности выделенных штаммов и детекция β-лактамазы расширенного спектра в отделениях термической травмы ФГБУ ННИИТО Минздрава России за 2010–2013 годы.
Материалы и методы исследования
В задачи исследования входили анализ частоты обнаружения энтеробактерий, определение их видового спектра, изучение антибиотикорезистентности выделенных штаммов и детекция β-лактамаз расширенного спектра в отделениях термической травмы ФГБУ ННИИТО Минздрава России за 2010–2013 годы.
Видовая идентификация микроорганизмов проводилась на анализаторе iEMS Reader FM (Labsystems, Финляндия) с помощью коммерческих тест-систем (Lachema, Чехия). Антибиотикорезистентность оценивалась диско-диффузионным методом на агаре Мюллера‒Хинтон (BD) с помощью сенси-дисков (Oxoid, Англия) в соответствии с методическими указаниями 4.2.1890-04 [3]. Минимальные подавляющие концентрации (МПК) препаратов определялись на анализаторе ADAGIO (Bio-Rad, США). С 2012 года энтеробактерии тестировали на предмет продукции бета-лактамаз расширенного спектра (БЛРС). Детекцию БЛРС проводили с помощью Е-тестов с цефтазидимом и цефтазидимом/клавуланатом (BioMerieux, Франция) по инструкции. Для сравнения зоны задержки роста использовали штамм E.coli АТСС 25922, не продуцирующий бета-лактамазы и штамм E.coli АТСС 700603, продуцирующий БЛРС.
Результаты исследования и их обсуждение
Выделенные в анализируемый период бактерии семейства Enterobacteriaceae составили 359 штаммов. Удельный вес энтеробактерий в спектре других возбудителей раневой ожоговой инфекции относительно небольшой, вместе с тем прослеживается тенденция к его увеличению в 2013 году (рис. 1). Кроме того, абсолютное количество раневых энтеробактерий выросло в 5,1 раза (рис. 2).
Структура выделенных у пациентов с ожоговой инфекцией энтеробактерий отличается многообразием, среди них присутствуют Klebsiella sp., E.coli, Enterobacter sp., Citrobacter sp., Proteus sp. Лидирующее положение принадлежит бактериям рода Klebsiella, число которых выросло за период наблюдения в 11,2 раза и составило 47,2 % от всех энтеробактерий (рис. 3). Количество штаммов E.coli увеличилось в два раза, это 9,8 % представителей семейства Enterobacteriaceae, другие представители выделялись еще реже. Анализ видового состава микроорганизмов показал, что 89 % всех клебсиелл составляет Klebsiella pneumoniae. Участие Klebsiella pneumoniae в развитии инфекций в хирургических стационарах и отделениях реанимации и интенсивной терапии обсуждается в научной литературе уже много лет [2]. Для ожоговых стационаров эта ситуация ранее не была актуальной, однако к настоящему времени раневая ожоговая инфекция, вызванная K. рneumoniae, становится самостоятельной проблемой не только в силу увеличения частоты обнаружения, но и нарастания антибиотикорезистентности K. рneumoniae (рис. 4).
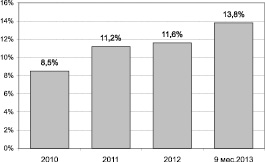
Рис. 1. Удельный вес энтеробактерий в структуре возбудителей раневой ожоговой микрофлоры
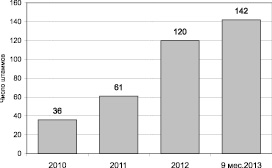
Рис. 2. Число штаммов энтеробактерий из раневого отделяемого пациентов с термической травмой

Рис. 3. Доля Klebsiella sp. cреди раневых бактерий рода Enterobacteriaceae в ожоговом стационаре
Основные проблемы резистентности энтеробактерий связаны с выработкой бета-лактамаз расширенного спектра – ферментов, способных разрушать различные β-лактамные антибиотики. На сегодняшний день известно большое количество хромосомных и плазмидных β-лактамаз, разрушающих цефалоспорины I-IV поколений и азтреонам [4].
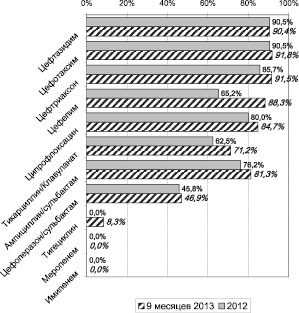
Рис. 4. Резистентность Klebsiella pneumoniae, выделенных у пациентов с термической травмой в 2012–2013 гг.
Анализ продукции бета-лактамаз расширенного спектра у раневых клебсиелл, выделенных у пациентов с тяжелой термической травмой, показал, что в 2011 году 62,5 % штаммов были продуцентами БЛРС, в 2012 году – 89,7 % штаммов, а за 9 месяцев 2013 года – 91,8 %. Детекция БЛРС существенно затрудняется при наличии у микроорганизмов нескольких детерминант резистентности. Так, например, продукция хромосомных бета-лактамаз класса С обусловливает устойчивость микроорганизмов к клавуланату, маскируя при этом присутствие БЛРС [7]. Но даже без учета таких штаммов фенотип резистентности и количество явных продуцентов бета-лактамаз расширенного спектра свидетельствуют о том, что резистентные энтеробактерии становятся самостоятельной проблемой в лечении пострадавших с тяжелой термической травмой.
На практике крайне важно, что устойчивость штаммов Klebsiella pneumoniae – продуцентов БЛРС часто ассоциируется с устойчивостью к аминогликозидам и фторхинолонам [6]. Клиническую эффективность в отношении этих микроорганизмов могут сохранять ингибиторзащищенные бета-лактамы. Изучение резистентности БЛРС-продуцирующих штаммов к различным антибиотикам β-лактамного ряда доказывает, что большинство штаммов, устойчивых к цефоперазон/сульбактаму, проявляют высокую резистеность к ингибиторзащищенным пенициллинам. Вместе с тем большое число штаммов, не чувствительных к тикарциллин/клавуланату и ампициллин/сульбактаму, сохраняют чувствительность к цефоперазон/сульбактаму (рис. 4). Однако наиболее надежными являются карбапенемы, отличающиеся высокой активностью в отношении большинства β-лактамаз. В то же время широкое использование карбапенемов в качестве средств эмпирической терапии опасно в плане селекции микроорганизмов, продуцирующих карбапенемазы.
Использование цефепима в настоящее время не может рассматриваться как возможный вариант антибактериальной терапии инфекций, вызванных энтеробактериями, в силу широкого распространения СТХ-М β-лактамаз, обусловливающих устойчивость ко всем цефалоспоринам, включая препараты IV поколения [1]. Повышение резистентности клебсиелл к цефепиму с 65,2 % в 2012 г. до 88,3 % в 2013 г. в ожоговом стационаре является тому подтверждением.
Таким образом, в последние годы среди возбудителей раневой ожоговой инфекции наблюдается увеличение частоты обнаружения микроорганизмов семейства Enterobacteriaceae. В спектре энтеробактерий лидирующее место занимает K. рneumoniae. Более 90 % выделенных клебсиелл не чувствительны к цефалоспоринам, практически все они продуцируют бета-лактамазы расширенного спектра. Антимикробные препараты для эмпирической стартовой терапии раневой инфекции в отделениях термической травмы должны назначаться на основе протоколов определения видового состава циркулирующей микрофлоры в определенный промежуток времени, данных о распространении антибиотикорезистентных возбудителей инфекции, а также тщательном анализе причин резистентности.
Рецензенты:
Королев С.Б., д.м.н., профессор, заведующий кафедрой травматологии, ортопедии и военно-полевой хирургии им. М.В. Колокольцева, ГБОУ ВПО НижГМА Минздрава России, г. Нижний Новгород;
Никифоров В.А., д.м.н., профессор, зав. лабораторией микробиологии, ФБУН ННИИЭМ им. акад. И.Н. Блохиной Роспотребнадзора, г. Нижний Новгород.
Работа поступила в редакцию 16.12.2013.
Библиографическая ссылка
Гординская Н.А., Сабирова Е.В., Абрамова Н.В., Дударева Е.В., Некаева Е.С. ЗНАЧЕНИЕ МИКРООРГАНИЗМОВ СЕМЕЙСТВА ENTEROBACTERIACEAE В ЭТИОЛОГИИ РАНЕВОЙ ОЖОГОВОЙ ИНФЕКЦИИ // Фундаментальные исследования. 2013. № 12-2. С. 191-194;URL: https://fundamental-research.ru/en/article/view?id=33302 (дата обращения: 14.05.2026).



