Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
THERMODYNAMIC CALCULATION OF THE IMPACT ON THE SYSTEM FE2O3 CONSISTING OF LIMESTONE AND FELSITES
Снижение потребления топлива на обжиг клинкера является актуальной задачей. Существует несколько способов снижения затрат на обжиг клинкера. Во-первых, снизить затраты на испарение воды путем перехода с мокрого на сухой способ производства портландцемента; во-вторых, применяя нетрадиционный алюмосиликатный и железосодержащий сырьевой материал, обладающий более низкой температурой размягчения и плавления. В данной статье более подробно остановимся на рассмотрении последнего способа снижения затрат на обжиг.
В этой статье в качестве глинистого компонента рассмотрена горная порода Среднего Урала ‒ фельзит. Замена глинистого компонента на фельзит позволяет снизить температуру обжига клинкера до 1250–1300 °С.
Целью данной статьи является изучение при помощи термодинамических расчетов возможности применения фельзита в качестве глинистого компонента сырьевой смеси для производства портландцементного клинкера (система CaCO3–CaO-фельзит) и изучение влияния корректирующей добавки Fe2O3 на систему CaCO3–CaO-фельзит.
Сначала рассмотрим возможность применения фельзита в качестве алюмосиликатного и железосодержащего компонента сырьевой смеси для производства портландцементного клинкера, т.е. систему, состоящую из CaCO3–CaO-фельзит.
Для того чтобы узнать возможность протекания реакций фельзита с известняком с целью получения традиционных клинкерных минералов, были проведены термодинамические расчеты. Свободная энергия Гиббса рассчитывалась по стандартной методике [1, 2, 3].
Для термодинамических расчетов в данной статье использовались материалы, представленные в табл. 1. Анализ химического состава показывает, что фельзит относится к кислой горной породе с содержанием диоксида кремния 78,98 % и оксида кальция 1,33 %. Горная порода фельзит имеет низкую температуру образования расплава 1120 °С.
Таблица 1
Химический состав исходных материалов
|
Материал |
Содержание оксидов, % масс. |
||||||
|
SiO2 |
Al2O3 |
Na2O |
K2O |
Fe2O3 |
CaO |
Dmпрк |
|
|
Фельзит |
78,98 |
11,57 |
2,10 |
3,91 |
1,60 |
1,33 |
0,51 |
|
Известняк |
0,69 |
1,15 |
– |
– |
0,52 |
54,00 |
42,95 |
Легкоплавкость фельзиту придают щелочные и щелочноземельные оксиды: K2O, Na2O, CaO и трехвалентный оксид железа [4, 5].
Расчетный минералогический состав фельзита представлен следующими минералами: 47,24 % кварц; 17,73 % Na2O·AL2O3·6SiO2; 23,13 % K2O·AL2O3·6SiO2; 3,69 % AL2O3·2SiO2·2H2O; 1,6 Fe2O3; 6,61 % CaO·AL2O3·2SiO2.
При взаимодействии фельзита с известняком возможно получить следующие продукты реакции, такие как алит (3CaO·SiO2), белит (2CaO·SiO2), алюминат кальция (3CaO·AL2O3), браунмиллерит (4CaO·AL2O3·Fe2O3), K2O·SiO2, Na2O·SiO2, CO2, H2O в разных пропорциях. При исследовании системы известняк – фельзит можно получить разнообразный минералогический состав клинкера, меняя соотношение исходных компонентов.
Коэффициенты уравнения реакции взаимодействия фельзита с известняком были посчитаны по формуле (1), где n – количество вещества, моль; m – масса вещества, г; M – молярная масса, г/моль.
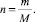 (1)
(1)
Реакцию взаимодействия известняка с фельзитом можно записать в виде, представленном формулой (2). Поскольку неизвестно, сколько будет образовано алита и белита из 1,24065SiO2, введем коэффициенты реакции y и х = 1 – y, которые будут показывать сколько кварца израсходуется на образование алита, а сколько на образование белита соответственно.
(0,32679 + 2,4813·x + 3,72195·y)CaCO3 + 0,03383Na2O·AL2O3·6SiO2 + + 0,0416K2O·AL2O3·6SiO2 + 0,0143AL2O3·2SiO2·2H2O + 0,01Fe2O3 + + 0,0238CaO·AL2O3·2SiO2 + 0,7873SiO2 → 0,01(4CaO·AL2O3·Fe2O3) + + 0,10353(3CaO·AL2O3) + 1,24065(x(2CaO·SiO2) + y(3CaO·SiO2)) + +0,0416(K2O·SiO2) + 0,03383(Na2O·SiO2) + 0,0286H2O↑ + + (0,32679 + 2,4813·x + 3,72195·y)CO2↑ (2)
Результаты расчета минералогического состава и коэффициента насыщения (КН) по реакции, приведенной выше, представлены в табл. 2. Коэффициент насыщения был рассчитан по минералогическому составу (см. формулу (3)) [6].
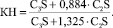 (3)
(3)
Проанализировав табл. 2, можно сделать вывод, что фельзит теоретически может полностью связать в клинкерные минералы от 73,74 до 80,19 % известняка, при избытке известняка (больше 80,19 %) в клинкере будет оставаться свободная известь, при недостатке известняка (меньше 73,74 %) в клинкере будет оставаться кварц и другие минералы фельзита.
Таблица 2
Расчетный фазовый состав и коэффициент насыщения реакций
|
Номер реакции |
Коэффициенты реакции |
Исходные вещества, % масс |
Продукты реакции (по расчету), % масс |
КН |
|||||||
|
y |
x |
Известняк |
Фельзит |
C4AF |
C3A |
C2S |
C3S |
K2O·SiO2 |
Na2O·SiO2 |
||
|
1 |
0 |
1 |
73,74 |
26,26 |
1,89 |
10,89 |
83,12 |
0,00 |
2,50 |
1,61 |
0,67 |
|
2 |
0,7 |
0,3 |
78,62 |
21,38 |
1,59 |
9,15 |
20,96 |
64,84 |
2,10 |
1,35 |
0,90 |
|
3 |
1 |
0 |
80,19 |
19,81 |
1,49 |
8,57 |
0,00 |
86,71 |
1,96 |
1,27 |
1,00 |
Результаты расчета свободной энергии Гиббса для системы CaCO3–CaO-фельзит представлены на рис. 1. Выше температуры 1211,61 K использовались данные для системы CaO-фельзит.
Анализ результатов термодинамического расчета показывает, что начало протекания реакций взаимодействия известняка с фельзитом возможно выше температуры, K: 789,44; 892,55 и 923,88 для реакции 1; 2 и 3 соответственно. Термодинамический анализ реакции показывает, что с уменьшением количества минералов плавней (С3A, C4AF) и щелочных минералов (K2O·SiO2, Na2O·SiO2) в клинкере температура возможности протекания реакции возрастает с 789,44 до 923,88 K. Таким образом, доказана возможность применения фельзита в качестве глинистого компонента для производства портландцементного клинкера.
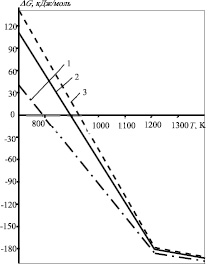
Рис. 1. Зависимость свободной энергии Гиббса в системе CaCO3–CaO-фельзит от температуры (номера кривых соответствуют номерам реакций, указанных в табл. 2)
Поскольку фельзит имеет более низкое количество Fe2O3 = 1,60 %, чем в традиционном глинистом сырье используемом для производства портландцементного клинкера, то требуется ввести дополнительно железосодержащий компонент. В качестве корректирующей добавки был выбран химически чистый Fe2O3 для упрощения термодинамических расчетов.
Далее в статье будет рассмотрена возможность применения корректирующей добавки Fe2O3 для системы CaCO3–CaO-фельзит.
Гипроцемент для производства портландцементного клинкера рекомендует использовать в смеси с коэффициентом насыщения кремнезема известью равным 0,90, поэтому для дальнейших термодинамических расчетов в качестве базового состава примем смесь, состоящую из 78,62 % известняка и 21,38 % фельзита [6]. Реакцию взаимодействия 78,62 % известняка и 21,38 % фельзита без введения Fe2O3 была подробно рассмотрена выше (см. в табл. 2 реакцию 2 и рис. 1 реакцию 2). Базовый состав с коэффициентом насыщения, равным 0,90, имеет повышенный глиноземистый (p) и силикатный (n) модуль. Введение трехвалентного оксида железа в сырьевую смесь для производства портландцемента из известняка и фельзита позволяет снизить модульные характеристики (глиноземистый и силикатный модуль) до рекомендуемых величин.
К базовому составу будем добавлять трехвалентный оксид железа до полного усвоения AL2O3 в браунмиллерит.
Для полного усвоения оксида алюминия в C4AF потребуется ((0,10353 + 0,01)Fe2O3). Для упрощения расчетов введем коэффициент Z от 0 до 1, который будет показывать, сколько из 0,10353AL2O3 уйдет на образование C4AF. На образование C3A уйдет (0,10353-0,10353·z)AL2O3, т.е. при z = 1 весь AL2O3 будет связан в C4AF. Тогда реакцию взаимодействия базового состава с трехвалентным оксидом железа можно записать следующим образом (см. формулу (4)) (коэффициенты реакции посчитаны по формуле (1)):
(0,03383Na2O·AL2O3·6SiO2 + 0,0416K2O·AL2O3·6SiO2 + + 0,0143AL2O3·2SiO2·2H2O + 0,01Fe2O3 + 0,0238CaO·AL2O3·2SiO2 + 0,7873SiO2) + + (3,676545 + 0,10353·z)CaCO3 + (0,10353·z·Fe2O3) → → (0,01 + 0,10353·z)(4CaO·AL2O3·Fe2O3) + (0,10353 – 0,10353·z)(3CaO·AL2O3) + + 0,372195(2CaO·SiO2) + 0,868455(3CaO·SiO2) + 0,0416(K2O·SiO2) + + 0,03383(Na2O·SiO2) + 0,0286H2O↑ + (3,676545 + 0,10353·z)CO2↑ (4)
Результаты расчета модульных характеристик и минералогического состава реакции взаимодействия Fe2O3 с известняком и фельзитом представлены в табл. 3 (для всех реакций КН = 0,90). Силикатные и глиноземистый модуль был рассчитан с помощью (5) и (6) [6].
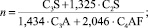 (5)
(5)
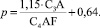 (6)
(6)
Таблица 3
Расчетный фазовый состав и силикатный и глиноземистый модуль реакций
|
Номер реакции |
Коэффициент реакции z |
Исходные вещества, % масс |
Продукты реакции (по расчету), % масс |
n |
p |
|||||||
|
Известняк |
Фельзит |
Fe2O3 |
C4AF |
C3A |
C2S |
C3S |
K2O·SiO2 |
Na2O·SiO2 |
||||
|
2 |
0 |
78,62 |
21,38 |
0 |
1,59 |
9,15 |
20,96 |
64,84 |
2,10 |
1,35 |
5,65 |
7,25 |
|
4 |
0,49 |
77,51 |
20,80 |
1,69 |
9,33 |
4,51 |
20,24 |
62,59 |
2,02 |
1,31 |
3,50 |
1,20 |
|
5 |
0,6 |
77,28 |
20,67 |
2,05 |
10,99 |
3,51 |
20,08 |
62,11 |
2,01 |
1,30 |
3,22 |
1,00 |
|
6 |
1 |
76,43 |
20,22 |
3,35 |
16,83 |
0 |
19,53 |
60,42 |
1,96 |
1,26 |
2,50 |
0,64 |
Проанализировав табл. 3, можно сделать вывод, что для полного усвоения AL2O3 в браунмиллерит потребуется добавить к базовому составу 3,35 % Fe2O3. При добавлении к базовому составу больше 3,35 % Fe2O3 в клинкере будет появляться двухкальциевый феррит 2CaO·Fe2O3.
Результаты расчета свободной энергии Гиббса системы CaCO3–CaO-фельзит–Fe2O3 представлены на рис. 2. Выше температуры 1211,61K использовались данные для системы CaO-фельзит-Fe2O3. Анализ результатов термодинамического расчета показывает, что начало протекания реакций взаимодействия известняка с фельзитом с добавлением Fe2O3 от 0 до 3,35 % возможно выше температуры, K:892,55; 838,74; 826,59 и 782,36 для реакции 2; 4, 5 и 6 соответственно. Термодинамический анализ реакции показывает, что с увеличением количества корректирующей добавки Fe2O3 (от 0 до 3,35 %) температура возможности протекания реакции уменьшается с 892,55 до 782,36 K, а количество минерала плавня браунмиллерита возросло с 1,59 % (реакция 2) до 16,83 % (реакция 6).
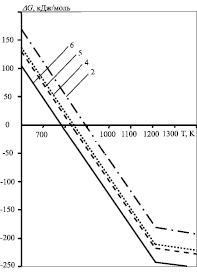
Рис. 2. Зависимость свободной энергии Гиббса в системе CaCO3–CaO-фельзит–Fe2O3 от температуры (номера кривых соответствуют номерам реакций, указанных в табл. 3)
По результатам проведенных расчетов можно сделать вывод, что наиболее оптимальным составом является состав, содержащий 77,28 % известняка, 20,67 % фельзита и 2,05 % Fe2O3 (реакция 5) с температурой начала реакции выше 826,59 K. Также удалось доказать возможность применения фельзита в качестве перспективного глинистого компонента сырьевой смеси для производства портландцементного клинкера при пониженных температурах обжига. Кроме того, была доказана возможность применения Fe2O3 в качестве корректирующей добавки сырьевой смеси для снижения силикатного и глиноземистого модулей в двухкомпонентной смеси, состоящей из фельзита и известняка.
Рецензенты:
Дерябин В.А., д.т.н., профессор, зав. кафедрой «Технологии стекла» Института материаловедения и металлургии, ФГАОУ ВПО «УрФУ имени первого Президента России Б.Н. Ельцина», г. Екатеринбург;
Кащеев И.Д., д.т.н., профессор, зав. кафедрой «Химическая технология керамики и огнеупоров» Института материаловедения и металлургии, ФГАОУ ВПО «УрФУ имени первого Президента России Б.Н. Ельцина», г. Екатеринбург.
Работа поступила в редакцию 25.12.2013.
Библиографическая ссылка
Гаврилюк М.Н., Семериков И.С. ТЕРМОДИНАМИЧЕСКИЕ РАСЧЕТЫ ВЛИЯНИЯ Fe2O3 НА СИСТЕМУ, СОСТОЯЩУЮ ИЗ ИЗВЕСТНЯКА И ФЕЛЬЗИТА // Фундаментальные исследования. 2013. № 11-6. С. 1167-1171;URL: https://fundamental-research.ru/en/article/view?id=33270 (дата обращения: 24.05.2026).



