Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
PECULIARITIES OF DIAGNOSTICS AND TREATMENT OF EXTRAHEPATIC PORTAL HYPERTENSION
Под термином «портальная гипертензия» (ПГ) подразумевается повышение давления в воротной вене (ВВ) из-за обструкции кровотока на любом ее участке. По данным Ш. Шерлок, Дж. Дули (1999), портальная гипертензия делится на 2 группы:
1) пресинусоидальную (внепеченочная или внутрипеченочная);
2) печеночную (внутрипеченочная и постсинусоидальная).
В основе такого деления лежат патологические процессы, не приводящие к печеночной недостаточности при пресинусоидальной ПГ и приводящие к печеночной недостаточности при печеночной ПГ [10].
В отечественной литературе (М.Д. Пациора, 1974), исходя из градиента между давлением заклинивания печёночных вен и портальным венозным давлением, принято различать
1) подпечёночную;
2) внутрипечёночную;
3) надпечёночную;
4) смешанную ПГ [2,11].
Причиной подпеченочной ПГ могут служить гнойно-воспалительные заболевания брюшной полости (8 %) (омфалит после катетеризации пупочной вены у детей, острый аппендицит, перитонит, пилефлебит, сепсис); травмы, миелопролиферативные заболевания, забрюшинный фиброз, болезнь Ходжкина, опухоли забрюшинного пространства (17 %); ятрогенные повреждения, в том числе абдоминальные операции, трансплантация поджелудочной железы (8–23 %); артериовенозные фистулы селезенки (1 %), аневризма селезеночной артерии, врожденные аномалии развития, прием пероральных контрацептивов [8, 9, 10, 11].
Гемодинамические нарушения по левостороннему типу развиваются примерно в 5–7 % случаев внепеченочной ПГ. Изолированная обструкция селезёночной вены (СВ) вызывает левостороннюю портальную гипертензию. Особенно большое значение имеют заболевания поджелудочной железы: панкреатиты (39–65 %), хронические панкреатиты в сочетании с псевдокистами поджелудочной железы (14–33 %), доброкачественные и злокачественные опухоли (4–35 %) [9]. Надпеченочная ПГ обусловлена нарушением оттока крови от печени по печеночным венам вследствие их сужения или непроходимости (синдромом Бадда‒Киари). Синдром может развиться у пациентов с системной красной волчанкой, идиопатическим гранулематозным васкулитом, пароксизмальной ночной гемоглобинурией, при недостаточночности естественных антикоагулянтов, болезни Бехчета, при приеме пероральных контрацептивов, беременности, травме, злокачественных опухолях почки, надпочечника, инвазивном росте опухоли печени, при лейомиосаркоме печеночных вен, при метастазах рака яичка в правое предсердие, при метастазировании опухоли Вильмса, у больных с соединительнотканными мембранами в просвете нижней полой вены [1].
Смешанный тип ПГ обусловлен сочетанием нескольких факторов, определяющих блок воротной вены. Так, при циррозе печени, гепатоцеллюлярной карциноме возможен тромбоз воротной вены [6,11], узловая трансформация печени может вызвать синдром Бадда‒Киари, причем функция гепатоцитов при данном редком заболевании не страдает [10], врожденная патология (гипоплазия печеночных вен) может сочетаться с тромбозом воротной вены или циррозом печени.
Появление синдрома ПГ имеет чрезвычайно важное значение в течение заболевания. Являясь приспособительным явлением в начале заболевания, ПГ с прогрессированием процесса приобретает роль ведущего патогенетического клинического фактора. Основные проявления внепеченочной ПГ – это массивные пищеводно-желудочные кровотечения, спленомегалия с явлениями гиперспленизма, повышение объема крови в органах, склонность больных к эрозивно-язвенным поражениям верхних отделов желудочно-кишечного тракта [3, 7]. Самым грозным проявлением является кровотечение из варикозно-расширенных вен пищевода и желудка [5].
Целью нашего исследования является определение оптимальной схемы обследования больных с внепеченочной портальной гипертензией путем применения современных методик для выбора хирургического пособия конкретно в каждом случае заболевания.
Материалы и методы исследования
Из 341 больного, пролеченного в хирургической клинике ГБОУ ВПО РостГМУ Минздрава РФ с 1997 года по настоящее время, внепеченочная (подпеченочная) портальная гипертензия развилась у 42 (12,3 %) больных, внутрипеченочная возникла у 297 (87,1 %) и у 2 (0,6 %) пациентов носила смешанный тип (внутрипеченочный и надпеченочный).
Из 42 пациентов с внепеченочной (подпеченочной) ПГ у 9 на фоне хронических заболеваний поджелудочной железы (панкреатит, постпанкреонекротические кисты), сформировалась «левосторонняя» портальная гипертензия (обструкция селезеночной вены), проявившаяся кровотечением из варикозно-расширенных вен пищевода и выраженной спленомегалией. У одного пациента причиной ПГ стал фиброз клетчатки забрюшинного пространства, в шести случаях развился тромбоз воротной вены, посттромбофлебитическая трансформация воротной вены была выявлена во время обследования у 21 пациента, у 2-х из них сочеталась с аневризмой селезеночной артерии. Врожденные аномалии развития воротной вены были выявлены у 5 больных.
Всем пациентам проводилось комплексное обследование, включающее в себя общеклинические, лабораторные и инструментальные методы исследования. Из инструментальных методов исследования всем пациентам для осмотра пищевода, желудка и 12-перстной кишки, установки источника кровотечения и проведения дифференциальной диагностики кровотечения выполняли фиброгастродуоденоскопию (ФГДС) на аппарате «Olympus» (Япония), в последние годы эзофаговидеогастроскопию (ЭВГДС) при помощи видеокомплекса «Olympus Exera II».
Для определения проходимости воротной и селезеночной вены всем пациентам с внепеченочной ПГ выполнялось ультразвуковое исследование органов брюшной полости (печени, селезенки и поджелудочной железы, желчного пузыря) и сосудов портальной системы с определением качественных и количественных параметров кровотока на эхосканерах : Acuson Aspen (Simens) и Logic P6 PRO (GE) в В-режиме, режимах цветовой (ЦДК) и импульсноволновой (PW) эхографии по методу В.В. Митькова (2002) с использованием мультичастотных секторных датчиков 2,5–5 МГц.
Также выполнялась селективная ангиография селезеночной артерии (СА) для определения её патологии и при необходимости селективной эмболизации. Для определения проходимости, типа ветвления, особенностей внутрипеченочного расположения ВВ проводили непрямую портографию (мезентерикопортографию) на ангиографическом комплексе с С-дугой Siemens Arcadis Avantic (Германия).
В последние годы в комплекс исследования больных вошла мультиспиральная компьютерная томография (МСКТ) на аппарате «Brilliance CT 64 Slice» («Phillips Medical Systems», Нидерланды) с обязательным болюсным контрастированием. Постпроцессионную обработку результатов выполняли на рабочей станции «Extended Brilliance Workspace», входящей в комплект томографа. Пациентам на 64-срезовом томографе оценивали размеры, патологические изменения печени, селезенки, поджелудочной железы, воротной и селезеночной вены, естественных анастомозов. Для визуализации и оценки естественных шунтов и сосудов портальной системы использовали MIP-реконструкцию (проекция максимальной интенсивности) и SSD (изображение оттененных поверхностей).
Результаты исследования и их обсуждение
Все пациенты с внепеченочной (подпеченочной) ПГ обратились за помощью в хирургическую клинику РостГМУ в связи с первым проявлением заболевания (эпизодом кровотечения из варикозно-расширенных вен пищевода и желудка). Из особенностей анамнеза отмечаем, что ни у одного из больных не было выявлено маркеров вирусных гепатитов В или С. Злоупотребляли алкоголем 7 пациентов с хроническими заболеваниями поджелудочной железы из 9. Особенности клинических проявлений приведены в табл. 1.
Таблица 1
Особенности клинических проявлений внепеченочной портальной гипертензии
|
Тип ПГ |
Частота встречаемости симптомов |
|||||
|
Варикозное расширение вен пищевода и желудка |
Кровотечение в анамнезе |
Кровотечение при госпитализации |
Асцит |
Спленомегалия |
Гиперспленизм |
|
|
Внепеченочный (подпеченочный) N = 42 |
42 (100 %) |
36 (85,7 %) |
4 (9,5 %) |
0 |
42(100 %) |
30 (71,4 %) |
По результатам клинического обследования видно, что все пациенты имели варикозное расширение вен пищевода и желудка, а также спленомегалию. Свободная жидкость в животе не определялась ни у одного больного. Кровотечение в анамнезе было установлено у 36 (85,7 %) больных с подпеченочной ПГ, на высоте кровотечения поступило 4 человека (9,5 %). Причиной кровотечения было варикозное расширение вен пищевода и кардиального отдела желудка, что было подтверждено во время фиброгастродуоденоскопии. Явления гиперспленизма (анемия за счет уменьшения количества эритроцитов и падение гемоглобина, тромбоцитопения и лейкопения) были выявлены у 30 больных (71,4 %) с подпеченочной ПГ.
При анализе результатов ультразвукового исследования пациентов с подпеченочной портальной гипертензией хотим обратить внимание на отсутствие у этой категории пациентов изменений в эхоструктуре печени. Во всех случаях нами был зарегистрирован неизмененный фазный кровоток HV0 типа по печеночным венам, что свидетельствовало о сохраненной эластичности печеночной ткани. У всех больных по данным сонографии присутствовала спленомегалия, отсутствал асцит.
Чаще всего были выявлены нарушения проходимости основного ствола ВВ, развившегося вследствие тромбоза, посттромбофлебитической трансформации (ПТФС), аномалий развития ВВ, фиброза клетчатки забрюшинного пространства и сдавления ВВ за счет хронических заболеваний поджелудочной железы.
При тромбозе ВВ в ее просвете визуализировалась тромботические массы. В большинстве случаев тромбоз носил окклюзирующий характер, стенка вены чаще всего была утолщена. При ПТФС динамическое наблюдение за просветом ВВ позволило выявить появление кровотока внутри тромботических масс и пристеночно (рис. 1).
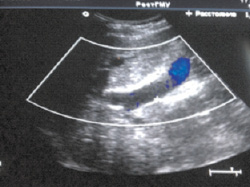
Рис. 1. Тромбоз воротной вены (собственное наблюдение)
При кавернозной трансформации ВВ в воротах печени не удавалось визуализировать единый основной ствол. ВВ была представлена множеством венозных сосудистых структур размером от 3,5 мм до 1,3 см – каверном. Кровоток в этих сосудистых образованиях имел смешанный характер (рис. 2 (а,б)).
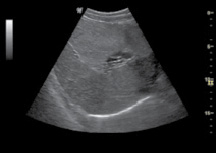
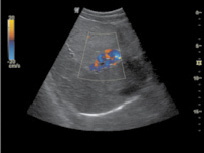
Рис. 2. Кавернозная трансформация воротной вены (собственное наблюдение): а – В-режим; б – режим ЦДК
Из-за разнообразия причин подпеченочной ПГ сложно провести анализ изменений портального кровотока, поэтому мы остановились на общих признаках дифференциальной диагностики. При выявлении увеличения максимальной скорости кровотока по СВ в воротах селезенки и возникновения турбулентного характера чаще всего во время оперативного вмешательства были выявлены артерио-венозные фистулы, но не во всех случаях, подтвержденные результатами ультразвукового исследования.
Надпеченочная форма ПГ в изолированном виде нами не выявлялась. Лишь у 2 пациенток нами был установлен смешанный тип ПГ за счет полинодулярной трансформации печени и гипоплазии нижней полой вены в области впадения печеночных вен с деформацией и стенозом их устьев в одном случае и полинодулярной трансформация печени со стенозом печеночных вен и нижней полой вены в другом случае. Поставить этот диагноз нам удалось при выполнении биопсии печени (инцизионной) и оценке результатов мультиспиральной компьютерной томографии брюшной полости с болюсным контрастированием.
У пациентов с аневризмой селезеночной артерии (СА) и артериовенозными свищами ворот селезенки возникла необходимость выполнения целиакографии, а в 2 наблюдениях и эмболизации селезеночной артерии перед спленэктомией.
У 12 пациентов с внепеченочной ПГ для визуализации вен портальной системы, путей портального шунтирования выполняли непрямую портографию. Ангиографическая картина ВВ и ее ветвей при этом исследовании достаточно информативна при тромбозе ВВ (определяется сужение просвета или его отсутствие). При кавернозной трансформации ВВ представлена конгломератом венозных коллатералей, нередко с признаками тромбоза. Косвенными признаками артериовенозных соустий ворот селезенки является ускоренное заполнение селезеночной вены во время селективной ангиографии СА, хотя само соустье ни в одном случае нами не было визуализировано.
Оценивая результаты МСКТ с болюсным контрастированием, хочется отметить, что выявить тромбы в просвете ВВ достаточно сложно. Достоверным признаком тромбоза является отсутствие контрастного вещества в зоне локализации ВВ. После наступления реканализации определяется дефект контрастирования в просвете ВВ. Кавернозная трансформация ВВ определяется по данным МСКТ в виде множественных портопортальных и портокавальных анастомозов в воротах печени. Пациентам же с «левосторонней» ПГ диагноз постпанкреонекротических кист поджелудочной железы, вызывающих сдавление СВ, был поставлен именно по результатам этого исследования (рис. 3).
Таким образом, всем 42 пациентам был подтвержден диагноз внепеченочной (подпеченочной) ПГ. Распределение больных в зависимости от вида операции представлено в табл. 2.
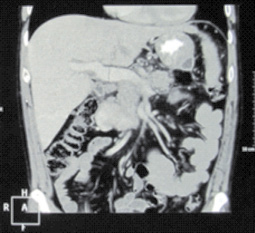
Рис. 3. Постпанкреонекротическая киста хвоста поджелудочной железы, сдавливающая селезеночную вену, «левосторонняя портальная гипертензия» (собственное наблюдение)
Таблица 2
Распределение пациентов с внепеченочной ПГ по виду оперативных вмешательств
|
Вид операции |
Число больных |
|
Спленэктомия |
19 |
|
Спленэктомия + перевязка артерио-венозных свищей ворот селезенки |
12 |
|
Спленэктомия + резекция аневризмы селезеночной артерии |
2 |
|
Спленэктомия + каудальная резекция поджелудочной железы |
4 |
|
Эмболизация селезеночной артерии |
2 |
|
Всего |
39 |
Большинство хирургов в условиях неустойчивого гемостаза отдают предпочтение неоперативным методам лечения, включающим коррекцию гиповолемии, адекватную гемотрансфузию (при необходимости), гемостатические процедуры (применение медикаментов, баллонную тампонаду пищевода и кардии), эндоскопическую склеротерапию и лигирование [4].
Применение селективных вазоконстрикторов из группы аналогов соматостатина у больных с варикозными пищеводно-желудочными кровотечениями является общепризнанным. Применение неселективных бета-адреноблокаторов предпочтительно для профилактики кровотечения, вазопрессин имеет серьезные побочные эффекты, нитроглицерин недостаточно результативен. Приведенные факторы позволяют считать аналоги соматостатина и терлипрессин в большинстве клинических случаев средством предпочтения [13, 14, 15].
В сочетании с фоновой патологией синдром гиперспленизма представляет для пациента серьезную опасность, а иногда и угрозу жизни. Выраженная тромбоцитопения в сочетании с коагулопатией повышает риск гибели от кровотечения многократно [4, 12].
Вопросы сохранения или удаления селезенки при ПГ неоднократно обсуждались в отечественной и зарубежной литературе. Эта проблема остается актуальной и в настоящее время, что подчеркивается разноречивыми и в основном малоутешительными результатами операции спленэктомии, которая доминировала в хирургии ПГ более столетия.
П.М. Хамидов (1983), М.Д. Пациора, А.Г. Шерцингер (1984), П.Н. Напалков, А.Е. Борисов (1985), И.А. Поршенников и соавт. (2011), Ю.В. Хоронько и соавт. (2013) считают спленэктомию показанной операцией, если имеют место выраженные клинические проявления гиперспленизма (анемия за счет уменьшения количества эритроцитов и падение гемоглобина, тромбоцитопения и лейкопения), а также А.Н. Чалый и соавт. (1997), Э.В. Могилевец (2011), В.Л. Коробка (2012) считают, что выполнение спленэктомии оправдано при левосторонней портальной гипертензии.
Выполнение оперативных вмешательств пациентам по поводу подпеченочной портальной гипертензии, представленных в работе, было определено в первую очередь явлениями гиперспленизма в 30 наблюдениях (71,4 %). Такие находки, как артериовенозные свищи ворот селезенки только в 2 наблюдениях были выявлены до операции, в остальных же 10 случаях были обнаружены интраоперационно (рис. 4). Такие диагностические приемы, как выполнение ангиографии и МСКТ не помогли выявить данную патологию, и только в 2 случаях косвенные признаки изменения характера венозного кровотока по селезеночной вене помогли заподозрить наличие свищей.
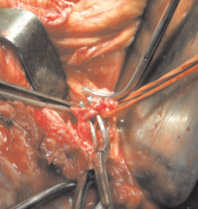
Рис. 4. Перевязка артериовенозного свища ворот селезенки (собственное наблюдение)
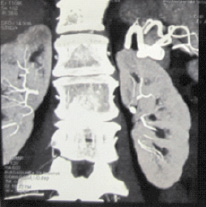
Рис. 5. Аневризма селезеночной артерии (собственное наблюдение)
Аневризму селезеночной артерии в одном наблюдении установили до операции по данным МСКТ (рис. 5), в другом наблюдении она стала также интраоперационной находкой. Сложностью операции спленэктомии были большие размеры селезенки от 24 до 42 см (вертикальный размер) и от 7 до 15 см (горизонтальный размер). Каудальную резекцию поджелудочной железы одновременно со спленэктомией выполняли по поводу постпанкретонекротических кист железы, причем все 4 пациента злоупотребляли алкоголем и перед операцией нами исключался алкогольный цирроз печени (ЦП). Для подтверждения диагноза подпеченочной ПГ всем пациентам выполняли биопсию печени (инцизионную при оперативном вмешательстве) и пункционную, если операцию не выполняли. Во всех наблюдениях был исключен внутрипеченочный тип ПГ.
Выводы
Внепеченочная ПГ по результатам нашего исследования встречалась в 12,3 % случаев заболевания. Изолированно надпеченочная ПГ не была установлена ни в одном наблюдении из 341 и только в 2 случаях (0,6 %) носила смешанный тип (внутрипеченочный и надпеченочный). Скрининг – исследованием является фиброгастродуоденоскопия, в 100 % наблюдений выявившая варикозное расширение вен пищевода и желудка. Ни один из инструментальных методов обследования не является основным в диагностике внепеченочной ПГ и только умелое сочетание нескольких методов дает положительный эффект в установке диагноза. Хотя наиболее информативным из неинвазивных методов исследования для определения вариантов патологии ВВ и СВ является ультразвуковой метод. Показанием к операции спленэктомии является гиперспленизм, выявленный в 71,4 % наблюдений, а также артериовенозные свищи ворот селезенки и аневризма селезеночной артерии. При ПГ, вызванной изменениями со стороны поджелудочной железы и сдавлением или окклюзией СВ оптимальным способом коррекции является резекция поджелудочной железы при кистах со спленэктомией или изолированная спленэктомия. Эмболизация селезеночной артерии не может быть самостоятельным методом лечения ПГ, а предполагает дальнейшее удаление селезенки, показанием для которой является гиперспленизм.
Рецензенты:
Хоронько Ю.В., д.м.н., заведующий кафедрой оперативной хирургии и топографической анатомии, ГБОУ ВПО «Ростовский государственный медицинский университет» Минздрава России, г. Ростов-на-Дону;
Грошилин В.С., д.м.н., заведующий кафедрой хирургических болезней № 2, ГБОУ ВПО «Ростовский государственный медицинский университет» Минздрава России, г. Ростов-на-Дону.
Работа поступила в редакцию 10.12.2013.
Библиографическая ссылка
Сапронова Н.Г., Ерошенко О.Л., Косовцев Е.В., Блинов И.М. ОСОБЕННОСТИ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ВНЕПЕЧЕНОЧНОЙ ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ // Фундаментальные исследования. 2013. № 9-6. С. 1139-1145;URL: https://fundamental-research.ru/en/article/view?id=32913 (дата обращения: 02.05.2026).



