Scientific journal
Fundamental research
ISSN 1812-7339
"Перечень" ВАК
ИФ РИНЦ = 1,798
MATERIAL «LITAR» AND BIG DEFECTS OF BONE FABRIC
Известно, что стандартно принятыми способами решения задач по заполнению больших дефектов и полостей костной ткани являются методики применения естественных и искусственных материалов (ксено-, гетеро-, алло- и аутотрансплантатов) [1, 2]. Все вышеперечисленные материалы можно разделить на биодеградируемые и небиодеградируемые [3]. Биодеградируемые материалы за время нахождения в реципиентной зоне проходят несколько стадий биотрансформации, каждая из которых влияет на скорость формирования и роста нативной костной ткани в зоне замещения костного дефекта.
Наиболее распространенным из вышеперечисленных способов является использование свободных костных аутотрансплантатов, важнейшими преимуществами которого являются абсолютная тканевая совместимость, отсутствие опасности внесения в организм больного экзогенного инфекционного начала и отсутствие реакции «трансплантат-хозяин». Недостатком аутотрансплантатов является ограниченный замещаемый объем даже в случае полифокального забора кости, трудности моделирования дефекта, неизбежность нарушения ростковой зоны в хирургии детского возраста.
Таким образом, при необходимости удалить достаточно большей фрагмент костной ткани, невозместимый аутотрансплантатами (будь то опухолевое образование, или очаг воспаления костной ткани) хирург становится бессильным оказать помощь больному в условиях отсутствия банка костных гетеротрансплантатов.
На базе кафедры травматологии, ортопедии и ВЭМ Пензенского государственного медицинского института проведен ряд оперативных вмешательств с использованием материала «ЛитАр» (гидроксоапатит-коллагенового композита). Гидроксоапатит (иногда его неверно называют гидроксиапатит [4], можно называть апатит) является основой неорганического матрикса костной ткани[1], биосовместим с тканями человека и не вызывает реакции отторжения.
Он стимулирует остеогенез. После заполнения костных полостей биотрансформация коллаген-апатитового комплекса проходит стадию формирования мягкотканевой структуры, что длится около 10–15 дней.
Далее образовавшаяся соединительная ткань начинает оссифицироваться, что в конечном счете приводит к формированию полноценной костной структуры [6].
Цель. Данная работа посвящена изучению поведения композитного препарата материала «ЛитАр», содержащего коллаген и гидроксофосфат кальция (гидроксоапатит) при замещении дефектов костной ткани у больных с различной травматолого-ортопедической патологией.
Материалы и методы исследования
«ЛитАр» является гидроксоапатит-коллагеновым композитом, отличающимся от других имплантатов подобного рода минимальным временем биодеградации, составляющим 15–20 дней. «ЛитАр» состоит из гидроксофосфата кальция (апатита) (около 80 %), введенного в объем ксеногенного коллагена специальной технологией, защищенной патентом РФ. Материал имеет 70 % пористости, что обеспечивает его быструю васкуляризацию. «ЛитАр» представляет собой пластины серо-желтого цвета, набухающие в биологических жидкостях, при этом полностью восполняющие полость дефекта [6]. Имплантат мало рентгеноконтрастен, его оптическая плотность до 100 Хаунсфилда, но в случае присоединения ионов железа из кровяного сгустка исходная оптическая плотность может быть 150–200 Х). Контроль образования в зоне костного дефекта остеорегенерата осуществлялся методом ренгенологического и компьютерно-томографического (КТ) исследования с интервалами в 1 мес.
Результаты исследования и их обсуждение
За 2003–2004 годы материалом «ЛитАр» было пролечено 10 пациентов с различными нозологиями. Композит применялся как изолированно, так и с использованием аутотрансплантатов (4 наблюдения).
У 5 больных с замещением дефектов костной ткани 70 см³ и более в раннем послеоперационном периоде (7–10 день) отмечались выделения из области послеоперационного шва в виде жидкости сливкообразной консистенции, светлого цвета, без запаха на фоне нормальной температуры тела и без признаков местного воспаления и отсутствия воспалительных изменений в анализах крови. При неоднократных посевах данного выделяемого на различных средах роста микрофлоры не наблюдалось, что позволило сделать вывод о том, что выделения не носят воспалительной этиологии, а являются следствием использования большего объема материала «ЛитАр», нежели было необходимо в данном конкретном случае. Учитывая способность композита увеличиваться в объеме при контакте с биологическими жидкостями [7], вышеописанное объяснялось самопроизвольной эвакуацией имплантата по пути наименьшего сопротивления – через послеоперационную рану. Все наблюдаемые свищи (у 2-х больных) самопроизвольно купировалились к 20–25 дню с момента проведенного оперативного вмешательства. При проведении последующих оперативных вмешательств объем имплантируемого материала «ЛитАр» был уменьшен до 2/3 от объема имеющейся операционной полости, в результате чего повторных случаев формирования асептического свища не наблюдалось.
В качестве клинического примера приводим случай пациентки. В., 52-х лет, поступила в отделение травматологии с диагнозом: Остеобластокластома обоих мыщелков правой бедренной кости. Патологический перелом дистального метафиза правой бедренной кости, без смещения отломков. Из анамнеза: считает себя больной на протяжении 1,5 лет, когда впервые отметила появление болей в области правого коленного сустава. Обращалась за медицинской помощью по месту жительства, проводилась рентгенография правого коленного сустава. На данном этапе патология не диагностирована. Спустя 6 месяцев вновь обратилась с прежними жалобами, проведена рентгенография, по результатам которой выставлен диагноз остеобластокластомы. Больная направлена в Областной онкологический диспансер, где проведен курс лучевой терапии. Спустя 10–12 месяцев с момента от начала заболевания, больная была вынуждена перейти на ходьбу с дополнительной опорой на ортопедическую трость, стала выраженной хромота. За 2 недели до госпитализации при незначительной нагрузке произошел патологический перелом дистального метафиза правой бедренной кости. На момент госпитализации образование занимало 3/4 мыщелков правой бедренной кости (рис. 1).
Больной после предварительной гистологической верификации опухолевого образования произведено оперативное вмешательство в объеме экскохлеации опухоли с замещением образовавшейся полости аутотрансплантатами из крыльев подвздошных костей и «ЛитАром» (предварительно обработав костную полость раствором йодопирона и антибиотиками цефалоспоринового ряда, после чего полость прикрыта местными тканями), с фиксацией внеочаговым аппаратом, необходимость наложения которого была обусловлена наличием патологического перелома на уровне дистального метафиза правой бедренной кости. Суммарный замещенный дефект составил около 200 см³ (рис. 2).
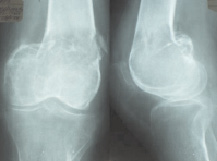
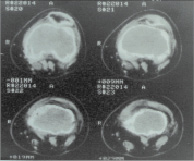
Рис. 1. Рентгенограмма (а) и КТ (б) пациентки В. до операции
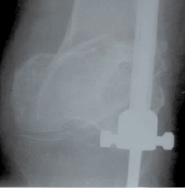
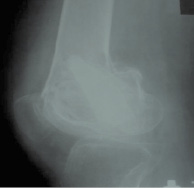
Рис. 2. Рентгенограмма пациента В. после заполнения дефекта аутокостью и материалом «ЛитАр» (плохо рентгеноконтрастен, его исходная оптическая плотность 60–100 Х)
Контрольные рентгенографии проводились каждые 30 дней. Спустя 2 мес. с момента оперативного вмешательства определялись достоверные признаки консолидации перелома (рис. 3), на основании чего аппарат после проведения клинической пробы демонтирован.
Мы предполагаем, что заполнение места установки препарата «ЛитАр» полноценной костной тканью произошло к 3 мес. с момента оперативного вмешательства (рис. 4).
Спустя 12 месяцев с момента проведенного оперативного вмешательства на контрольной рентгенограмме и компьютерной томограмме существенных изменений плотности костной ткани в зоне заполненного дефекта не отмечено, что может свидетельствовать о завершенности процесса перестройки трансплантатов в срок до 3 месяцев. Нозологические группы и объем интраоперацинных дефектов костной ткани приведены в таблице.
Принимая во внимание способность материала «ЛитАр» хорошо растворяться в анестезирующем препарате, физиологическом растворе, не теряя при этом своих свойств, проведено пункционное введение препарата в дистракционный регенерат с целью его стимуляции и заполнения формирующегося его дефекта. Во всех случаях получено заполнение костных дефектов и полостей полноценной костной тканью, что подтверждено клиническими и дополнительными методами исследования.
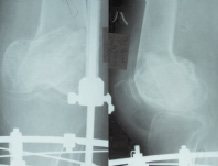
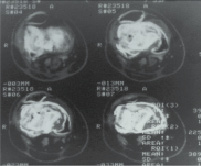
Рис. 3. Рентгенограммы (а) и КТ (б) пациента В. через 2 мес. после операции
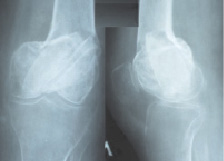
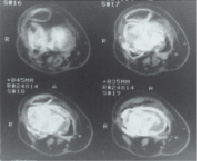
Рис. 4. Рентгенограмма и КТ пациента В. через 3 мес. после операции
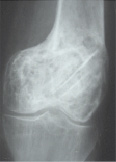
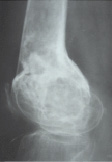
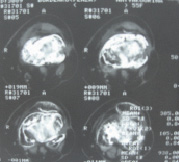
Рис. 5. Рентгенограмма и КТ пациента В. через 12 мес. после операции
Нозологические группы и объем интраоперацинных дефектов костной ткани
|
Нозология |
Кол-во больных |
Объем интраоперационного дефекта |
|
1. ОБК мыщелков бедренной кости |
1 |
200 см³ |
|
2. Последствия переломов тел позвонков с формированием кифотической деформации 70–90° |
3 |
12 см³ |
|
3. ОБК метафиза большеберцовой |
2 |
70 см³ |
|
4. Киста шейки бедренной кости |
1 |
7 см³ |
|
5. Ложный сустав бедренной кости, болтающаяяся форма |
1 |
2 см³ |
|
6. Дефект формирующегося дистракционного регенерата |
1 |
5 см³ |
|
7. Ложный сустав лучевой кости |
1 |
1 см³ |
|
8. Остеомиелит бедра |
1 |
3 см³ |
Вывод
Результаты показывают, что лечение больных способом замещения дефектов костной ткани с применением композита «ЛитАр» позволило добиться заполнения больших дефектов полноценной костной тканью и сократило средние сроки лечения по сравнению со средними сроками лечения больных с аналогичными нозологиями (3 месяца при использовании «ЛитАр» против 5–6 месяцев при перестройке аутотрансплантанов). Достоинством материала «ЛитАр» является возможность его применения в целях замещения больших дефектов костной ткани, не прибегая к использованию костного банка. Благодаря особенностям имплантата «ЛитАр» полноценная костная ткань при замещении больших дефектов костной ткани формируется в сроки значительно меньшие, чем обычно, что в свою очередь уменьшает затраты на лечения и улучшает качество жизни у больных с заболеваниями, требующими замещения больших дефектов костной ткани.
Рецензенты:Измалков С.Н., д.м.н., профессор, директор ИПО, проректор по последипломному образованию и лечебной работе, заведующий кафедрой травматологии и ортопедии Самарского государственного медицинского университета, лауреат премии Правительства РФ, заслуженный врач РФ, г. Самара;
Моисеенко В.А., д.м.н., профессор, заведующий кафедрой травматологии и ортопедии, гбоу дпо «Пензенский институт усовершенствования врачей» Министерство здравоохранения Российской Федерации, г. Пенза.
Библиографическая ссылка
Митрошин А.Н., Кислов А.И., Литвинов С.Д., Кибиткин А.С., Абдуллаев А.К. МАТЕРИАЛ «ЛИТАР» И БОЛЬШИЕ ДЕФЕКТЫ КОСТНОЙ ТКАНИ // Фундаментальные исследования. 2013. № 9-6. С. 1061-1065;URL: https://fundamental-research.ru/en/article/view?id=32896 (дата обращения: 02.05.2026).



